Clear Sky Science · pl
Eksperymentalna i teoretyczna ocena zależnego od geometrii załadowania doksorubicyny na nanocząstki tlenku ceru przy użyciu modelowania oddziaływań van der Waalsa
Dlaczego kształt malutkich nośników leków ma znaczenie
Leki przeciwnowotworowe, takie jak doksorubicyna, są silne, ale mogą uszkadzać zdrowe tkanki. Jedną ze strategii zwiększenia ich bezpieczeństwa jest przytwierdzenie ich do nanocząstek, które dostarczają lek bezpośrednio do guza. W tym badaniu postawiono z pozoru proste pytanie o dalekosiężnych konsekwencjach: czy kształt nanocząstki — czy przypomina kulkę, pręt czy arkusz — wpływa na to, ile leku może zabrać i jak skuteczne będzie jego działanie?
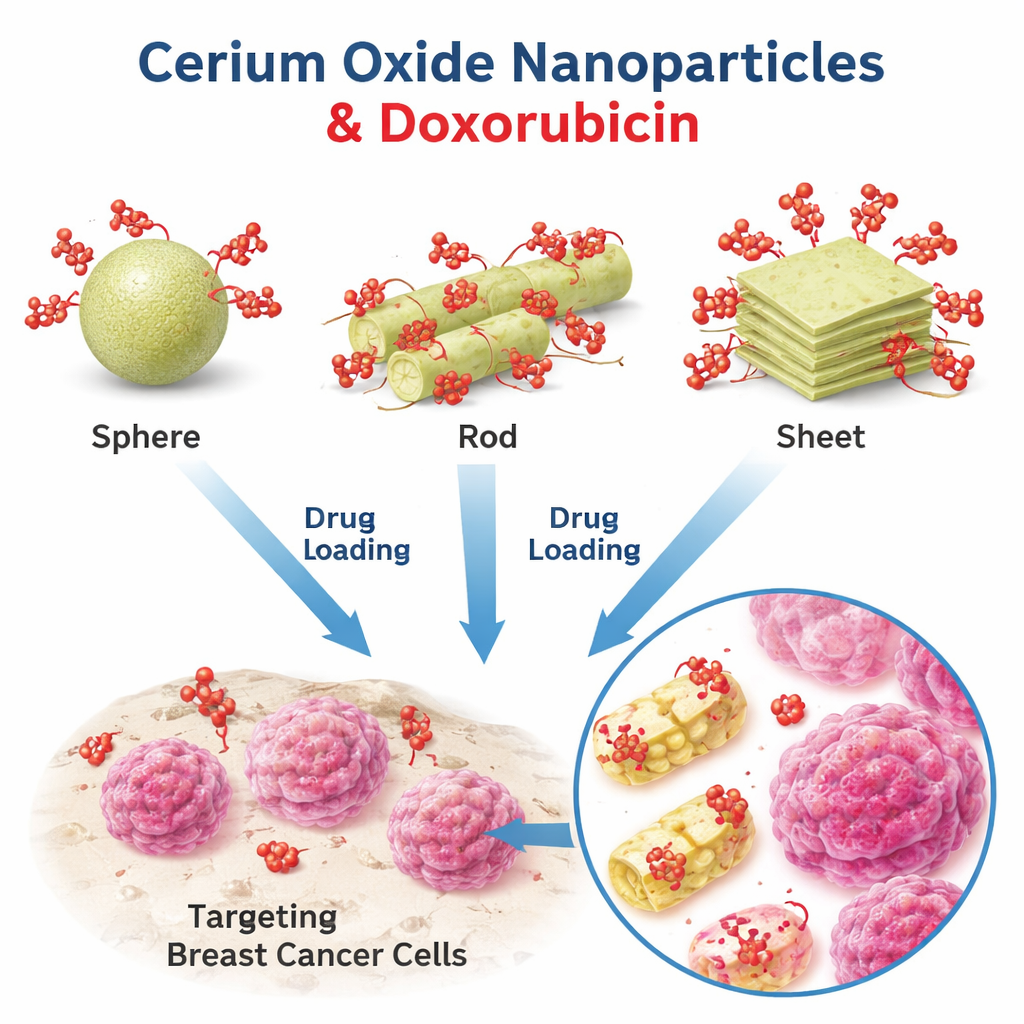
Trzy malutkie kształty, jeden lek przeciwnowotworowy
Naukowcy skupili się na nanocząstkach z tlenku ceru, materiale już znanym z właściwości antyoksydacyjnych, antybakteryjnych i wspomagających gojenie, i zbadali jego potencjał jako nośnika doksorubicyny — powszechnie stosowanego leku chemioterapeutycznego. Przygotowali trzy odrębne kształty tlenku ceru: niemal idealne kule, walcowate pręty i cienkie, płaskie płatki. Za pomocą mikroskopii elektronowej i pomiarów rozproszenia światła potwierdzili rozmiary i kształty cząstek: kule tworzyły zwartych ziarn, cylindry przypominały smukłe pręciki, a płatki szerokie, płaskie warstwy. Ten kontrolowany zestaw kształtów pozwolił im zbadać, jak sama geometria wpływa na zachowanie leku, przy niezmienionym materiale.
Pomiary, ile leku może znieść każdy kształt
Aby sprawdzić, jak skutecznie każdy kształt może przenosić doksorubicynę, zespół wymieszał nanocząstki z roztworem leku, a następnie zmierzył, ile leku pozostało w cieczy. Mniej pozostałego leku oznaczało, że więcej zostało załadowane na cząstki. Przy użyciu precyzyjnych metod optycznych (spektroskopia UV–widzialna i fluorescencyjna) stwierdzili, że nanocząstki kuliste załapały najwięcej doksorubicyny — około 86% leku znalazło się na lub w kulach. Na drugim miejscu były cylindry — około 79%, a na końcu płatki — około 67%. Gdy te nośniki z załadowanym lekiem przetestowano na agresywnej linii komórek raka piersi, formulacja z kulkami ponownie okazała się najbardziej skuteczna w zabijaniu komórek nowotworowych, następnie cylindry, a potem płatki. Co ciekawe, kule także uwalniały lek najwolniej w czasie, co sugeruje, że duże załadowanie połączone z powolnym uwalnianiem może zwiększać działanie leku wewnątrz komórek.
Wprowadzenie matematyki do świata nano
Obok pracy laboratoryjnej badacze zbudowali model analityczny — swego rodzaju uproszczony matematyczny mikroskop — aby obliczyć, jak silnie pojedyncza, w przybliżeniu kulista cząsteczka doksorubicyny powinna przylegać do każdego kształtu nanocząstki. Skoncentrowali się na siłach van der Waalsa, słabych lecz wszechobecnych przyciąganiach, które pomagają cząsteczkom przylegać do siebie. Traktując lek jako małą kulkę blisko sferycznej, cylindrycznej lub płaskiej powierzchni tlenku ceru, wyprowadzili dokładne formuły na energię oddziaływania podczas zbliżania się lub odsuwania leku. Te rachunki pozwoliły przewidzieć, który kształt powinien zapewnić najbardziej stabilne związanie — zarówno gdy lek jest schowany wewnątrz cząstki, jak i gdy leży na powierzchni — bez uruchamiania dużych symulacji komputerowych.
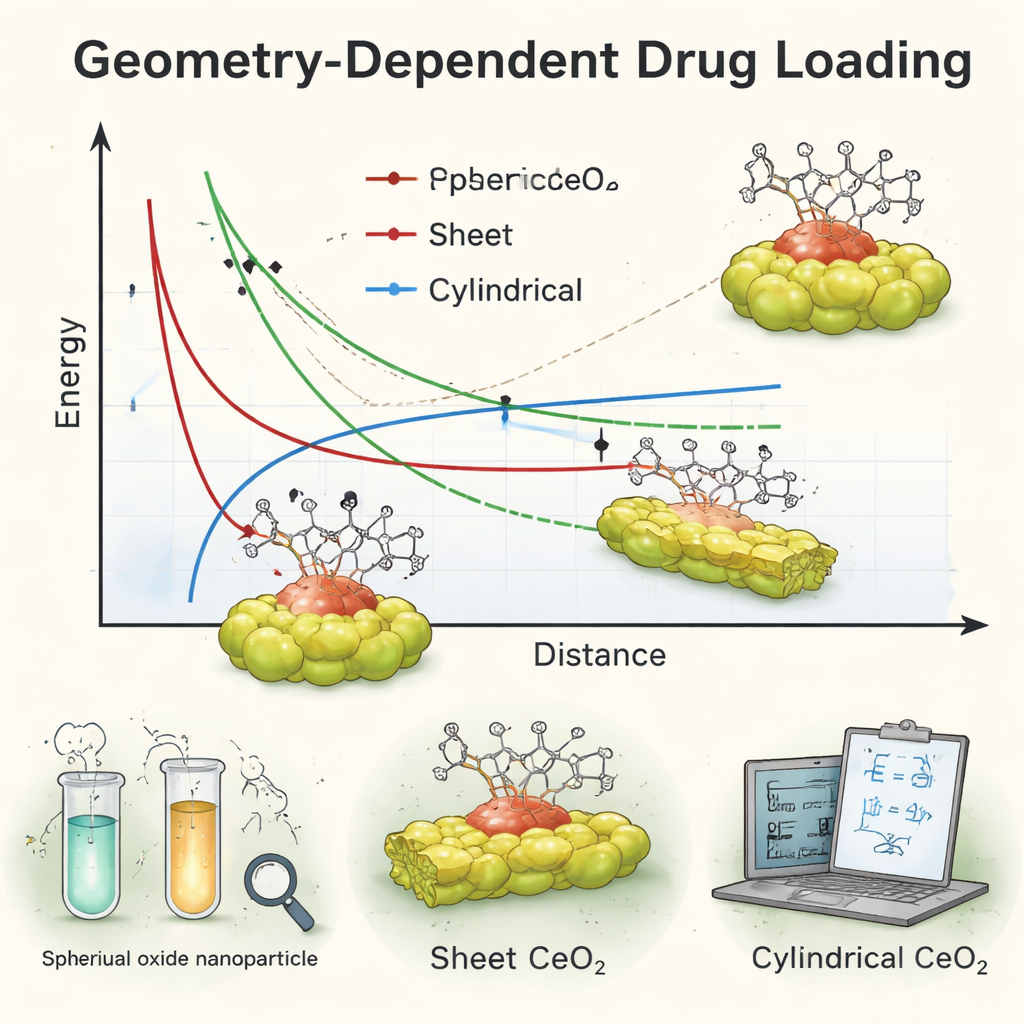
Gdzie teoria się zgadza — i gdzie zawodzi
Porównując swoje równania z danymi eksperymentalnymi, zespół znalazł uderzające, częściowe dopasowanie. Matematyka sugerowała, że cząstki o kształcie kulistym i płaskim powinny wiązać doksorubicynę z bardzo podobną siłą, co dobrze pasowało do ogólnie wysokiego załadowania obserwowanego dla tych dwóch kształtów. Ponadto, gdy przyjęto, że lek jest uwięziony wewnątrz cząstek, kule wyszły nieco stabilniej niż pozostałe kształty, co odzwierciedlało silne wyniki nośników kulistych w laboratorium. Jednak pojawiła się zagadka: model przewidywał relatywnie słabsze wiązanie dla cylindrów, podczas gdy eksperymenty pokazały, że cząstki w kształcie prętów i tak załadowywały lek dość efektywnie — prawie tak samo dobrze jak kule. Ta rozbieżność, szczególnie dla kształtu cylindrycznego, ujawniła, że prosty model traktujący otoczenie jako próżnię i uśredniający szczegóły powierzchni nie jest w stanie w pełni uchwycić rzeczywistego zachowania systemów lek–nanocząstka zanurzonych w cieczy i oddziałujących z komórkami.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
Dla nie-specjalistów przesłanie jest dwojakie. Po pierwsze, kształt nanocząstki to nie detal kosmetyczny; bezpośrednio wpływa na to, ile leku przeciwnowotworowego może przenosić, jak szybko go uwalnia i jak silnie może atakować komórki nowotworowe. Kuliste cząstki tlenku ceru w tym badaniu okazały się szczególnie obiecującymi nośnikami dla doksorubicyny, łącząc wysokie załadowanie, silne działanie przeciwnowotworowe i powolne wyciekanie leku. Po drugie, badanie pokazuje ograniczenia nawet eleganckich modeli matematycznych, gdy upraszczają one zbyt mocno złożoną rzeczywistość biologii. Aby projektować naprawdę niezawodne nanoleki, w przyszłości trzeba będzie łączyć szczegółowe eksperymenty z bardziej wyrafinowanymi teoriami uwzględniającymi wodne środowisko, złożone powierzchnie cząstek i ich agregację. Razem te postępy mogą doprowadzić do inteligentniejszych projektów nanocząstek, które dostarczają silne leki bezpieczniej i skuteczniej.
Cytowanie: Sripaturad, P., Keo, S., Wongpan, A. et al. Experimental and theoretical evaluation of geometry-dependent doxorubicin loading onto cerium oxide nanoparticles via van der Waals interaction modeling. Sci Rep 16, 6169 (2026). https://doi.org/10.1038/s41598-026-36893-5
Słowa kluczowe: nanomedycyna, nanocząstki tlenku ceru, dostarczanie doksorubicyny, geometria nanocząstek, terapia raka piersi