Clear Sky Science · pl
Synteza i ocena przeciwnowotworowa nowych pochodnych tioimidazolu zawierających motyw trimetoksyfenylowy
Nowe narzędzia chemiczne w walce z rakiem
Leki chemioterapeutyczne często uszkadzają zdrowe komórki razem z guzem, powodując poważne skutki uboczne. W tym badaniu zbadano nową rodzinę syntetycznych cząsteczek, które mają na celu silniejsze uderzenie w komórki nowotworowe przy ograniczonym wpływie na tkanki zdrowe. Poprzez sprytne połączenie dwóch bloków budulcowych już znanych z zastosowań farmaceutycznych, badacze stworzyli związki wykazujące silne, ukierunkowane działanie zabójcze wobec komórek nowotworowych w badaniach in vitro i modelach 3D guzów, jednocześnie pozostawiając komórki zdrowe w dużej mierze nietknięte.
Projektowanie „mądrzejszych” cząsteczek zabijających raka
Zespół skupił się na dwóch „uprzywilejowanych” strukturach chemicznych, które pojawiają się wielokrotnie w skutecznych lekach. Jedną z nich jest imidazol — małe pierścieniowe ugrupowanie dobrze dopasowujące się do wielu biologicznych celów. Drugim jest grupa trimetoksyfenylowa (TMP), układ trzech łańcuchów zawierających tlen na pierścieniu aromatycznym, kluczowy w kilku lekach przeciwnowotworowych zaburzających podział komórek. Dodając atom siarki do rdzenia imidazolu (tworząc tioimidazol) i łącząc go z grupą TMP, chemicy liczyli na dopracowanie właściwości farmakokinetycznych oraz siły wiązania z białkami związanymi z nowotworami. Stosując etapową syntezę, zbudowali bibliotekę powiązanych związków, z których każdy został subtelnie zmodyfikowany, aby sprawdzić, które cechy mają największe znaczenie dla aktywności przeciwnowotworowej. 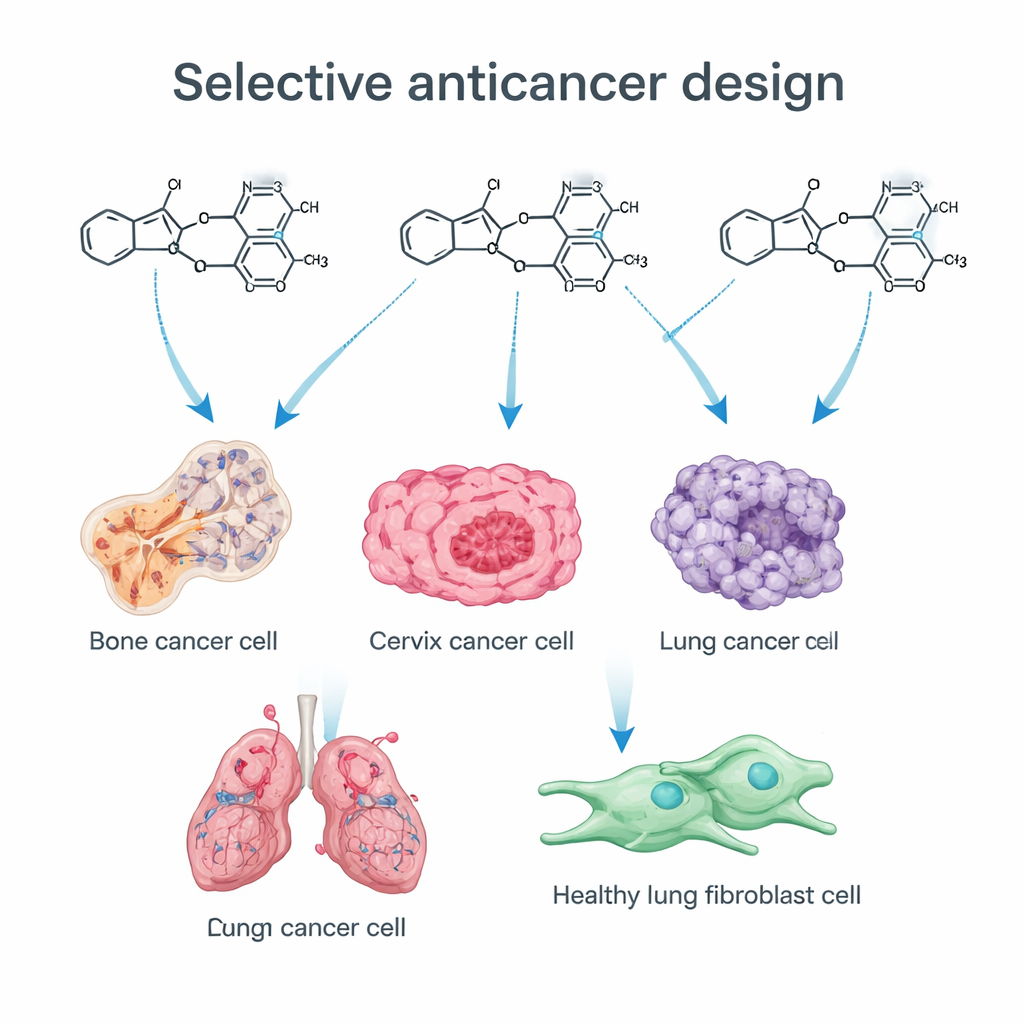
Testowanie działania na komórkach nowotworowych przy jednoczesnym oszczędzaniu tkanek zdrowych
Nowe związki testowano na czterech ludzkich liniach komórek nowotworowych — osteosarcoma (kość), rak szyjki macicy, rak jelita grubego i rak płuc — oraz na niekancerogennych fibroblastach płucnych. Wiele z badanych związków hamowało lub zatrzymywało wzrost komórek nowotworowych, ale jeden z nich, oznaczony jako 13b, wyróżnił się szczególnie. Zabijał komórki raka kości i szyjki macicy w bardzo niskich stężeniach, a jednocześnie nie wykazywał wykrywalnej toksyczności wobec normalnych fibroblastów nawet przy dawkach ponad 60 razy wyższych. Kilka innych związków było umiarkowanie silnych, lecz mniej selektywnych, co podkreśla, jak niewielkie zmiany strukturalne — na przykład wprowadzenie atomu chloru lub grupy nitrowej w określonych pozycjach — mogą przesunąć równowagę między ogólną toksycznością a działaniem ukierunkowanym na nowotwór.
Jak związek wiodący zmusza komórki nowotworowe do samozniszczenia
Aby zrozumieć, co 13b robi wewnątrz komórek, badacze szukali cech charakterystycznych dla zaprogramowanej śmierci komórki, czyli apoptozy. Komórki nowotworowe traktowane 13b stawały się dodatnie w teście Annexin V oraz aktywowały enzymy kaspazy-3 i -7, klasyczne markery wskazujące, że komórka została popchnięta do uporządkowanego programu samobójczego, a nie jedynie uległa pęknięciu. Mikroskopia ujawniła jasne ogniska γH2AX, sygnał złamanych nici DNA, w jądrach leczonych komórek. Z czasem wewnętrzny szkielet komórek zaczął się rearanżować i rozpadać, szczególnie w komórkach raka szyjki macicy, które zaokrąglały się i odklejały — wizualne wskazówki, że apoptoza była w toku. Razem te obserwacje pokazują, że 13b uszkadza DNA komórek nowotworowych, a następnie napędza je w kierunku kontrolowanej ścieżki śmierci.
Z płaskich warstw komórek do mini-guzów 3D
Większość testów laboratoryjnych hoduje komórki nowotworowe w cienkich warstwach, które nie odzwierciedlają w pełni gęstej, warstwowej struktury prawdziwych guzów. Aby to uwzględnić, zespół wyhodował komórki nowotworowe w trójwymiarowe sferoidy — małe kuliste skupiska, które lepiej przypominają architekturę guza i wyzwania związane z penetracją leku. Po traktowaniu tych sferoidów 13b kurczyły się w sposób zależny od dawki. Sferoidy raka kości były szczególnie wrażliwe, stawały się małe, luźne i fragmentaryczne przy wyższych stężeniach związku. Barwienia fluorescencyjne wykazały fale apoptozy rozchodzące się od zewnętrznej warstwy sferoidu do wnętrza wraz ze wzrostem stężenia, dowodząc, że 13b potrafi przenikać i zabijać komórki w całej objętości tych zwartych struktur. 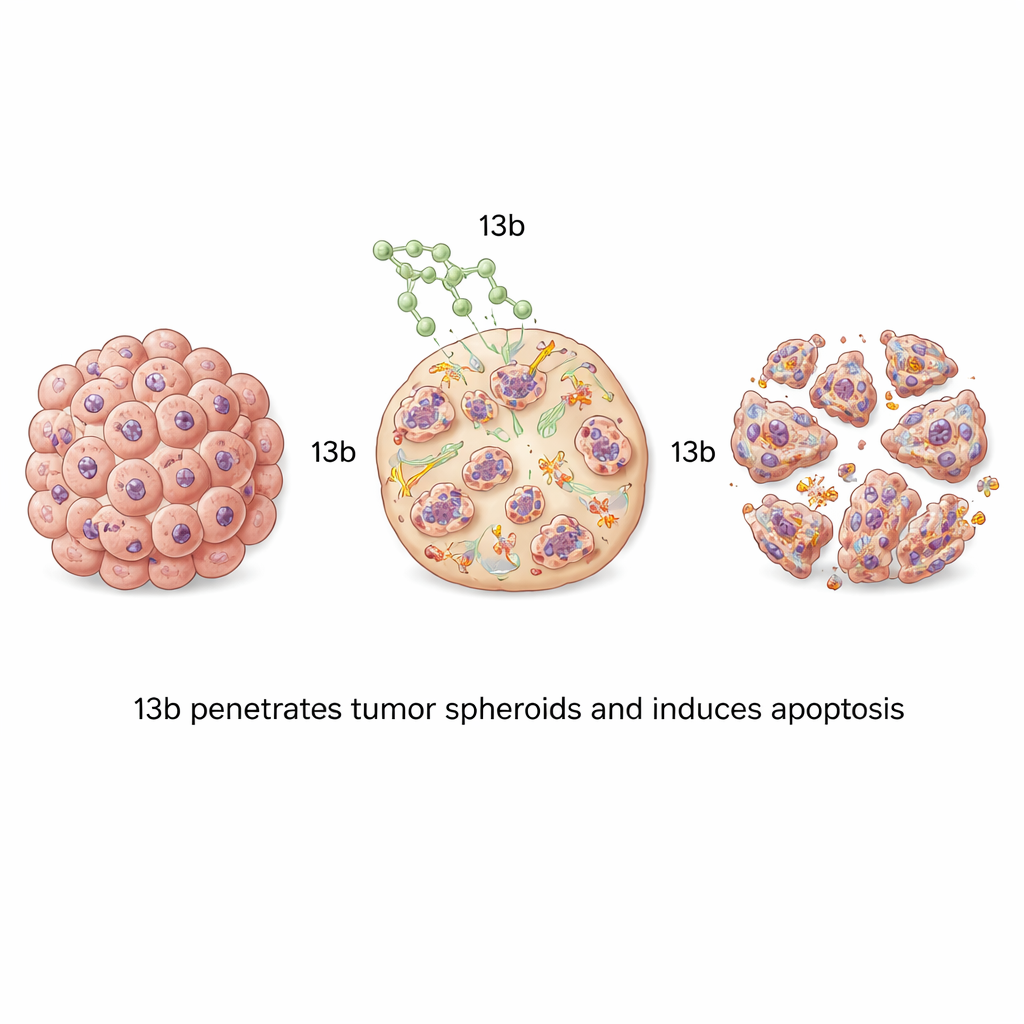
Dlaczego ta praca ma znaczenie dla przyszłych terapii przeciwnowotworowych
Dla odbiorcy niespecjalistycznego kluczowy wniosek jest taki, że badacze stworzyli nową klasę małych cząsteczek łączących najlepsze cechy dwóch sprawdzonych komponentów leków w jedną hybrydową konstrukcję. Związek wiodący, 13b, potrafi rozpoznawać i efektywnie niszczyć komórki nowotworowe przy jednoczesnym ograniczonym uszkadzaniu komórek zdrowych w testach laboratoryjnych i pozostaje skuteczny nawet w bardziej realistycznych modelach 3D. Choć przed nami jeszcze wiele pracy — na przykład określenie jego dokładnych celów molekularnych, poprawa rozpuszczalności i badania in vivo — to badanie pokazuje, że łączenie ram tioimidazolu i TMP jest obiecującą strategią w opracowywaniu bardziej selektywnych i silnych środków przeciwnowotworowych.
Cytowanie: Maciejewska, N., Grybaitė, B., Anusevičius, K. et al. Synthesis and anticancer evaluation of novel thioimidazole derivatives bearing a trimethoxyphenyl moiety. Sci Rep 16, 6271 (2026). https://doi.org/10.1038/s41598-026-36890-8
Słowa kluczowe: środki przeciwnowotworowe, pochodne imidazolu, trimetoksyfenyl, apoptoza, sferoidy nowotworowe 3D