Clear Sky Science · pl
Różne mechanizmy inaktywacji SARS-CoV-2 przez anionowe środki powierzchniowo czynne: badanie porównawcze soli kwasów tłuszczowych i surfaktantów syntetycznych
Dlaczego rodzaj używanego mydła nadal ma znaczenie
Pandemia COVID‑19 uczyniła mycie rąk domowym mantrą, ale nie wszystkie mydła działają tak samo przeciwko wirusowi wywołującemu chorobę. W tym badaniu przyjrzano się pod mikroskopem powszechnym składnikom mydeł, aby ustalić, które z nich najlepiej unieszkodliwiają SARS‑CoV‑2 i w jaki sposób to robią. Wyniki mogą pomóc w lepszym wyborze codziennych mydeł i środków dezynfekujących, dzięki czemu rutynowy zabieg, jak mycie rąk, stanie się jeszcze skuteczniejszym narzędziem ochrony zdrowia.
Jak mydło atakuje tłustą osłonę
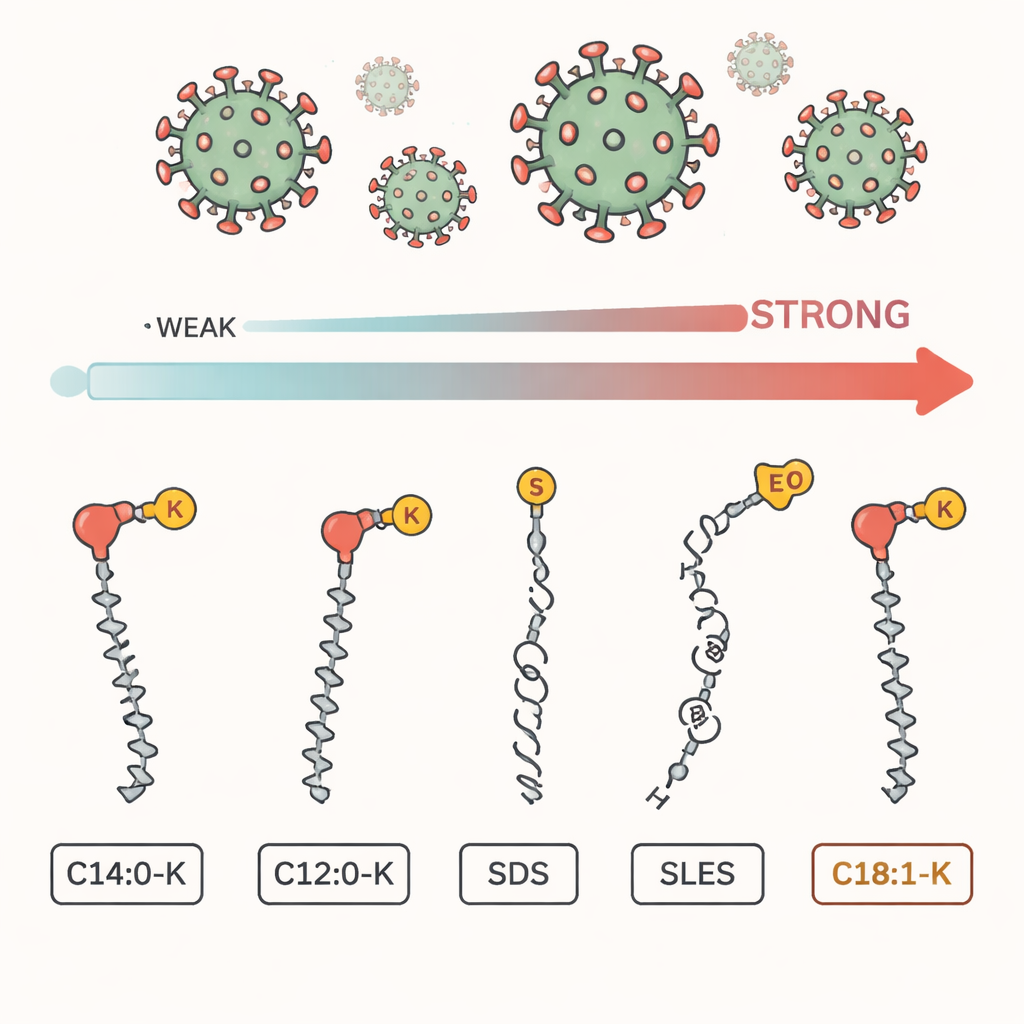
SARS‑CoV‑2, podobnie jak wiele niebezpiecznych wirusów, jest otoczony kruchą, oleistą powłoką złożoną z lipidów. Molekuły mydła mają dwie „twarze”: jedna strona lubi wodę, druga lubi tłuszcz. Gdy myjemy ręce, te molekuły wnikają w tłustą osłonę i mogą ją rozrywać, przez co wirus traci zdolność do zakażania komórek. Jednak mydła składają się z różnych składników; w badaniu porównano pięć powszechnie używanych: trzy naturalne sole kwasów tłuszczowych (w tym stearynian potasu C18:1‑K) oraz dwa powszechne syntetyczne surfaktanty, SDS i SLES, często występujące w płynnych mydłach i szamponach.
Które składniki mydła najsilniej uderzają w wirusa
Gdy badacze zmieszali wirusa z tymi surfaktantami w warunkach laboratoryjnych, jeden składnik wyróżniał się wyraźnie. C18:1‑K, naturalny komponent mydła z długim, lekko zagiętym łańcuchem, zmniejszył zakaźność wirusa o ponad 100 000‑krotnie przy bardzo niskim stężeniu. SDS, ostrzejszy składnik syntetyczny, osiągnął jedynie około dziesięciokrotnego zmniejszenia przy tym samym poziomie, natomiast SLES i krótkołańcuchowy składnik mydła C12:0‑K niemal nie inaktywowały wirusa. Ogólnie ranking był jasny: C18:1‑K działał najlepiej, potem SDS, następnie SLES, a krótsze kwasy tłuszczowe odstawały. Dłuższe, bardziej lipofilowe łańcuchy powodowały znacznie silniejszą inaktywację wirusa.
Podgląd niewidocznych starć
Aby zrozumieć, dlaczego różnice były tak duże, zespół użył techniki pomiaru ciepła do śledzenia interakcji surfaktantów z wirusem. C18:1‑K dał wzór cieplny wskazujący, że głównie wsuwa swój oleisty ogon w lipidową powłokę wirusa — proces napędzany siłami hydrofobowymi (lubiącymi tłuszcz). SDS i C12:0‑K w przeciwieństwie do tego wykazywały odwrotny typ zmian cieplnych, co sygnalizuje, że bardziej przylegają do naładowanych części białkowych na powierzchni wirusa, zamiast głęboko zaburzać powłokę lipidową. SLES wydawał się leżeć pośrodku, z właściwościami lipofilowymi i hydrofilowymi częściowo się znoszącymi. Te energetyczne odciski palców ujawniły, że różniły się nie tylko siła działania, ale też sposób ataku poszczególnych składników.
Co ujawnił mikroskop
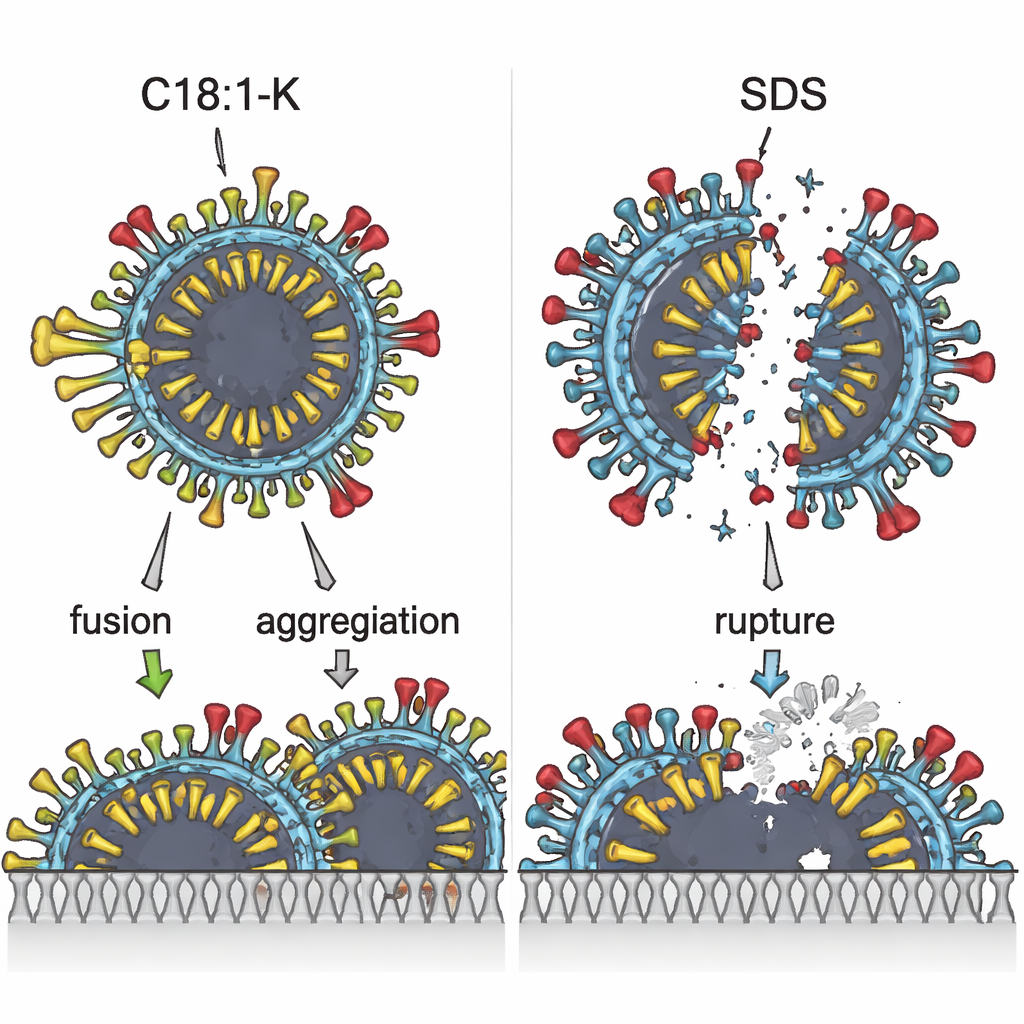
Mikroskopia elektronowa dała wizualne uzupełnienie dla tych niewidocznych zmian energetycznych. Gdy wirus był traktowany surfaktantami, które działały głównie przez przyciąganie elektryczne do białek, takimi jak SDS lub C12:0‑K, wiele cząstek wyglądało na rozdzierane lub pęknięte. Natomiast przy C18:1‑K cząstki wirusa częściej wydawały się zlane lub sklejone ze sobą, bez oczywistego rozrywania. Wszystkie surfaktanty powodowały pewien stopień agregacji wirusów przy wyższych stężeniach, ale tylko C18:1‑K tworzył rozległe skupiska „zrośniętych błon”, które prawdopodobnie nie pozostają zakaźne. Składnik, który najlepiej inaktywował wirusa — C18:1‑K — miał też najniższe krytyczne stężenie micelarne, co świadczy o tym, że jego ogony lipidowe łatwo się ze sobą układają i po przekroczeniu pewnego progu mogą silnie zaburzyć otoczkę wirusa.
Co to znaczy dla codziennej ochrony
Dla osób niebędących specjalistami, kluczowy wniosek jest prosty: mydło do rąk naprawdę chemicznie uszkadza SARS‑CoV‑2, a niektóre składniki pochodzenia naturalnego są w tym wyjątkowo skuteczne. Mydła bogate w sole kwasów tłuszczowych o długich łańcuchach, takie jak stearynian potasu (potocznie opisany tu jako potas oleinianowy), mogą atakować oleistą osłonę wirusa poprzez silne interakcje hydrofobowe i sprzyjać łączeniu się cząstek wirusa, czyniąc je nieszkodliwymi. Chociaż wszystkie przetestowane surfaktanty mogą przyczyniać się do inaktywacji, te zaprojektowane lub wybrane pod kątem silnego działania lipofilowego mogą oferować lepszą ochronę. Te wnioski mogą pomóc chemikom w projektowaniu bardziej skutecznych, przyjaznych dla skóry mydeł i środków dezynfekujących nie tylko przeciw SARS‑CoV‑2, ale także przeciw innym wirusom otoczkowym, które polegają na tej samej kruchej lipidowej warstwie.
Cytowanie: Yamamoto, A., Iseki, Y., Elsayed, A.M.A. et al. Differential mechanisms of SARS-CoV-2 inactivation by anionic surfactants: a comparative study of fatty acid salts and synthetic surfactants. Sci Rep 16, 6394 (2026). https://doi.org/10.1038/s41598-026-36858-8
Słowa kluczowe: mycie rąk, SARS-CoV-2, środki powierzchniowo czynne w mydłach, otoczka wirusa, dezynfekcja