Clear Sky Science · pl
Farmakokinetyka, patologia i skuteczność inhibitora głównej proteazy SARS-CoV-2 VPC285785 w mysim modelu zakażenia koronawirusem
Dlaczego wciąż potrzebujemy lepszych pigułek na COVID
Pierwsze antywirusowe pigułki przeciw COVID-19, takie jak Paxlovid, były przełomem w przebiegu pandemii. Nie są jednak doskonałe: trzeba je przyjmować bardzo wcześnie, składają się z kilku tabletek dziennie i mogą niebezpiecznie wchodzić w interakcje z innymi lekami. W tym badaniu oceniono nowe kandydaty na leki zaprojektowane tak, by blokować koronawirusa na więcej niż jeden sposób, dobrze działać jako pojedyncze dawki doustne i powodować mniej problemów związanych z interakcjami lekowymi, wykorzystując mysim model zakażenia koronawirusem.
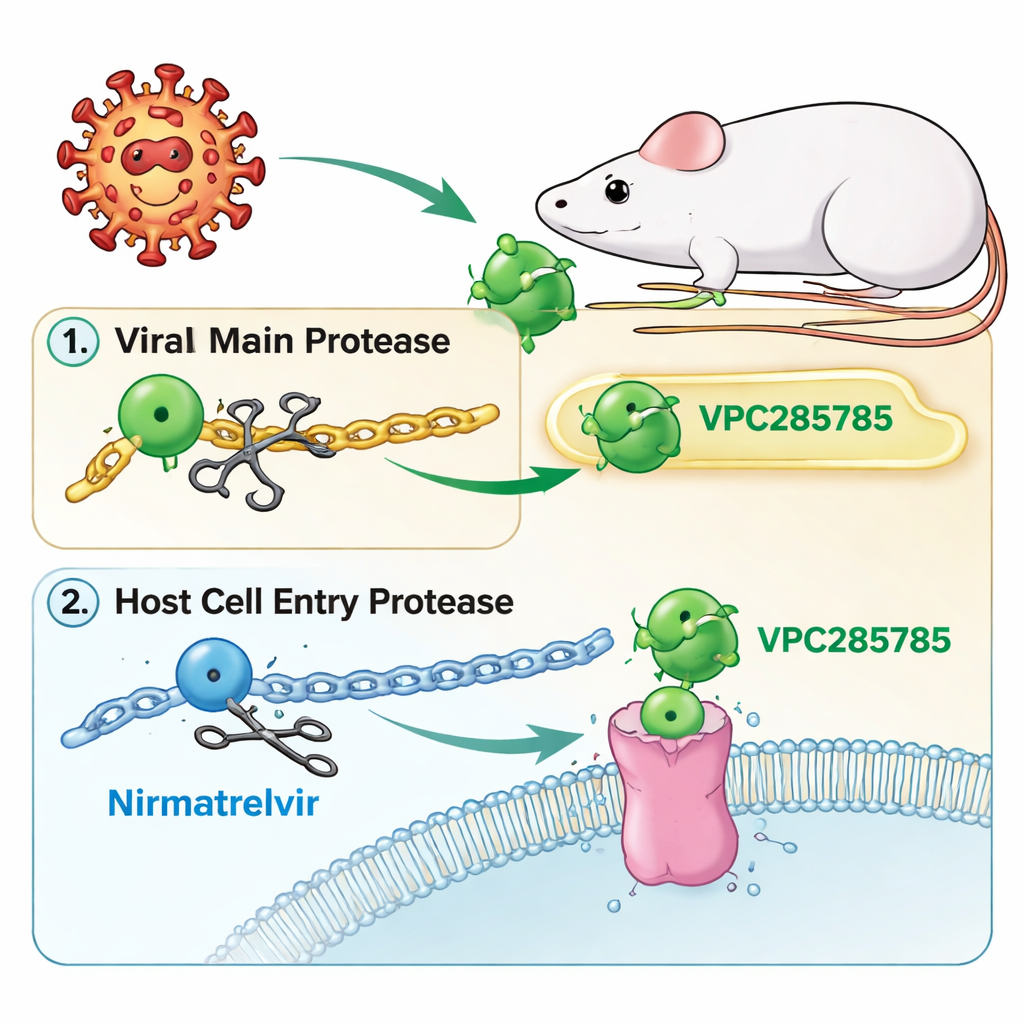
Nowe spojrzenie na cel proteazy SARS-CoV-2
Podobnie jak Paxlovid, nowe związki — nazwane VPC285785 i VPC285786 — celują w „główną proteazę” wirusa, molekularne nożyce, które tną długie białka wirusowe na funkcjonalne części. Jeśli te nożyce zostaną zablokowane, wirus nie jest w stanie się zmontować i zatrzymuje się. Badacze zaprojektowali także te molekuły tak, by oddziaływały na drugie białko w naszych komórkach, kathepsynę L, która pomaga niektórym koronawirusom wniknąć do komórki. Celując zarówno w wirusowe nożyce, jak i w pomocnika wejścia gospodarza, zespół miał nadzieję stworzyć lek o podwójnym mechanizmie działania, trudniejszy do ominięcia przez wirusa i nie wymagający leku wzmacniającego.
Skonstruowane z myślą o dłuższym działaniu, bez wzmacniacza
Paxlovid łączy nirmatrelwir z innym lekiem, rytonawirem, którego zadaniem nie jest walka z wirusem, lecz spowolnienie rozkładu nirmatrelwiru w wątrobie. Rytanowir jednak zakłóca działanie wielu enzymów metabolizujących powszechne leki, prowadząc do złożonych i czasem niebezpiecznych interakcji. VPC285785 i VPC285786 zostały chemicznie zmodyfikowane, by same opierały się rozkładowi — wykorzystano m.in. atomy fluoru i „usztywnienie” pierścieni, co czyni je mniej podatnymi na enzymy wątrobowe. W testach in vitro z preparatami wątroby ludzkiej i mysiej oba nowe związki wykazały stabilność nie mniejszą niż nirmatrelwir, a VPC285786 w pewnych aspektach była nawet bardziej odporna, i to bez udziału rytanowiru.
Jak leki zachowują się i przemieszczają u myszy
Zespół zbadał następnie farmakokinetykę związków w organizmach myszy, mierząc, jak szybko znikają z krwi i jak dobrze wchłaniają się doustnie. Po podaniu dożylnym VPC285785 i VPC285786 utrzymywały się we krwi mniej więcej tak długo jak nirmatrelwir i dawały większą ekspozycję ogólnoustrojową. Przy podaniu doustnym jednak ich losy się rozdzieliły: VPC285785 osiągnęła umiarkowane, ale użyteczne wchłanianie (około 15% połkniętej dawki docierało do krążenia), podczas gdy VPC285786 praktycznie nie trafiała do krwi (około 3%). Ponieważ doustne leki muszą przejść przez ścianę jelita, tylko VPC285785 została wybrana do dalszych eksperymentów zakażeniowych.
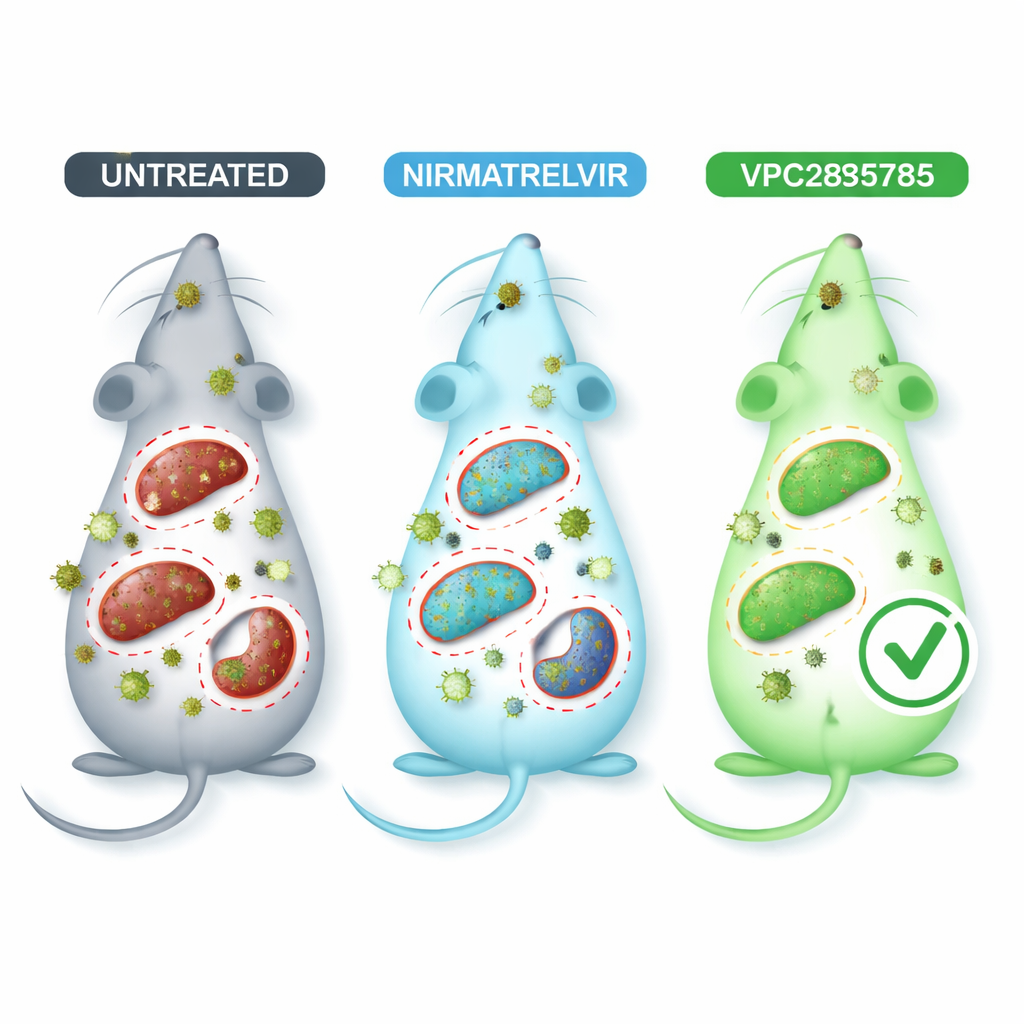
Próba nowej pigułki na zakażonych mysach
Aby naśladować chorobę wywoływaną przez koronawirusa w bezpieczniejszych warunkach, badacze użyli mysiego koronawirusa MHV-A59, który atakuje wiele narządów i powoduje uszkodzenia płuc i wątroby podobne w wielu aspektach do zakażenia ludzkiego. Zakażone myszy leczono doustnie VPC285785, porównawczo nirmatrelwirem lub nieaktywnym nośnikiem. Badania krwi wykazały, że zakażenie obciążało wątrobę i nerki, ale zwierzęta otrzymujące VPC285785 lub nirmatrelwir miały na ogół zdrowsze markery enzymów wątrobowych i nerkowych niż myszy nieleczone. Co najbardziej uderza, VPC285785 ostro obniżyła ilość materiału genetycznego wirusa w wątrobie, mózgu i śledzionie, podczas gdy nirmatrelwir wywołał wyraźny spadek jedynie w mózgu. W płucach, sercu i nerkach żadne z leczeń nie przyniosło mocnego efektu w warunkach zastosowanych testów.
Co to może znaczyć dla przyszłych terapii COVID
Chociaż VPC285785 jest w próbkach in vitro mniej silna przeciw wirusowej proteazie niż nirmatrelwir, dobrze działa in vivo, znacząco zmniejszając poziom wirusa w kilku kluczowych narządach przy jednoczesnym zachowaniu funkcji tych narządów, i to bez wzmacniacza rytanowiru. Siostrzany związek, VPC285786, pokazuje, że możliwe jest jeszcze silniejsze podwójne ukierunkowanie na proteazę wirusową i kathepsynę L, ale jego słabe wchłanianie wymaga poprawy. Razem wyniki sugerują, że leki nowej generacji przeciw COVID mogłyby być zaprojektowane jako pojedyncze, doustne preparaty celujące zarówno w cele wirusowe, jak i komórkowe gospodarza, powodujące mniej niebezpiecznych interakcji z innymi lekami i nadal zapewniające silną ochronę w istotnych tkankach.
Cytowanie: Smith, J.R., Toro, A., Sabater, A. et al. Pharmacokinetics, pathology and efficacy of SARS-CoV-2 main protease inhibitor VPC285785 in a murine model of coronavirus infection. Sci Rep 16, 6905 (2026). https://doi.org/10.1038/s41598-026-36842-2
Słowa kluczowe: antywirusowe SARS-CoV-2, <keyword>alternatywy dla Paxlovid, mysi model koronawirusa, doustne leczenie COVID