Clear Sky Science · pl
YTHDC1 modyfikuje złośliwy fenotyp siatkówczaka poprzez autofagię zależną od SQSTM1
Dlaczego to ma znaczenie przy dziecięcym raku oka
Siatkówczak jest najczęstszym nowotworem oka u małych dzieci. Lekarze często mogą go wyleczyć, jeśli zostanie wykryty wcześnie, ale gdy guz zaczyna naciekać tkanki wokół oka lub rozprzestrzeniać się w kierunku mózgu, uratowanie zarówno życia, jak i wzroku dziecka staje się znacznie trudniejsze. W tym badaniu analizowano molekularny „hamulec” wewnątrz komórek nowotworowych — dwie cząsteczki o nazwach YTHDC1 i SQSTM1 — które wydają się pomagać utrzymać siatkówczaka w mniej agresywnej formie. Zrozumienie, jak działa ten hamulec, może otworzyć nowe ścieżki dla łagodniejszych, bardziej ukierunkowanych terapii.
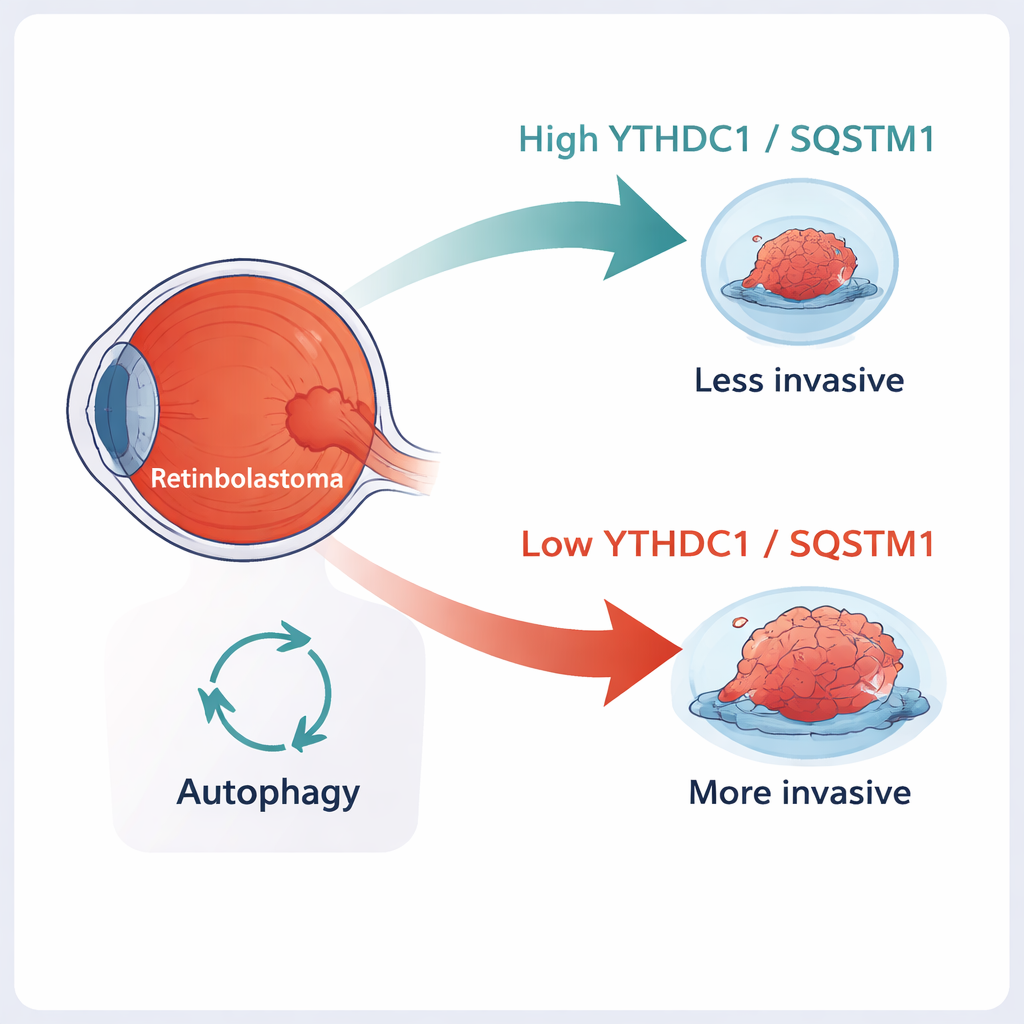
Bliższe spojrzenie na dziecięce guzy oka
Siatkówczak powstaje z warstwy siatkówki odpowiedzialnej za odbiór światła, zwykle u dzieci poniżej piątego roku życia. Klasycznie choroba rozpoczyna się, gdy obie kopie genu strażnika, RB1, zostają utracone. Jednak samo utracenie RB1 nie wyjaśnia w pełni, dlaczego niektóre guzy pozostają ograniczone do oka, podczas gdy inne naciekają pobliskie tkanki lub rozprzestrzeniają się wzdłuż nerwu wzrokowego. Coraz więcej badań pokazuje, że chemiczne znaczniki umieszczone na RNA — tymczasowych informacjach mówiących komórkom, jakie białka mają wytwarzać — mogą silnie wpływać na zachowanie nowotworów. Jednym z najczęstszych takich znaczników jest m6A, który może zmieniać stabilność tych wiadomości i ich trwałość w komórce.
Odkrycie brakującego molekularnego hamulca
Autorzy zaczęli od porównania aktywności genetycznej w guzach, które pozostały wewnątrz oka, z tymi, które już stały się inwazyjne. Korzystając z publicznego zestawu danych z sekwencjonowania RNA pobranych z próbek siatkówczaka, zidentyfikowali tysiące genów o różnej aktywności między obiema grupami, a następnie skupili się na kluczowych „regulatorach” m6A. Należą do nich enzymy dodające lub usuwające m6A oraz białka „czytające” ten znacznik. Spośród dziesięciu głównych regulatorów stwierdzili, że jeden czytnik, YTHDC1, był konsekwentnie niższy w guzach inwazyjnych. Analizując próbki od 50 dzieci oraz wykonując testy laboratoryjne na tkance nowotworowej, potwierdzili, że poziomy YTHDC1 — zarówno jego RNA, jak i białko — były obniżone w bardziej agresywnych nowotworach.
Testowanie roli YTHDC1
Aby sprawdzić, co YTHDC1 faktycznie robi, zespół manipulował jego poziomami w dwóch ludzkich liniach komórkowych siatkówczaka. Gdy obniżono poziom YTHDC1 za pomocą narzędzi genetycznych, komórki szybciej się namnażały i były lepiej zdolne do przemieszczania się przez sztuczne membrany imitujące bariery tkankowe — oznaki bardziej inwazyjnego guza. U myszy komórki pozbawione YTHDC1 tworzyły większe, cięższe guzy. Odwrotny efekt również występował: wymuszenie nadprodukcji YTHDC1 spowalniało ich wzrost oraz zmniejszało zdolność do migracji i inwazji. Te eksperymenty sugerują, że YTHDC1 działa jak supresor guza, pomagając powstrzymać najniebezpieczniejsze zachowania siatkówczaka.
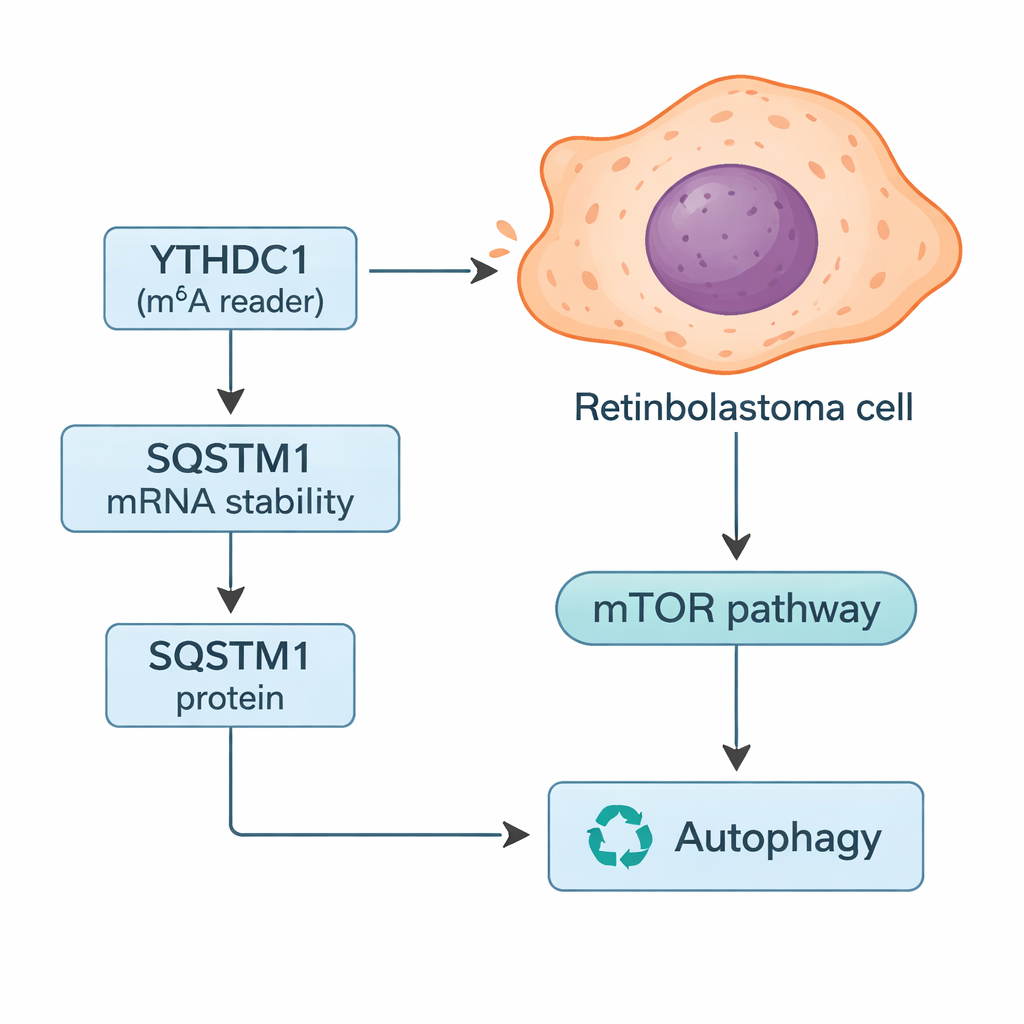
Jak YTHDC1 kontroluje system recyklingu komórkowego
Zagłębiając się dalej, badacze poszukiwali konkretnych genów, których wiadomości mogłyby być kontrolowane przez YTHDC1. Łącząc przeszukiwania baz danych z własnymi danymi guzów, skupili się na SQSTM1, białku szerzej znanym jako p62. SQSTM1 pomaga zarządzać autofagią — systemem recyklingu komórki, który rozkłada uszkodzone elementy i może dostarczać paliwa, gdy zasoby są ograniczone. Badanie wykazało, że YTHDC1 fizycznie wiąże się z RNA SQSTM1 i stabilizuje je, umożliwiając powstawanie większej ilości białka SQSTM1. Gdy YTHDC1 był zmniejszony, poziomy SQSTM1 spadały, a jego RNA ulegało szybszemu rozpadowi. Wyciszenie samego SQSTM1 powodowało, że komórki siatkówczaka bardziej rosły i inwadowały, a także częściowo niwelowało ochronne efekty obserwowane przy nadprodukcji YTHDC1, umieszczając SQSTM1 jako kluczowego pośrednika w tej ścieżce.
Autofagia, energia i złośliwość guza
Ponieważ SQSTM1 odgrywa centralną rolę w autofagii, zespół sprawdził, jak zmiana YTHDC1 i SQSTM1 wpływa na ten proces recyklingu. Wykorzystując kombinację znaczników fluorescencyjnych i pomiarów białek, stwierdzili, że obniżenie YTHDC1 lub SQSTM1 zwiększa „strumień” autofagiczny — więcej materiału komórkowego było kierowane do i przez system recyklingu. Zaobserwowali też zmiany w szlaku mTOR, głównym przełączniku reagującym na poziom składników odżywczych, który normalnie hamuje autofagię. Przy niższym poziomie SQSTM1 aktywność mTOR malała, co jest zgodne z nasileniem autofagii. Autorzy proponują, że w inwazyjnym siatkówczaku obniżenie YTHDC1 prowadzi do słabszych sygnałów SQSTM1, osłabienia aktywności mTOR i zwiększonej autofagii, co pomaga komórkom nowotworowym przetrwać stres i rozprzestrzeniać się.
Co to oznacza dla przyszłych terapii
Dla czytelnika niebędącego specjalistą główny wniosek jest taki, że to badanie identyfikuje łańcuch zdarzeń wewnątrz komórek siatkówczaka — YTHDC1 kontrolujący SQSTM1, który z kolei kształtuje mechanizmy recyklingu komórkowego — co wpływa na agresywność nowotworu. Gdy ten łańcuch zostaje osłabiony, guzy rosną szybciej i bardziej naciekają. Choć przed wprowadzeniem tych odkryć do praktyki klinicznej pozostaje wiele pracy, ta ścieżka daje nowe pomysły terapeutyczne: przywrócenie funkcji YTHDC1, stabilizacja SQSTM1 lub precyzyjne regulowanie autofagii i aktywności mTOR mogłyby w przyszłości uzupełniać istniejące chemioterapie. Dla dzieci z tym rakiem oka takie celowane strategie mogłyby ograniczyć rozprzestrzenianie się guza, przy jednoczesnym zachowaniu większej ilości wzroku i zmniejszeniu skutków ubocznych leczenia.
Cytowanie: Ding, J., Sun, J., Wang, J. et al. YTHDC1 modulates the malignant phenotype of retinoblastoma via SQSTM1-mediated autophagy. Sci Rep 16, 6292 (2026). https://doi.org/10.1038/s41598-026-36833-3
Słowa kluczowe: siatkówczak, YTHDC1, SQSTM1, autofagia, szlak mTOR