Clear Sky Science · pl
Iryzyna reguluje metabolizm lipidów i ferroptozę w komórkach raka jajnika przez modulację osi ALOX5-5-HETE-PD-L1
Dlaczego ten związek roślinny ma znaczenie dla raka jajnika
Rak jajnika jest jednym z najbardziej zabójczych nowotworów u kobiet, ponieważ zwykle wykrywany jest późno i często nawraca po leczeniu. W niniejszym badaniu sprawdzono, czy naturalny związek tectorigenin, występujący w roślinie Belamcanda chinensis, może spowolnić rozwój raka jajnika poprzez pozbawienie komórek guza określonych tłuszczów i wymuszenie wyjątkowego rodzaju śmierci komórkowej zależnej od żelaza. Badanie analizuje także, czy ten związek może osłabić „pelerynę niewidzialności”, której guzy używają, by ukryć się przed układem odpornościowym.
Ukryte źródło paliwa w komórkach guza
Podobnie jak wiele nowotworów, guzy jajnika przeprogramowują sposób gospodarowania tłuszczami. Zamiast używać tłuszczów jedynie jako źródła energii, komórki nowotworowe gromadzą je jako materiał do budowy błon oraz jako bufor przeciw uszkodzeniom. W hodowlach komórek raka jajnika dodatkowe jednonienasycone kwasy tłuszczowe powodowały nagromadzenie wolnych kwasów tłuszczowych, trójglicerydów i cholesterolu — kluczowych form magazynowanego tłuszczu. Ten nadmiar tłuszczu sprzyjał wzrostowi i inwazyjności komórek oraz pomagał im przeciwstawiać się destrukcyjnemu procesowi zwanemu ferroptozą, w którym żelazo i uszkodzone tłuszcze łączą się, prowadząc do pękania błon komórkowych. Innymi słowy, zaburzony metabolizm lipidów dawał nowotworowi przewagę wzrostową i tarczę ochronną.
Wymuszanie autodestrukcji komórek nowotworowych
Naukowcy przetestowali następnie tectorigenin na normalnych komórkach jajnika oraz na kilku liniach komórkowych raka jajnika. Przy dawkach do 200 mikrogramów na litr związek nie szkodził komórkom normalnym, ale wyraźnie hamował wzrost komórek nowotworowych, zmniejszał ich zdolność do inwazji przez błonę i zwiększał odsetek zaprogramowanej śmierci komórek. Gdy komórki nowotworowe były uprzednio traktowane lekiem blokującym ferroptozę, stawały się bardziej agresywne. Dodanie tectorigeninu odwracało te efekty: zapasy tłuszczu malały, rosły markery związane z żelazem i utlenianiem, a więcej komórek umierało. W modelach mysich z wszczepionymi ludzkimi guzami jajnika wstrzyknięcia tectorigeninu zmniejszały rozmiar guzów, obniżały zawartość tłuszczu w tkankach nowotworowych i zwiększały chemiczne oznaki ferroptozy, co ponownie sugeruje, że związek popycha komórki nowotworowe ku tej zależnej od żelaza ścieżce śmierci.
Kluczowy przełącznik molekularny łączący tłuszcze i ucieczkę przed układem odpornościowym
Aby ustalić, jak tectorigenin działa na poziomie molekularnym, zespół połączył analizę dużych zbiorów danych z modelowaniem komputerowym interakcji lek–białko. Skoncentrowali się na enzymie ALOX5, który przekształca powszechny kwas tłuszczowy w cząsteczkę sygnałową nazwaną 5‑HETE. W komórkach raka jajnika i próbkach guzów poziomy ALOX5 były znacznie wyższe niż w tkance prawidłowej. Dokowanie komputerowe i symulacje dynamiki molekularnej wykazały, że tectorigenin może stabilnie wiązać się z ALOX5, działając jak wewnętrzny hamulec. Gdy badacze sztucznie zwiększyli ekspresję ALOX5 w komórkach nowotworowych, zapasy tłuszczu rosły, markery ferroptozy malały, a komórki stawały się bardziej inwazyjne. Leczenie tectorigeninem cofało te zmiany. Upośledzenie ALOX5 przynosiło odwrotny skutek — mniej tłuszczu, więcej ferroptozy i słabszy wzrost — co jednoznacznie wskazuje ten enzym jako centralny element działania związku.
Jak guzy tracą swoją tarczę przed układem odpornościowym
Badanie powiązało także tę ścieżkę lipidową z ważną cząsteczką punktu kontrolnego odporności o nazwie PD‑L1, którą guzy wykorzystują do wyłączania atakujących komórek odpornościowych. Produkt ALOX5, 5‑HETE, podnosił poziomy PD‑L1, wzmacniając tę osłonę. Gdy ALOX5 był wyciszony, zarówno 5‑HETE, jak i PD‑L1 malały; przy ponownym wprowadzeniu 5‑HETE PD‑L1 wzrastał i komórki nowotworowe odzyskiwały część ochrony przed ferroptozą. Tectorigenin zmniejszał poziomy ALOX5, obniżał 5‑HETE, a w konsekwencji redukował PD‑L1 w hodowlach komórkowych i w guzach mysich. Sugeruje to, że celując w jeden enzym metaboliczny, związek może jednocześnie zaburzyć lipidowe mechanizmy obronne nowotworu i osłabić jego zdolność do ukrywania się przed atakiem immunologicznym.
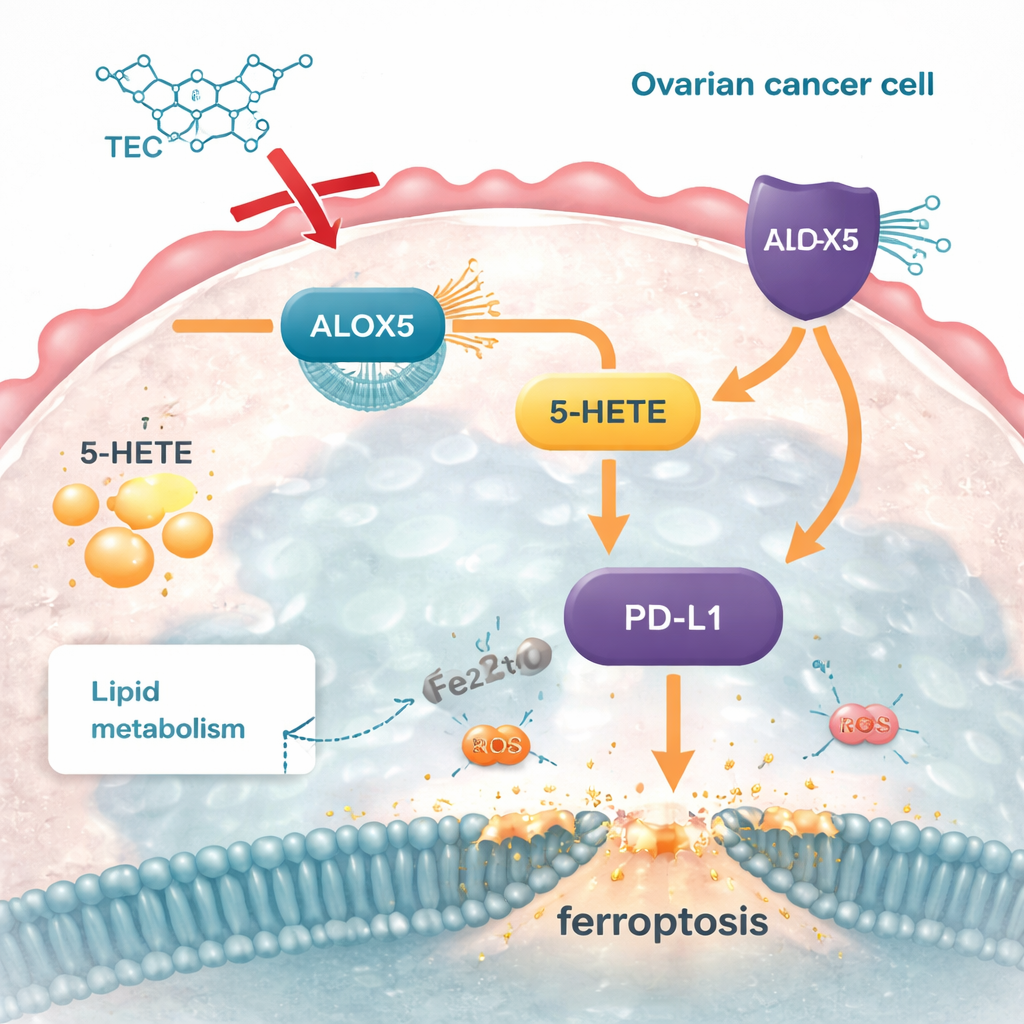
Co to może oznaczać dla przyszłych terapii
Krótko mówiąc, praca ta pokazuje, że tectorigenin działa jak precyzyjny klucz wrzucony w mechanikę gospodarowania tłuszczami w komórce nowotworowej. Blokując ALOX5, ogranicza produkcję 5‑HETE, redukuje nadmiar zapasów tłuszczu, uczula komórki na uszkodzenia zależne od żelaza i pozbawia je części maskowania immunologicznego. Choć wyniki pochodzą z badań in vitro i na modelach mysich — i wiele pozostaje do sprawdzenia u ludzi — wskazują na obiecującą strategię: celowanie w oś ALOX5–5‑HETE–PD‑L1, aby jednocześnie „zagłodzić” guzy jajnika na ich lipidowych zasobach i uczynić je bardziej podatnymi na eliminację przez własny układ odpornościowy lub przyszłe immunoterapie.
Cytowanie: Cai, H., Huang, C. & Zhang, Z. Irisin regulates lipid metabolism and ferroptosis in ovarian cancer cells by modulating the ALOX5-5-HETE-PD-L1 axis. Sci Rep 16, 7223 (2026). https://doi.org/10.1038/s41598-026-36816-4
Słowa kluczowe: rak jajnika, metabolizm lipidów, ferroptoza, ALOX5, terapia związkami naturalnymi