Clear Sky Science · pl
Eksperymentalna charakterystyka dostarczania terapii protonowej z minipromieniami w warunkach dawek FLASH
Szybsze, łagodniejsze wiązki promieniowania
Radioterapia jest jednym z podstawowych sposobów leczenia nowotworów, lecz może uszkadzać także zdrowe tkanki obok guza. W tym badaniu zbadano nowy sposób podawania promieniowania protonowego, którego celem jest mocne uderzenie w guz przy jednoczesnym zmniejszeniu szkód dla narządów zdrowych. Łącząc dwie nowatorskie koncepcje — bardzo gęsto rozmieszczone „minipromienie” oraz ultra‑szybkie dawki w trybie FLASH — autorzy pokazują, że technicznie możliwe jest przeprowadzenie bardzo precyzyjnego zabiegu w ciągu zaledwie kilku sekund przy użyciu sprzętu podobnego do tego, który jest już dostępny we współczesnych szpitalach.
Dlaczego przekształcać promieniowanie w maleńkie wiązki?
Tradycyjne pola promieniowania wyglądają gładko: dawka jest rozłożona stosunkowo równomiernie na leczonej powierzchni. Przestrzenne frakcjonowanie promieniowania łamie to założenie celowo. W terapii protonowej z minipromieniami promieniowanie jest podzielone na wiele cienkich, submilimetrowych wiązek rozdzielonych przerwami. Blisko powierzchni tworzy to wzór wysokodawkowych „grzbietów” i niskodawkowych „dolin”. Zdrowa tkanka między grzbietami ma większe szanse na regenerację, podczas gdy głębiej w ciele wiązki rozpraszają się i zachodzą na siebie, dostarczając guzowi bardziej jednorodną i skuteczną dawkę. Wczesne badania laboratoryjne i na zwierzętach sugerują, że taki wzór może zmniejszać skutki uboczne, a nawet wywoływać korzystne odpowiedzi immunologiczne przeciwko nowotworowi.
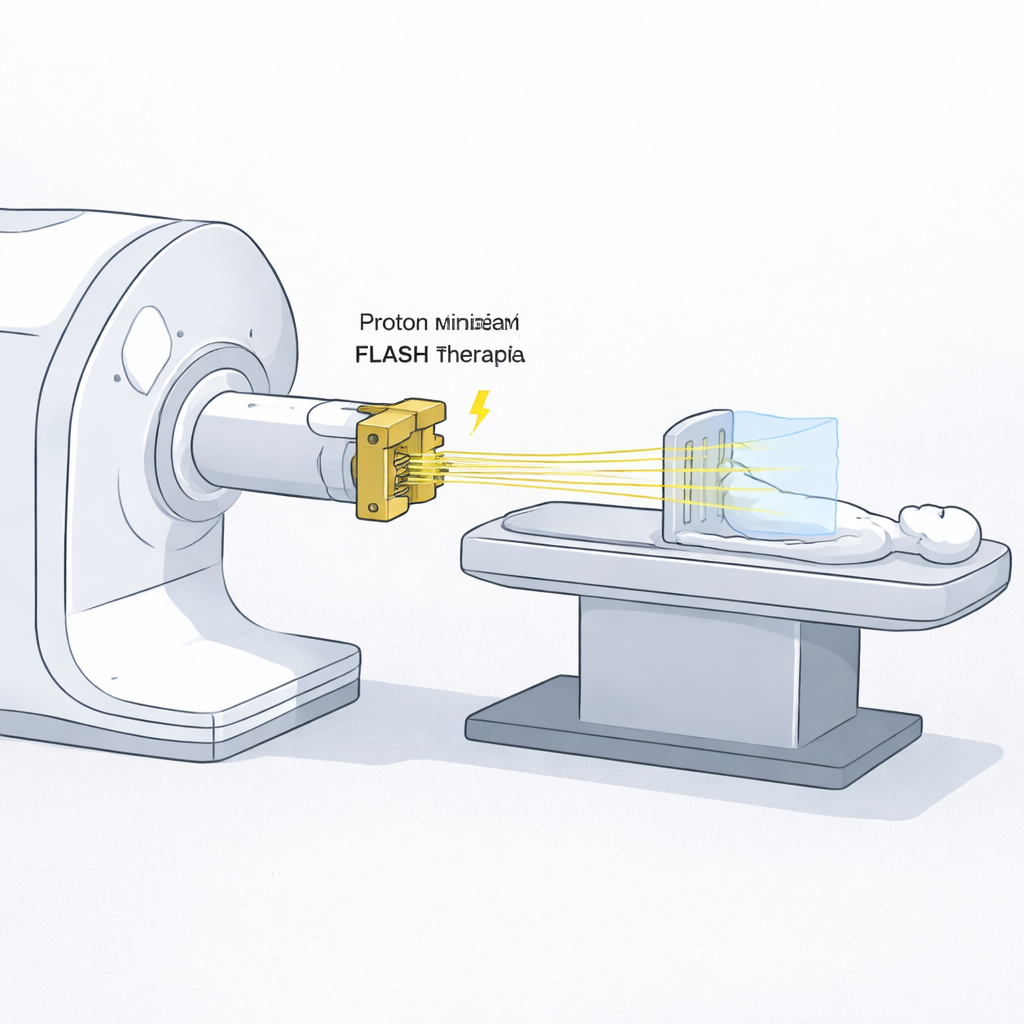
Czym jest FLASH i dlaczego ma znaczenie prędkość podania?
Terapia FLASH to nowe spojrzenie na wymiar czasu w dostarczaniu promieniowania. Zamiast powolnego podawania dawki przez kilkadziesiąt sekund lub minut, FLASH dostarcza tę samą dawkę w ułamku sekundy przy ultrawysokich szybkościach dawki — dziesiątkach do setek grayów na sekundę. Ku zaskoczeniu, wiele eksperymentów wykazało, że tkanki normalne mogą być lepiej chronione w tych ekstremalnych warunkach, podczas gdy guzy pozostają równie wrażliwe. W przypadku minipromieni protonowych istniała jednak praktyczna przeszkoda: metalowe bloki z wieloma szczelinami używane do formowania wiązki marnują znaczną część cząstek, przez co zabiegi mogą trwać kilka minut. Gdyby minipromienie można było podać w trybie FLASH, utracony czas mógłby zostać odzyskany, a korzyści biologiczne obu metod — połączone.
Wdrożenie minipromieni i FLASH na maszynie klinicznej
Zespół pracował z kompaktowym klinicznym systemem protonowym, który zwykle leczy pacjentów gładką, skanującą wiązką protonów. Do końcówki dyszy terapeutycznej zamontowali niestandardowe mosiężne kolimatory wieloszczelinowe — każdy zawierał pięć wąskich szczelin o szerokości zaledwie 1 milimetra, rozstawionych co 2,8 milimetra. Zwiększając prąd wiązki i starannie dostrajając optykę wiązki, pracowali w trybie ultrawysokiej szybkości dawki przy energii 228 MeV, zachowując jednocześnie możliwość przełączenia z powrotem na zwykłe ustawienia kliniczne. Następnie zmierzyli rozkład dawki w blokach z tworzywa imitujących wodę za pomocą specjalnych filmów radio‑czułych i porównali te pomiary ze szczegółowymi symulacjami komputerowymi śledzącymi indywidualne interakcje protonów.
Jak sprawdziła się nowa wiązka?
W warunkach FLASH wiązka protonowa zachowała wyraźny wzór minipromieni: ostre grzbiety wzdłuż torów szczelin i głębokie doliny pomiędzy nimi. Pomiary i symulacje ściśle zgadzały się co do tego, jak ten wzór zmieniał się wraz z głębokością oraz jak szybko się rozmazywał w wyniku rozpraszania wiązki. Grubszy kolimator o długości 10 cm zapewniał czystsze rozdzielenie między grzbietami a dolinami niż wersja 6,5 cm, szczególnie blisko powierzchni, co oznaczało lepszą ochronę regionów „doliny”. Co kluczowe, praca urządzenia w trybie FLASH skróciła czas dostarczenia typowego pola minipromieni 3 na 3 cm z około 3 minut do zaledwie 2,5 sekundy. Obliczenia oparte na logach czasowych maszyny wykazały, że lokalne szybkości dawki w obszarach grzbietów łatwo przekraczały powszechnie stosowane progi FLASH, przy jednoczesnym zachowaniu drobnej struktury przestrzennej minipromieni.
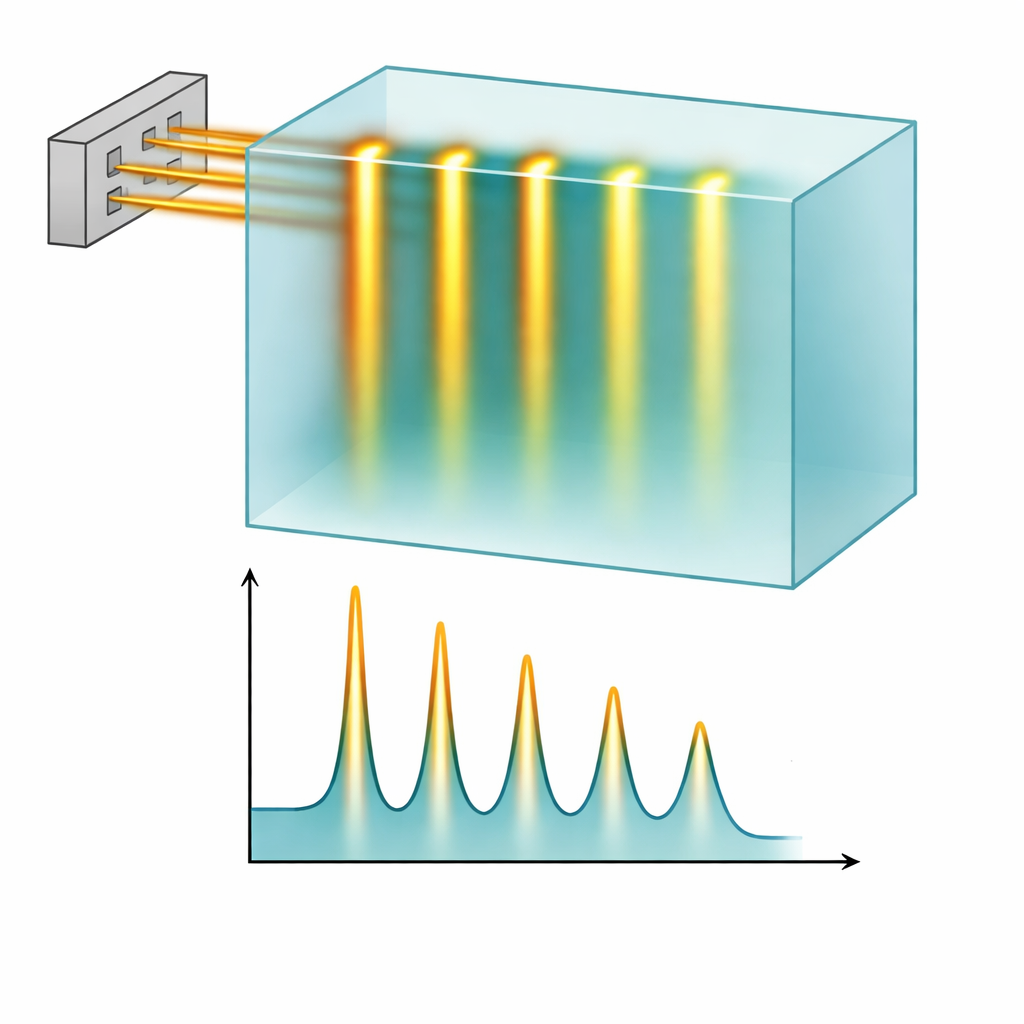
Co to może znaczyć dla przyszłej opieki onkologicznej
To badanie jest wczesnym, ale ważnym dowodem na zasadę. Pokazuje, że standardowy kliniczny system terapii protonowej może zostać zaadaptowany do dostarczania minipromieni protonowych przy szybkościach dawki FLASH bez poświęcania precyzji czy jakości wiązki. Pacjenci nie są jeszcze leczeni tą metodą: eksperymenty przeprowadzono w warunkach testowych i użyto tylko pojedynczej wiązki wysokiej energii, zamiast warstwowych schematów energetycznych potrzebnych do leczenia rzeczywistych guzów. Efekty biologiczne łączenia przestrzennych wzorów minipromieni z ultraszybkim dostarczaniem FLASH także muszą zostać potwierdzone na zwierzętach, a ostatecznie u ludzi. Mimo to badanie tworzy techniczne podstawy dla przyszłych terapii, które mogłyby kontrolować guzy równie skutecznie jak najlepsze dzisiejsze metody, jednocześnie dramatycznie zmniejszając uszkodzenia zdrowych narządów poprzez wykorzystanie zarówno miejsca, jak i szybkości podania promieniowania.
Cytowanie: Lin, Y., Wu, W., Setianegara, J. et al. Experimental characterization of proton minibeam therapy delivery under FLASH dose-rate conditions. Sci Rep 16, 7803 (2026). https://doi.org/10.1038/s41598-026-36739-0
Słowa kluczowe: terapia protonowa, radioterapia FLASH, promieniowanie minipromieniowe, leczenie raka, szybkość dawki promieniowania