Clear Sky Science · pl
Ukryty w profagach system obronny typu RexAB u Pseudomonas putida
Ukryci ochroniarze mieszkający wewnątrz bakterii
Bakterie są nieustannie ścigane przez wirusy zwane fagami, które potrafią zniweczyć całe populacje mikroorganizmów. W tym badaniu przyglądamy się, w jaki sposób „uśpione” wirusy już ukryte w DNA bakterii mogą potajemnie działać jako ochroniarze, poświęcając zakażone komórki, by ocalić resztę. Zrozumienie tych naturalnych forteli obronnych ma znaczenie dla terapii fagowej, biotechnologii, a także dla utrzymania stabilności mikroorganizmów stosowanych w przemyśle.
Wirusy, które zmieniają się z wrogów w sojuszników
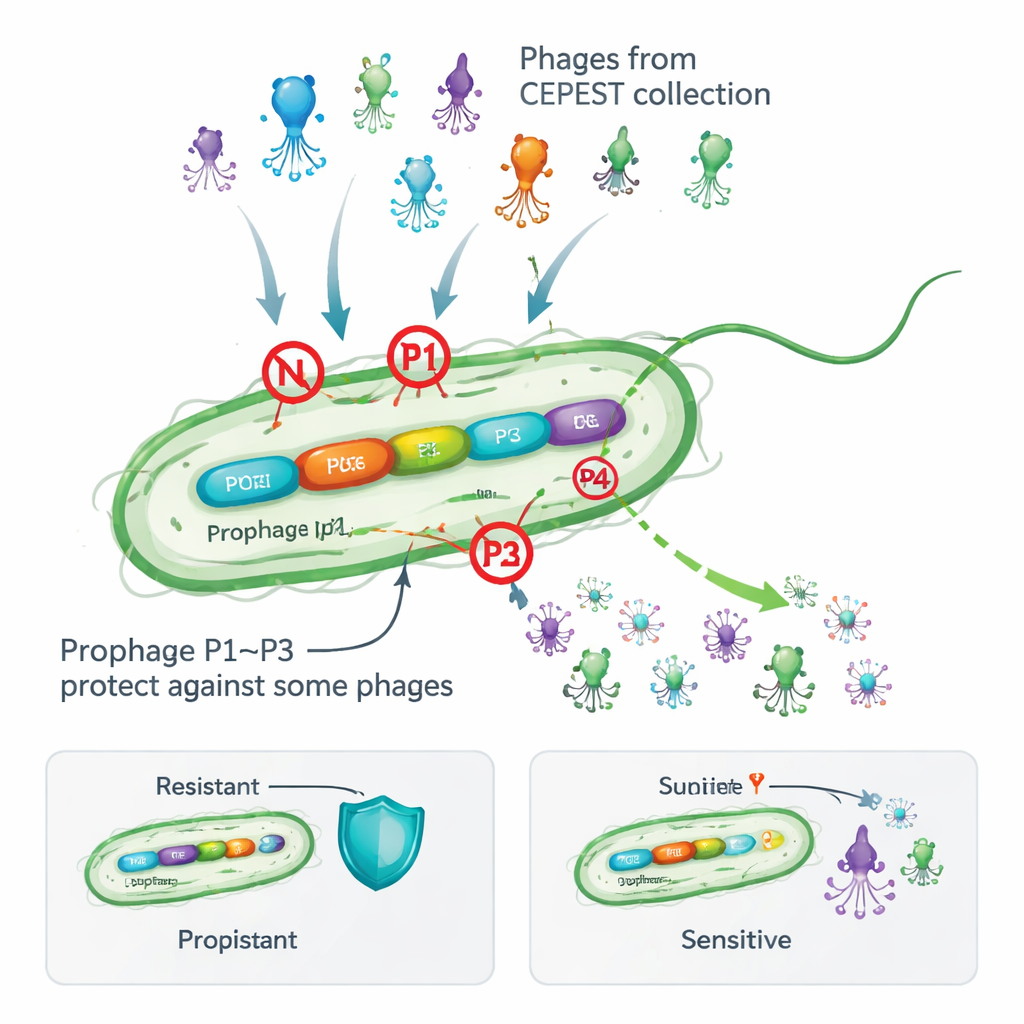
Wiele bakterii nosi przy sobie temperowane fagii w postaci uśpionej zwanej profagiem, włączonej w ich chromosomy. Na pierwszy rzut oka wydaje się to ryzykowne: ci wirusowi pasażerowie mogą się obudzić i uszkodzić komórkę-gospodarza, a także zwiększać rozmiar genomu. Jednak przeglądy tysięcy genomów bakteryjnych pokazują, że większość gatunków zachowuje takie profagi, co sugeruje, że dają one korzyści. Wcześniejsze prace na glebowej bakterii Pseudomonas putida wykazały, że usunięcie jej czterech krypticznych (nieproduktywnych) profagów uczyniło komórki bardziej podatnymi na atak przez eksperymentalny zestaw fagów nazwany CEPEST. To zasugerowało, że profagi przenoszą broń przeciwfagową, ale konkretne geny i mechanizmy pozostawały nieznane.
Trzy rezydentne wirusy dają ukierunkowaną ochronę
Autorzy rozłożyli na czynniki wkład poszczególnych profagów, usuwając je kolejno i testując, jak dobrze 26 różnych fagów z kolekcji CEPEST potrafi tworzyć płytki na monolitach bakteryjnych. Stwierdzili, że profagi nazwane P1, P2 i P3 każda zapewnia ochronę, ale tylko wobec konkretnych grup fagów, podczas gdy P4 wydaje się neutralny. Sam P1 potrafi zmniejszyć zakażenie niektórymi fagami w przybliżeniu o tysiąckrotną wartość, P2 daje bardziej umiarkowaną ochronę, a P3 jest spektakularnie skuteczny — lecz tylko przeciw pewnym „jumbo” fagom o dużych genomach. W większości przypadków pojedynczy profag tłumaczy obserwowany wzór oporności, choć dla kilku fagów wydaje się, że współdziałają ze sobą odmienne profagi. Wyniki te pokazują, że nawet „ciche” profagi mogą działać jako dostosowana tarcza, skierowana na konkretne zagrożenia wirusowe.
Wyśledzenie dwuczęściowego molekularnego alarmu
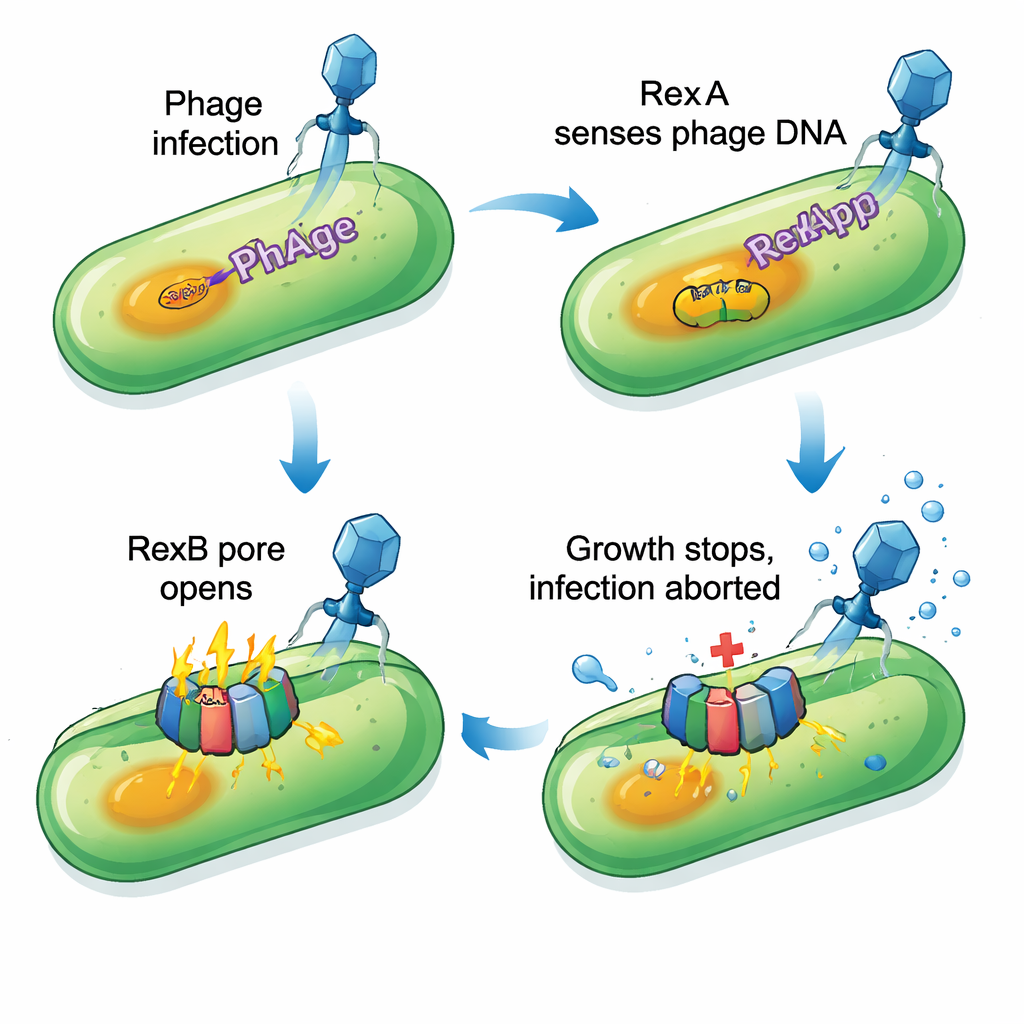
Koncentrując się na silnej i relatywnie szerokiej ochronie zapewnianej przez P1, zespół systematycznie usuwał bloki genów P1, aż obrona zniknęła. Zawężając poszukiwania, odkryli, że utrata zaledwie dwóch sąsiednich genów, PP_5643 i PP_5644, czyniła komórki tak wrażliwymi, jakby cały profag P1 został usunięty. Analizy bioinformatyczne wykazały, że PP_5643 przypomina RexA, białko wiążące DNA znane z klasycznych badań nad fagiem lambda, natomiast PP_5644 wygląda jak białko błonowe z kilkoma helisami, które mogłyby tworzyć porę, podobne do RexB. Razem ta para odpowiada dobrze znanemu typowi systemu „aborcji infekcji”: po wykryciu specyficznego faga zakażona komórka celowo przerywa własny wzrost, tak by wirus nie mógł się namnożyć i rozprzestrzenić na sąsiadów.
Jak obrona sabotażuje zakażone komórki
Eksperymenty potwierdziły, że wersja RexA z P1 (nazwana RexApp) wiąże DNA bez dużego znaczenia dla dokładnej sekwencji, co czyni ją dobrze przystosowaną do wykrywania nietypowych struktur DNA powstających podczas replikacji wirusa. Partner — RexBpp — osadza się w błonie komórkowej. Gdy RexApp jest sztucznie nadprodukowany, komórki, które nadal zawierają gen rexBpp, wykazują silne zahamowanie wzrostu i oznaki uszkodzenia błony: barwniki zwykle nieprzenikające przez nienaruszone błony nagle wnikają do wnętrza, a niewielkie ilości enzymu cytoplazmatycznego wyciekają na zewnątrz. Jeśli rexBpp jest nieobecny lub zmutowany, nadprodukcja RexApp przestaje szkodzić komórkom. Wskazuje to, że RexApp działa jako wyzwalacz, podczas gdy RexBpp jest efektorem uszkadzającym osłonkę komórkową. Co ciekawe, większość zaatakowanych komórek nie pęka całkowicie; zamiast tego wchodzą w głęboko spowolniony, niemal stacjonarny stan, który wydaje się niekompatybilny z namnażaniem fagów.
Dlaczego poświęcenie kilku komórek może uratować populację
Obraz, który się wyłania, to altruistyczna obrona: gdy wrażliwy fag zakaża P. putida, RexApp prawdopodobnie wykrywa kompleksy DNA‑białko wirusa i uruchamia RexBpp, który upośledza błonę i nagle zatrzymuje wzrost. Zakażona komórka płaci cenę, ale cykl życiowy faga zostaje przerwany, a szersza społeczność bakteryjna zostaje chroniona. Systemy typu RexAB zostały dotąd znalezione tylko w kilku różnych profagach, lecz dzielą tę samą podstawową logikę — wewnątrzkomórkowy sensor połączony z błonowym efektorem, który potrafi szybko przekształcić produktywną komórkę w ślepą uliczkę dla wirusa. Dla bakterii utrzymywanie kryptycznych profagów niosących takie moduły obronne może równoważyć koszty związane z posiadaniem wirusowego DNA, pomagając im przetrwać w świecie, w którym fagi są wszędzie.
Cytowanie: Rosendahl, S., Kängsep, A., Ainelo, A. et al. Prophage-encoded RexAB-type phage defense system in Pseudomonas putida. Sci Rep 16, 5898 (2026). https://doi.org/10.1038/s41598-026-36734-5
Słowa kluczowe: obrona przed bakteriofagami, profag, Pseudomonas putida, aborcja infekcji, system RexAB