Clear Sky Science · pl
Opracowanie i walidacja mysiego modelu potrójnie ujemnego raka piersi z ekspresją PSMA do przedklinicznych terapii radiokinetycznych ukierunkowanych
Dlaczego to badanie ma znaczenie
Potrójnie ujemny rak piersi jest jedną z najtrudniejszych postaci raka piersi do leczenia. Ma tendencję do szybkiego rozprzestrzeniania się, oferuje pacjentom mniej ukierunkowanych opcji terapeutycznych i często nawraca po standardowych terapiach. Jednocześnie nowa klasa „inteligentnych” leków radiacyjnych wiążących się z konkretną cząsteczką zwaną PSMA zrewolucjonizowała leczenie zaawansowanego raka prostaty. Niniejsze badanie stawia proste, ale istotne pytanie: czy można zbudować realistyczny model laboratoryjny potrójnie ujemnego raka piersi, który nosi ten sam cel PSMA, aby rzetelnie przetestować, czy te inteligentne leki radiacyjne mogłyby także pomóc pacjentom z tą agresywną postacią raka piersi?
Od celu w raku prostaty do wyzwania w raku piersi
PSMA, czyli swoisty antygen błonowy prostaty, to niewielka struktura obecna na powierzchni niektórych komórek. Występuje obficie w wielu rakach prostaty i może być wykrywana przez radioaktywne leki, które jednocześnie uwidaczniają guzy w badaniach obrazowych i dostarczają do nich promieniowanie. Ostatnio badacze odkryli, że PSMA pojawia się także, w różnym stopniu, w naczyniach krwionośnych i komórkach kilku innych nowotworów, w tym potrójnie ujemnego raka piersi. Jednak w tych nowotworach niezwiązanych z prostatą ekspresja PSMA bywa fragmentaryczna i słabsza, co utrudnia ocenę, czy terapie ukierunkowane na PSMA zadziałają. Zanim spróbuje się nowych terapii u pacjentów, naukowcy potrzebują modeli zwierzęcych, które wiernie odtwarzają wzór ekspresji PSMA w guzach piersi — co okazało się zaskakująco trudne do osiągnięcia.
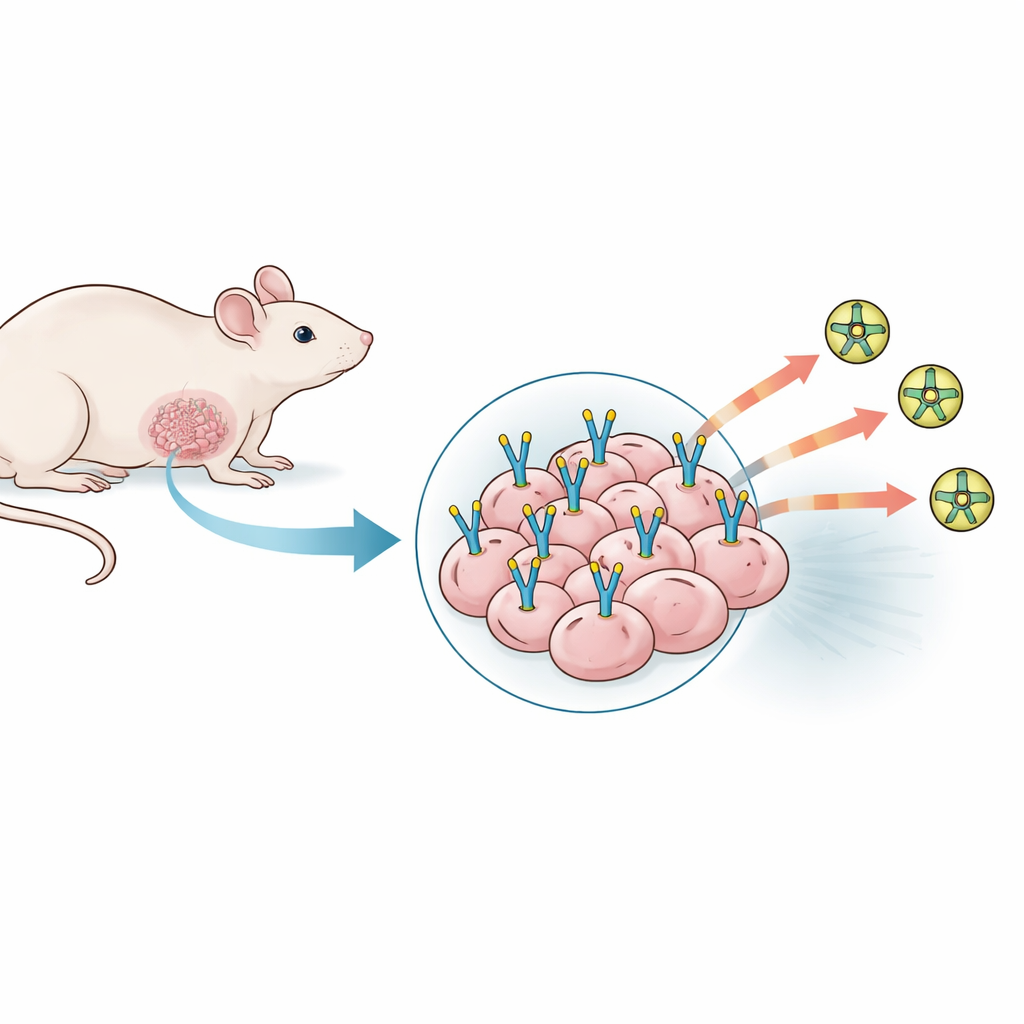
Testowanie wielu modeli guzów, które nie chciały współpracować
Zespół najpierw przebadał szeroki wachlarz istniejących mysich modeli potrójnie ujemnego raka piersi, stosując zarówno mysie, jak i ludzkie linie komórkowe wszczepiane w różnych miejscach i przy różnych warunkach. Zmieniano liczbę wstrzykniętych komórek nowotworowych, dodawano wspierające żele sprzyjające wzrostowi naczyń krwionośnych, a nawet mieszano komórki naczyń krwionośnych pochodzenia ludzkiego, licząc na zwiększenie poziomu PSMA. Dla każdego modelu oceniano, jak niezawodnie guzy się przyjmują i rosną, badano skrawki pod mikroskopem oraz używano PET-tracera celującego w PSMA, aby sprawdzić, czy guzy uwidocznią się w badaniu całego ciała. Pomimo silnego wzrostu guzów i bogatej sieci naczyń krwionośnych, żaden z tych 23 modeli nie wykazał istotnej obecności PSMA ani w barwieniach tkankowych, ani w obrazowaniu PET. Guzy wyglądały na aktywne i dobrze ukrwione, ale specyficzne „miejsce dokowania” PSMA, którego potrzebowali badacze, było w zasadzie nieobecne.
Inżynieria guza eksponującego właściwy cel
W obliczu tej przeszkody badacze poszli bardziej bezpośrednią drogą. Genetycznie zmodyfikowali szeroko stosowaną ludzką linię komórkową potrójnie ujemnego raka piersi MDA-MB-231, wymuszając ekspresję PSMA na jej powierzchni. Tak zmienione komórki wszczepiono następnie do podściółki tłuszczowej gruczołu mlekowego myszy pozbawionych odpowiedzi immunologicznej — miejsca lepiej naśladującego naturalne środowisko piersi. Naukowcy stworzyli dwie wersje modelu: jedną, w której wszystkie komórki guza wyrażały PSMA, oraz „mieszany” guz zawierający równe części komórek pozytywnych na PSMA i zwykłych komórek nowotworowych, aby naśladować mozaikowy wzór obserwowany u pacjentów. Oba modele tworzyły guzy równie niezawodnie i rosły z podobną prędkością jak guzy z komórek niemodyfikowanych, co pokazało, że dodanie PSMA nie zmieniało nieoczekiwanie zachowania samego nowotworu.
Widzenie nowego celu w skanach i pod mikroskopem
Po podaniu PET-tracera celującego w PSMA, zmodyfikowane guzy jasno świeciły na skanach, z wychwytem guza około dziesięciokrotnie wyższym niż w wątrobie lub mięśniach. Ten silny i selektywny sygnał potwierdził, że PSMA jest teraz obficie obecne na komórkach nowotworowych i dostępne dla krążącego leku. Analiza mikroskopowa tkanki zgadzała się z obrazami: barwienie na PSMA było wysokie, ale niejednolite, z obszarami silniejszej i słabszej ekspresji, przypominając heterogenny wzór obserwowany u ludzi z potrójnie ujemnym rakiem piersi. Co ważne, wprowadzone PSMA było ograniczone do komórek guza, a nie do otaczających naczyń krwionośnych, dzięki czemu model koncentruje się na terapiach ukierunkowanych na komórki. Obszary martwicy wewnątrz większych guzów nie pobierały tracera, co odpowiada obserwacjom klinicznym.
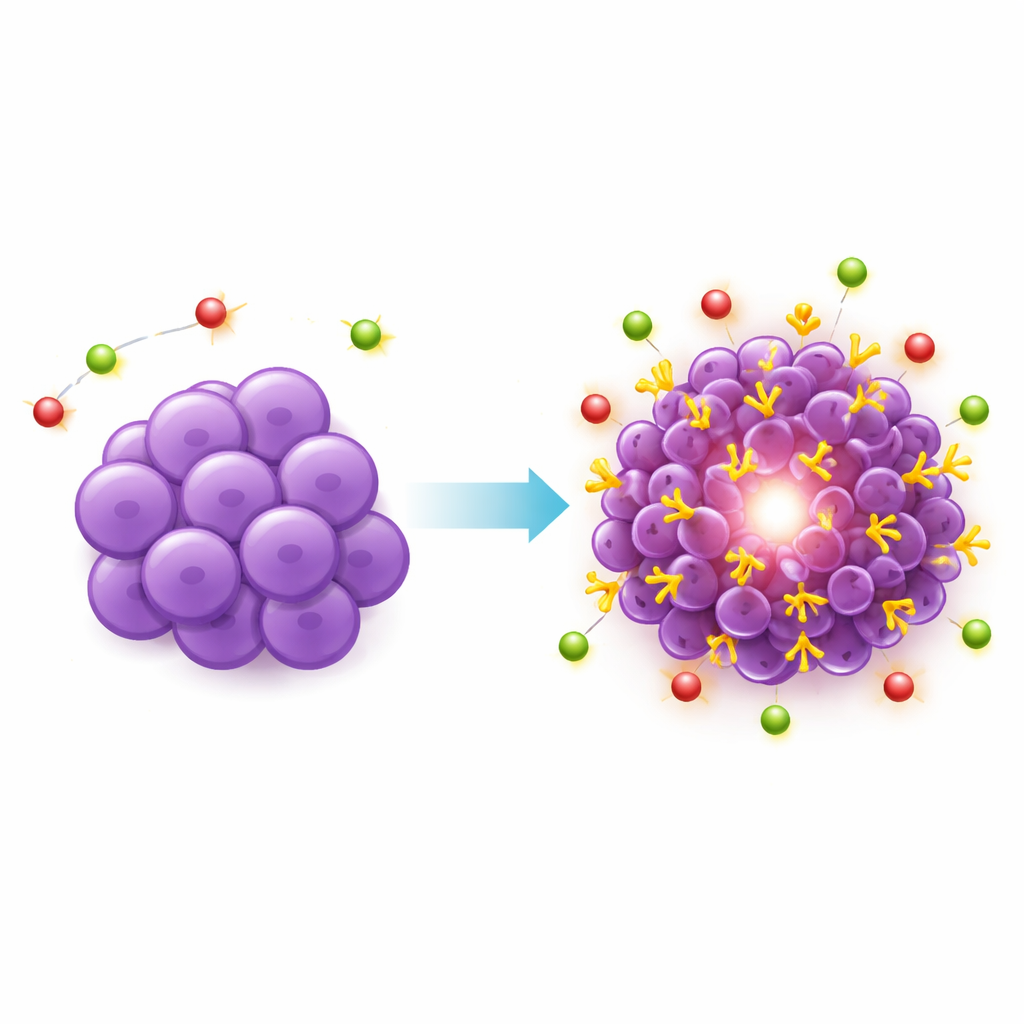
Co to oznacza dla przyszłych terapii
Poprzez systematyczne pokazanie, że standardowe mysie modele raka piersi nie wykazują wiarygodnej ekspresji PSMA, a następnie zbudowanie nowego modelu, który ją wykazuje, ta praca dostarcza kluczowego pola do testowania nowej generacji ukierunkowanych terapii radiacyjnych. PSMA-dodatni model potrójnie ujemnego raka piersi jest stabilny, rośnie przewidywalnie i wykazuje realistyczne zróżnicowanie obszarów o wysokiej i niskiej ekspresji PSMA, co czyni go odpowiednim do oceny zachowania leków skierowanych przeciw PSMA przed próbami u pacjentów. Chociaż model nie oddaje każdego aspektu choroby u ludzi — na przykład wpływu w pełni funkcjonującego układu odpornościowego — oferuje potężne narzędzie do badania, czy sukces terapii opartych na PSMA w raku prostaty można kiedyś rozszerzyć na osoby żyjące z tą szczególnie agresywną postacią raka piersi.
Cytowanie: Chaussin, B., Sanchez, L., Levesque, S. et al. Development and validation of a PSMA-positive triple-negative breast cancer mouse model for preclinical targeted radionuclide therapies. Sci Rep 16, 9348 (2026). https://doi.org/10.1038/s41598-026-36724-7
Słowa kluczowe: potrójnie ujemny rak piersi, PSMA, ukierunkowana terapia radiokinetyczna, przedkliniczny model myszy, obrazowanie PET