Clear Sky Science · pl
Identyfikacja i weryfikacja SPP1 w anoikis jako prognostycznego biomarkera metaplazji jelitowej i raka żołądka
Dlaczego to ma znaczenie dla zdrowia żołądka
Rak żołądka jest jednym z najgroźniejszych nowotworów na świecie, głównie dlatego, że zwykle rozpoznawany jest późno. Zanim pojawi się pełnoobjawowy guz, błona śluzowa żołądka często przechodzi przez ostrzegawczy etap zwany metaplazją jelitową, gdy komórki żołądka zaczynają przypominać komórki jelita. W tym badaniu śledzono całą tę drogę — od tkanki zdrowej, przez metaplazję jelitową, aż po raka żołądka — aby znaleźć pojedynczy mierzalny sygnał w tkance, który mógłby wcześnie wskazywać wysokie ryzyko i pomóc lekarzom przewidzieć, którzy pacjenci mogą mieć gorsze rokowania i skorzystać na bliższej obserwacji lub nowych terapiach.
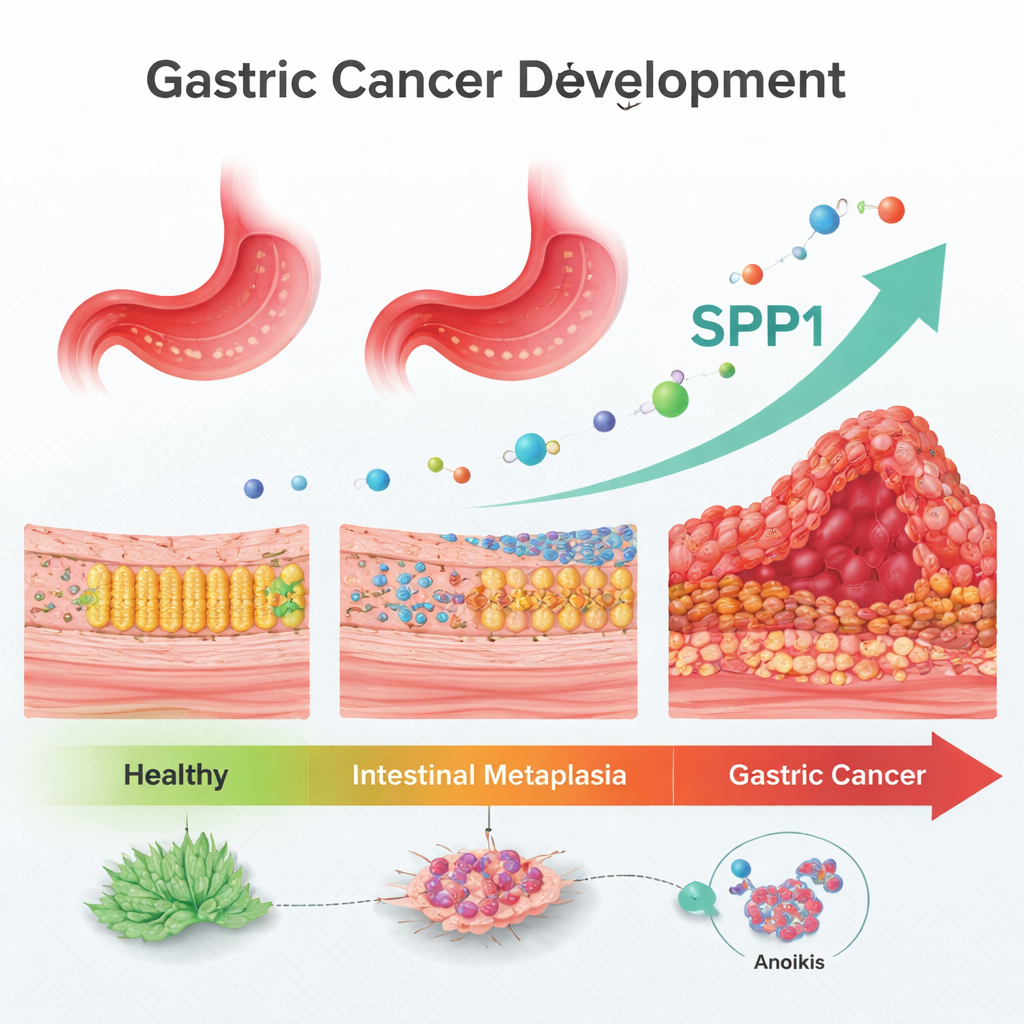
Krok po kroku na drodze do nowotworu
Lekarze od dawna wiedzą, że metaplazja jelitowa jest stanem przednowotworowym, ale brakuje im wiarygodnych markerów, które określałyby, kto faktycznie przejdzie do raka. Badacze skupili się na rodzaju śmierci komórkowej zwanej anoikis, która normalnie eliminuje komórki odłączone od ich prawidłowego miejsca w tkance. Komórki nowotworowe muszą nauczyć się opierać anoikis, aby poruszać się, przetrwać we krwi i zasiedlać odległe miejsca. Analizując duże publiczne bazy danych genowych od setek pacjentów, zespół poszukiwał genów związanych z anoikis, które zmieniają się stopniowo wzdłuż „kaskady Correi”: od zdrowej błony śluzowej, przez metaplazję jelitową, aż do raka żołądka.
Skupienie na kluczowej cząsteczce ostrzegawczej
Stosując zaawansowane narzędzia statystyczne i analizy sieciowe, naukowcy wielokrotnie wyróżnili jeden przełomowy gen: SPP1, kodujący białko znane także jako osteopontyna. W trzech niezależnych zestawach danych poziomy SPP1 były konsekwentnie niskie w zdrowej tkance żołądka, wyższe w metaplazji jelitowej i najwyższe w raku żołądka. Ten stopniowy wzorzec utrzymywał się nawet po skorygowaniu różnic technicznych między badaniami. Dalsze analizy komputerowe tysiąca genów wykazały, że wysoki poziom SPP1 często występował razem ze zmianami w ścieżkach związanych z układem odpornościowym oraz reakcjami na stres środowiskowy i chemiczny, co sugeruje, że cząsteczka ta może łączyć przetrwanie komórek, przewlekłe podrażnienie i układ odpornościowy w procesie powstawania raka.
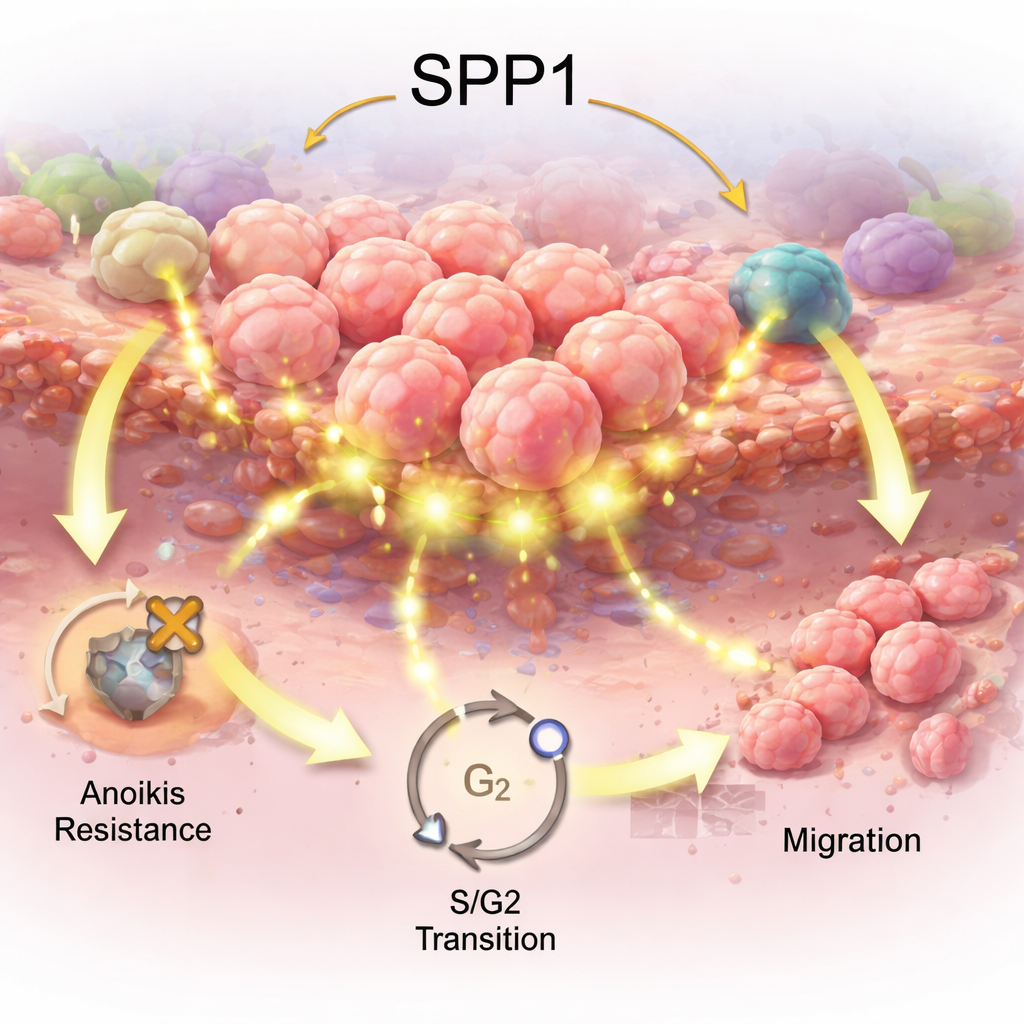
Wskazówki od komórek obronnych organizmu
Następnie zespół zbadał, jak SPP1 wiąże się z komórkami odpornościowymi, które naciekają guzy. W próbkach masowych guzów wyższe SPP1 korelowało ze zmianami w proporcjach komórek odpornościowych, w tym ze wzrostem pewnych makrofagów i komórek T, które mogą albo zwalczać nowotwór, albo zostać przez niego wyciszone. Sekwencjonowanie RNA pojedynczych komórek — odczyt aktywności genów po komórce — pokazało, że SPP1 jest silnie włączone w makrofagach związanych z guzem oraz innych komórkach mikrośrodowiska guza. Sygnały obejmujące SPP1 i jego receptor-partner CD44 wydawały się łączyć te makrofagi z pomocniczymi komórkami T, co sugeruje, że ta droga może pomagać tworzyć „sąsiedztwo” immunologiczne sprzyjające przetrwaniu guza zamiast jego eliminacji. Choć te powiązania są korelacyjne, wskazują na SPP1 jako potencjalnego uczestnika w mechanizmach, dzięki którym raki żołądka unikają ataku odpornościowego.
Od big data do rzeczywistych tkanek i komórek
Aby sprawdzić, czy wyniki komputerowe odpowiadają rzeczywistości, badacze zmierzyli SPP1 w 32 ludzkich próbkach tkanki żołądka. Zarówno testy genowe, jak i białkowe pokazały ten sam trend: najniższe poziomy w tkance normalnej, wyższe w metaplazji jelitowej i najwyższe w raku żołądka. Pacjenci, których guzy wyrażały więcej SPP1, mieli znacząco gorsze przeżycie ogólne, a modele statystyczne sugerowały, że SPP1 pomaga przewidywać wyniki jedno-, trzy- i pięcioletnie. W hodowlach komórkowych obniżenie ekspresji SPP1 w linii komórek raka żołądka spowolniło wzrost komórek, zmniejszyło ich zdolność migracji, zwiększyło programowaną śmierć komórek i spowodowało zatrzymanie w krytycznej fazie cyklu komórkowego. Eksperymenty te wspierają hipotezę, że SPP1 aktywnie pomaga komórkom nowotworowym opierać się śmierci i dalej się dzielić.
Co to może znaczyć dla pacjentów
Dla czytelników niebędących specjalistami najważniejsze jest to, że SPP1 zachowuje się jak rosnący sygnał alarmowy na drodze od „ryzykownej, ale jeszcze nie nowotworowej” błony śluzowej do pełnego raka. Wysokie poziomy tej cząsteczki oznaczają tkanki bardziej skłonne do progresji i pacjentów z gorszym rokowaniem. Choć potrzeba dalszych badań — zwłaszcza większych badań pacjentów i eksperymentów na zwierzętach — monitorowanie SPP1 w biopsjach z metaplazji jelitowej mogłoby w przyszłości pomóc lekarzom zdecydować, kto wymaga bliższej kontroli lub wcześniejszego leczenia. W przypadku ustalonego raka żołądka leki blokujące SPP1 lub jego kluczowych partnerów mogłyby osłabić obronę guza, zarówno czyniąc komórki nowotworowe bardziej podatnymi na śmierć, jak i przekształcając otaczające komórki odpornościowe, aby skuteczniej zwalczały chorobę.
Cytowanie: Wu, K., Ye, Y., Pei, B. et al. Identification and verification of SPP1 in anoikis as a prognostic biomarker for intestinal metaplasia and gastric cancer. Sci Rep 16, 5842 (2026). https://doi.org/10.1038/s41598-026-36714-9
Słowa kluczowe: rak żołądka, metaplazja jelitowa, biomarkery, osteopontyna SPP1, mikrośrodowisko guza