Clear Sky Science · pl
Czy terapię ewolucyjną można zastosować w niedrobnokomórkowym raku płuca?
Ponowne przemyślenie leczenia raka jako konkursu ewolucyjnego
Opieka nad chorobą nowotworową jest często przedstawiana jako prosta bitwa: zastosować najsilniejsze możliwe leki i spróbować wyeliminować każdą komórkę nowotworową. Jednak w szybkim, agresywnym nowotworze, takim jak zaawansowany niedrobnokomórkowy rak płuca (NSCLC), to podejście „maksymalnego ataku” często się zemści. Guzy początkowo się zmniejszają, ale niemal zawsze odrastają, teraz zdominowane przez komórki odporne na leki. Badanie stawia prowokujące pytanie: co jeśli zamiast próbować zniszczyć guz, lekarze potraktowaliby go jak ewolu ekosystem i stosowali schematy dawkowania, które celowo pozostawiają część wrażliwych na lek komórek przy życiu, aby powstrzymywały komórki odporne?
Dlaczego standardowe leczenie dużymi dawkami może przyspieszać oporność
W obecnej praktyce pacjenci z przerzutowym NSCLC i określonymi zmianami genetycznymi często otrzymują codzienne pigułki zwane inhibitorami kinazy tyrozynowej (TKI), takie jak erlotynib. Leki te mogą początkowo dramatycznie zmniejszyć guzy, ale niemal wszyscy pacjenci ostatecznie doświadczają nawrotu, ponieważ przetrwały komórki odporne. Gdy lekarze zwiększają dawkę do maksymalnej tolerowanej przez pacjenta, głównie zabijają komórki wrażliwe, które dobrze odpowiadają na lek. Komórki odporne, które potrafią przetrwać nawet duże dawki, nagle mają mniej konkurencji o przestrzeń i zasoby. W rezultacie dochodzi do ewolucyjnego „zwycięstwa” najsilniejszych komórek nowotworowych, a guz wraca, teraz znacznie trudniejszy do leczenia. 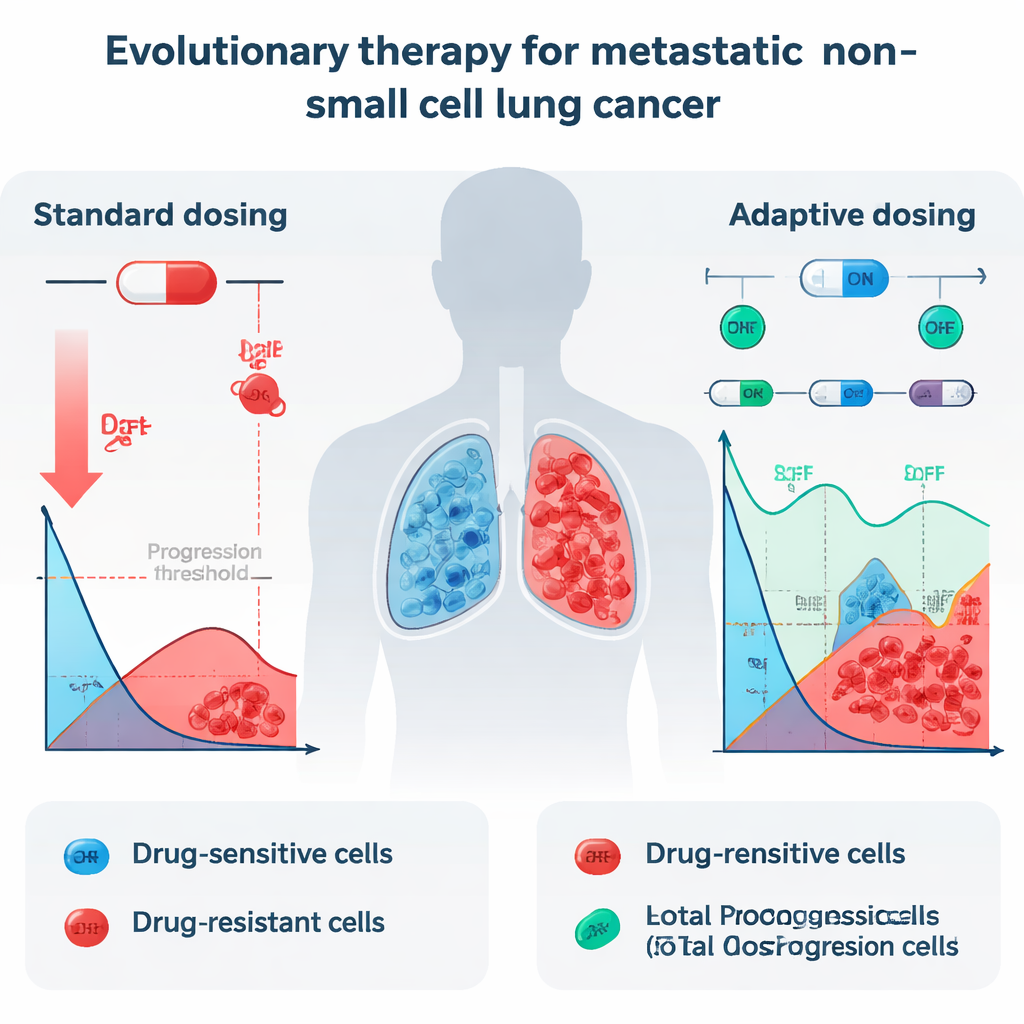
Użycie matematyki do przetestowania nowej strategii dawkowania na rzeczywistych pacjentach
Naukowcy zbadali, czy inna strategia, zwana terapią ewolucyjną, mogłaby zadziałać w NSCLC w stadium IV. Terapia ewolucyjna nie dąży do całkowitego wyeliminowania guza. Zamiast tego próbuje go kontrolować, utrzymując stabilny udział komórek wrażliwych i odpornych, pozwalając komórkom wrażliwym „wypierać” odporne. Zespół zapożyczył konkretny protokół dawkowania „włącz‑wyłącz”, który już wykazał obiecujące wyniki w raku prostaty, a następnie zapytał: czy ten rodzaj strategii byłby teoretycznie skuteczny również w raku płuca? Aby to sprawdzić, przeanalizowali szczegółowe pomiary rozmiaru guza u 13 pacjentów z NSCLC leczonych erlotynibem w badaniu klinicznym, przekształcili skany w całkowitą objętość guza w czasie i wprowadzili te dane do zestawu modeli matematycznych.
Odnalezienie modelu, który rzeczywiście oddaje oporność
Badacze przetestowali 26 różnych modeli wzrostu guza, wszystkie dzieląc komórki nowotworowe na dwie grupy: wrażliwe na lek i odporne na lek. Modele różniły się tym, jak opisywały ograniczenia wzrostu, jak dwa typy komórek ze sobą konkurują, jak lek jest przetwarzany w organizmie i jak leczenie zabija komórki. Wiele prostszych modeli dobrze dopasowywało się do danych pacjentów, gdy guzy tylko się zmniejszały. Jednak gdy guzy podążały bardziej realistyczną „U-kształtną” ścieżką — kurczyły się pod wpływem leczenia, a potem odrastały wraz z pojawieniem się oporności — większość modeli zawodziła. Najlepiej pasował model typu gompertzjańskiego, który zawierał dwa kluczowe założenia: po pierwsze, guzy nie mogą rosnąć bez ograniczeń (odczuwają tłok), a po drugie, komórki wrażliwe i odporne konkurują w sposób asymetryczny, więc powodzenie jednego typu zależy od liczebności drugiego.
Symulacja terapii adaptacyjnej w porównaniu ze standardową opieką
Gdy zidentyfikowano najlepiej dopasowane modele, zespół użył ich do symulacji dwóch strategii leczenia dla każdego pacjenta: zwykłej stałej maksymalnej dawki oraz protokołu adaptacyjnego inspirowanego pracą Zhanga i współpracowników. W podejściu adaptacyjnym erlotynib podawano aż do momentu, gdy guz skurczył się do połowy swojej pierwotnej wielkości, następnie przerwano lek, aby pozwolić komórkom wrażliwym odrosnąć; leczenie wznawiano, gdy guz wracał do wyjściowego rozmiaru, i cykl się powtarzał. We wszystkich dobrze działających modelach, które uwzględniały konkurencję między typami komórek, ta adaptacyjna strategia konsekwentnie opóźniała moment, w którym guz przekraczał 110% początkowego rozmiaru — powszechny punkt odniesienia progresji. W najlepiej dopasowanym modelu gompertzjańskim z konkurencją mediana czasu do progresji wydłużyła się z około 24,8 miesiąca przy standardowym dawkowaniu do 42,3 miesiąca przy protokole adaptacyjnym, zyskując mniej więcej półtora roku. 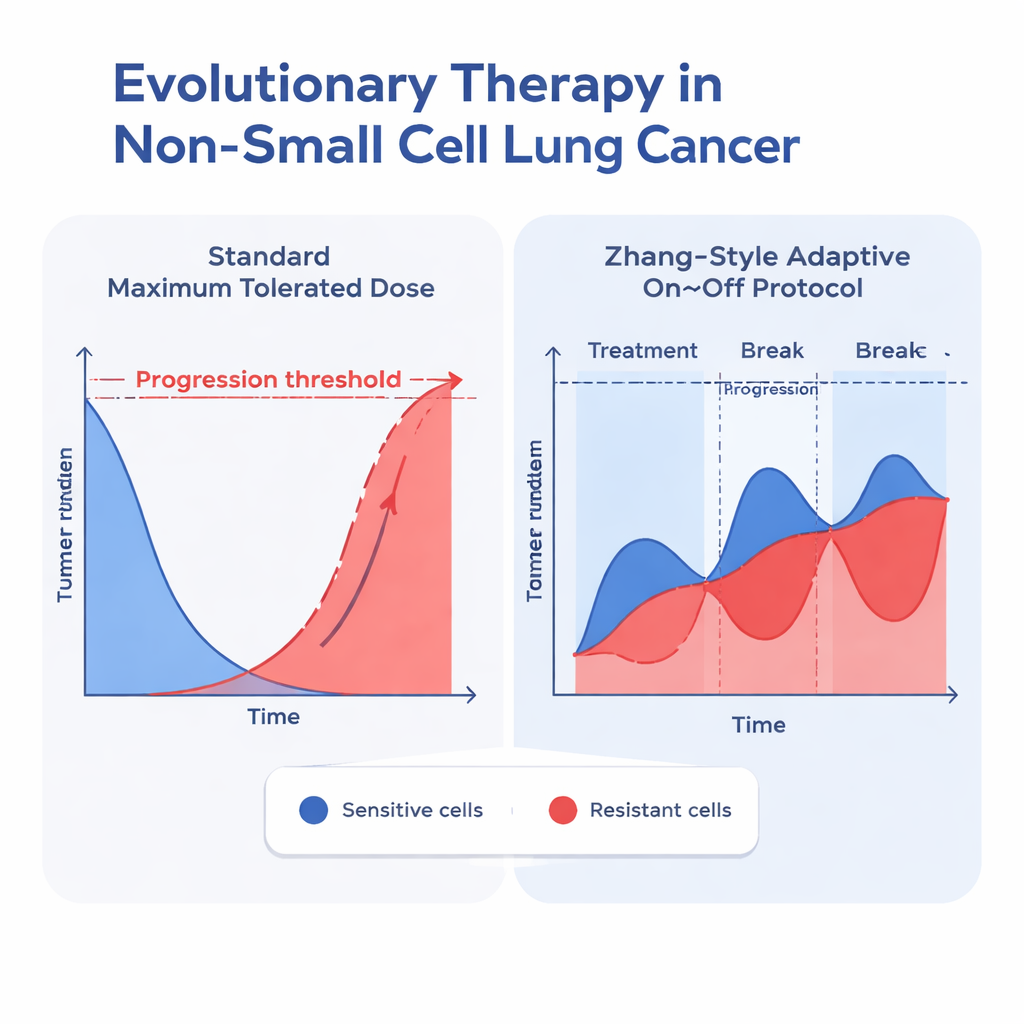
Co to może oznaczać dla przyszłych pacjentów
Ta praca jeszcze nie zmienia sposobu, w jaki dziś lekarze leczą pacjentów z NSCLC, ale stanowi mocne potwierdzenie koncepcji. Opierając swoje modele na rzeczywistych danych pacjentów i wymagając, by modele odtwarzały nie tylko wczesne kurczenie się guza, ale także odrastanie napędzane opornością, autorzy pokazują, że terapia ewolucyjna jest teoretycznie wykonalna nawet w szybko rosnącym i śmiertelnym nowotworze. Ich wyniki sugerują, że starannie zaplanowane przerwy w leczeniu mogą wydłużyć kontrolę choroby, wykorzystując komórki wrażliwe jako sojuszników, a nie jako kolateralne straty. Wdrożenie tej idei w praktyce będzie wymagać więcej danych, lepszych biomarkerów, takich jak badania krwi śledzące DNA nowotworu, oraz rygorystycznych badań klinicznych. Mimo to przesłanie dla czytelników niebędących specjalistami jest jasne: czasami najrozsądniejszym sposobem walki z rakiem nie jest uderzanie w niego jak najmocniej, lecz ukierunkowanie jego ewolucji tak, by pozostał możliwym do kontrolowania, wolniej poruszającym się przeciwnikiem.
Cytowanie: Jansén-Storbacka, L.R., Honasoge, K.S., Molnárová, E. et al. Can evolutionary therapy be applied in non-small cell lung cancer?. Sci Rep 16, 7442 (2026). https://doi.org/10.1038/s41598-026-36712-x
Słowa kluczowe: terapia ewolucyjna, niedrobnokomórkowy rak płuca, oporność na leki, dawkowanie adaptacyjne, matematyczna onkologia