Clear Sky Science · pl
Zastosowanie Lactococcus ekspresującego kolagenopodobny białko 1 paciorkowców grupy A jako nowego immunoterapeutyku przeciwko gruczolakorakowi przewodów trzustkowych
Przekształcanie „dobrych” bakterii w wojowników przeciw nowotworom
Rak trzustki jest jednym z najgroźniejszych nowotworów, częściowo dlatego, że ukrywa się za potężnymi barierami tłumiącymi odpowiedź immunologiczną organizmu. W tym badaniu badacze rozważają nieoczekiwanego sojusznika w walce z tą chorobą: powszechną „dobrą” bakterię z świata produktów mlecznych, przeprojektowaną tak, by lokowała się w guzach trzustki i pomagała układowi odpornościowemu skuteczniej je atakować. Dzięki użyciu lepkiego białka powierzchniowego zapożyczonego od groźnego paciorkaowca, naukowcy przekształcili nieszkodliwy mikrob w celowany, przeciwnowotworowy środek u myszy.
Trudny nowotwór, który przechytrza układ odpornościowy
Gruczolakorak przewodów trzustkowych jest notorycznie śmiertelny — tylko około jedna na osiem pacjentów przeżywa pięć lat od rozpoznania. Jednym z głównych powodów jest mikrośrodowisko guza: gęsta, przypominająca bliznę otoczka wypełniona komórkami i cząsteczkami, które tłumią ataki immunologiczne i blokują wiele leków. Jednymi z winowajców są neutrofilowe pułapki zewnątrzkomórkowe, zwane NET — sieci DNA i białek, które komórki odpornościowe wyrzucają do otoczenia. W raku trzustki te lepkie sieci przynoszą więcej szkody niż pożytku: sprzyjają wzrostowi guza, trzymają z dala cytotoksyczne komórki T i wiążą się z gorszymi wynikami leczenia. Zablokowanie NET przy jednoczesnym pobudzeniu przeciwguenowej odpowiedzi immunologicznej stało się atrakcyjną strategią.
Pożyczenie lepkiego białka, ale nie groźnego zarazka
Wcześniejsze badania wykazały, że białko powierzchniowe z paciorkowców grupy A, zwane Scl1, może zarówno przyczepiać się do włóknistej macierzy związanej z guzem, jak i hamować tworzenie NET, spowalniając wzrost guzów trzustki u myszy. Jednak paciorkowiec grupy A jest też bakterią wywołującą anginę i poważne zakażenia inwazyjne, co czyni go nieodpowiednim jako żywe leczenie. Aby zachować korzystne białko, unikając przy tym niebezpiecznego zarazka, zespół genetycznie zmodyfikował Lactococcus lactis — probiotyk szeroko stosowany w żywności i uznawany za bezpieczny — tak by eksponował Scl1 na swojej powierzchni. Nowy szczep, nazwany Lactococcus::620, testowano u myszy z guzami trzustki, używając zarówno prostszych guzów na flankach, jak i bardziej realistycznych guzów rosnących w samej trzustce.
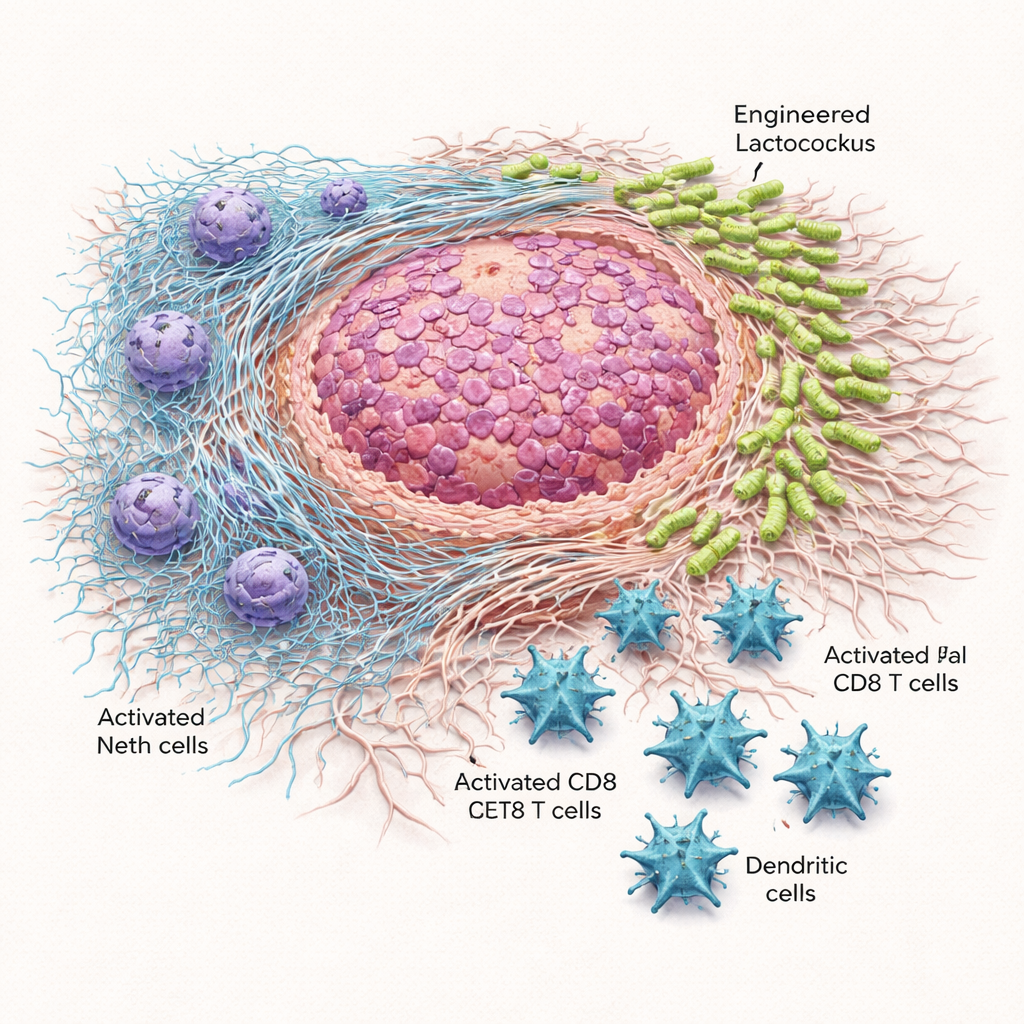
Ukierunkowane bakterie hamują wzrost guza i przedłużają przeżycie
Gdy pojedynczą dawkę modyfikowanych bakterii wstrzyknięto bezpośrednio do guzów na flankach lub podano do jamy brzusznej, guzy rosły wolniej i ważyły mniej niż u myszy otrzymujących zwykły Lactococcus lub sól fizjologiczną. W bardziej wymagającym modelu trzustkowym konieczne były wielokrotne dawki co trzy dni, ale korzyści były znaczące. Lactococcus::620 zmniejszał rozmiar guzów, redukował ich masę i wydłużał przeżycie zwierząt bez powodowania zgonów związanych z leczeniem. Mikroskopia i hodowla tkanki nowotworowej pokazały, że bakterie noszące Scl1 konsekwentnie gromadziły się w obszarze guza, szczególnie w włóknistej macierzy wytwarzanej przez fibroblasty związane z nowotworem, przy jednoczesnym względnym oszczędzaniu śledziony. Dla kontrastu, niemodyfikowany Lactococcus rozprzestrzeniał się szerzej w organizmie i czasami był toksyczny przy podawaniu systemowym.
Rozbrajanie szkodliwych sieci i wpuszczanie komórek odpornościowych
Modyfikowane bakterie zmieniły też krajobraz immunologiczny wokół guzów. Guzy od myszy leczonych Lactococcus::620 zawierały więcej komórek CD8, czyli „zabójczych” limfocytów T, oraz komórek dendrytycznych — kluczowych uczestników rozpoznawania i niszczenia komórek nowotworowych — a te limfocyty wykazywały mniej markerów wyczerpania i więcej cząsteczek związanych z aktywnością. Równocześnie zmniejszyły się wskaźniki aktywności NET. W testach in vitro neutrofile narażone na Lactococcus::620 uwalniały mniej wolnego DNA i wykazywały niższą aktywność mieloperoksydazy, enzymu niezbędnego do budowy NET. U leczonych myszy obniżył się poziom krążącego DNA związanego z NET. Co istotne, kiedy te same eksperymenty przeprowadzono u myszy genetycznie niezdolnych do formowania NET, modyfikowane bakterie przestały hamować wzrost guza. Utrata efektu silnie sugeruje, że blokowanie NET jest kluczowe dla działania terapii.
Co to może znaczyć dla przyszłej opieki onkologicznej
W sumie wyniki przedstawiają nową koncepcję: użycie bezpiecznej, żywieniowej bakterii jako programowalnego nośnika dostarczającego blokujące NET, do tego homingowe białko prosto do wrogiego mikrośrodowiska raka trzustki. U myszy takie podejście zmniejszyło obciążenie guzem, poprawiło przeżycie i umożliwiło komórkom odpornościowym skuteczniejsze działanie. Choć przed próbami u ludzi stoi jeszcze wiele pracy — w tym testy w modelach choroby przerzutowej i łączenie tej strategii z nowoczesnymi immunoterapiami — badanie pokazuje, że starannie zaprojektowane „dobre” bakterie mogą pewnego dnia pomóc przechylić szalę przeciw jednemu z najbardziej opornych nowotworów.
Cytowanie: Godfrey, E.A., Choi, S.J., Sestito, M. et al. Application of group A streptococcal collagen-like protein 1-expressing Lactococcus as a novel immunotherapeutic against pancreatic ductal adenocarcinoma. Sci Rep 16, 5911 (2026). https://doi.org/10.1038/s41598-026-36657-1
Słowa kluczowe: rak trzustki, terapia probiotyczna, mikrośrodowisko guza, modulacja układu odpornościowego, neutrofilowe pułapki zewnątrzkomórkowe