Clear Sky Science · pl
Marker powierzchniowe na supermerach przewyższają pęcherzyki pozakomórkowe w diagnostyce raka jelita grubego
Dlaczego mikroskopijne cząstki we krwi mogą zmienić badania przesiewowe w onkologii
Rak jelita grubego jest jednym z najczęstszych nowotworów na świecie, a lekarze pilnie potrzebują lepszych testów krwi, które wykryją go wcześnie i pozwolą monitorować skuteczność leczenia. Badanie to analizuje nowo rozpoznawaną klasę ultramłych cząstek we krwi, nazywanych „supermerami”, i pokazuje, że mogą one przenosić wyraźniejsze sygnały nowotworowe niż lepiej znane cząstki. Autorzy prezentują też szybki sensor, który potrafi zmierzyć supermery bezpośrednio z maleńkiej kropli krwi w mniej niż pół godziny, co może otworzyć drogę do szybszej i dokładniejszej diagnostyki nowotworów.
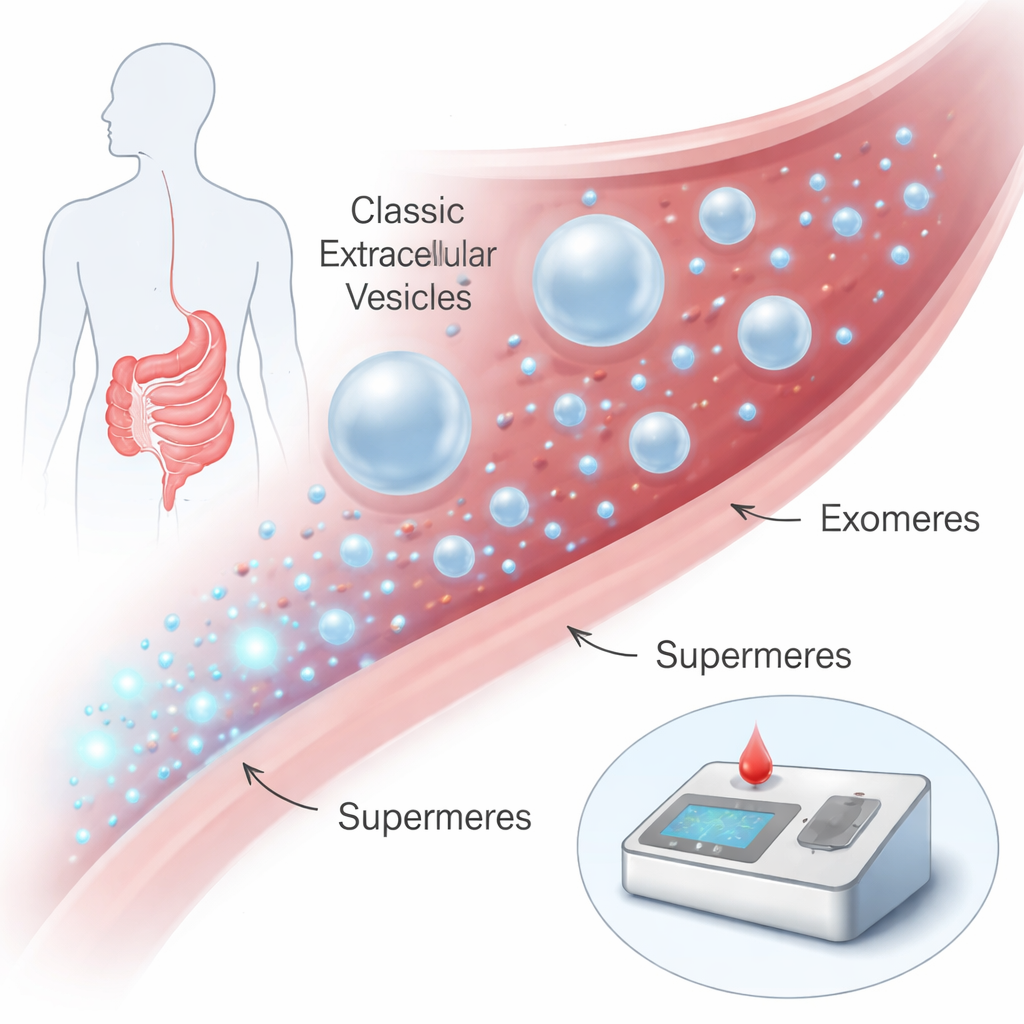
Maleńcy posłańcy w krwiobiegu
Nasze komórki nieustannie uwalniają nanoskopijne paczki do płynów ustrojowych, takich jak krew. Przez lata największą uwagę skupiano na otoczonych błoną cząstkach, takich jak egzososomy i inne pęcherzyki pozakomórkowe, które mogą przenosić białka i materiał genetyczny między komórkami i badano je jako biomarkery chorób. W ostatnim czasie badacze odkryli jeszcze mniejsze, niemembranowe cząstki zwane egzomerami, a jeszcze mniejsze — supermerami. Supermery mają zaledwie około 15–25 nanometrów średnicy — tysiące zmieściłyby się na szerokości ludzkiego włosa — a mimo to zawierają wiele cząsteczek związanych z chorobami. Wcześniejsze prace sugerowały, że supermery mogą być szczególnie bogate w sygnały nowotworowe, lecz ich izolacja i badanie były trudne i wymagały dni ultrawirowania oraz specjalistycznego sprzętu.
Co wyróżnia supermery
Zespół starannie rozdzielił trzy główne typy nanocząstek z hodowli komórek nowotworowych i ludzkiej krwi: małe pęcherzyki pozakomórkowe, egzomery i supermery. Potwierdzili, że każda grupa ma charakterystyczny zakres rozmiarów, a supermery są najmniejsze. Kluczowa różnica była jednak elektryczna. Supermery miały znacznie silniejszy ujemny ładunek powierzchniowy niż pozostałe cząstki — około dwukrotnie przekraczający poziom, przy którym istotne stają się losowe ruchy termiczne — co w dużej mierze wynikało z nici RNA przylegających do ich powierzchni. Kiedy badacze strawili te RNA enzymami, ładunek gwałtownie spadł, co pokazuje, że RNA powierzchniowe są centralne dla elektrostycznego sygnatu supermerów. Mapowanie białek ujawniło też, że supermery mają własne „znaczniki identyfikacyjne”: białka takie jak HSPA13, ENO2 i DDR1 były silnie wzbogacone w supermerach, a w dużej mierze nieobecne w innych typach cząstek, podobnie jak klasyczne markery identyfikujące zwykłe pęcherzyki pozakomórkowe.
Szybki sensor reagujący na ładunek
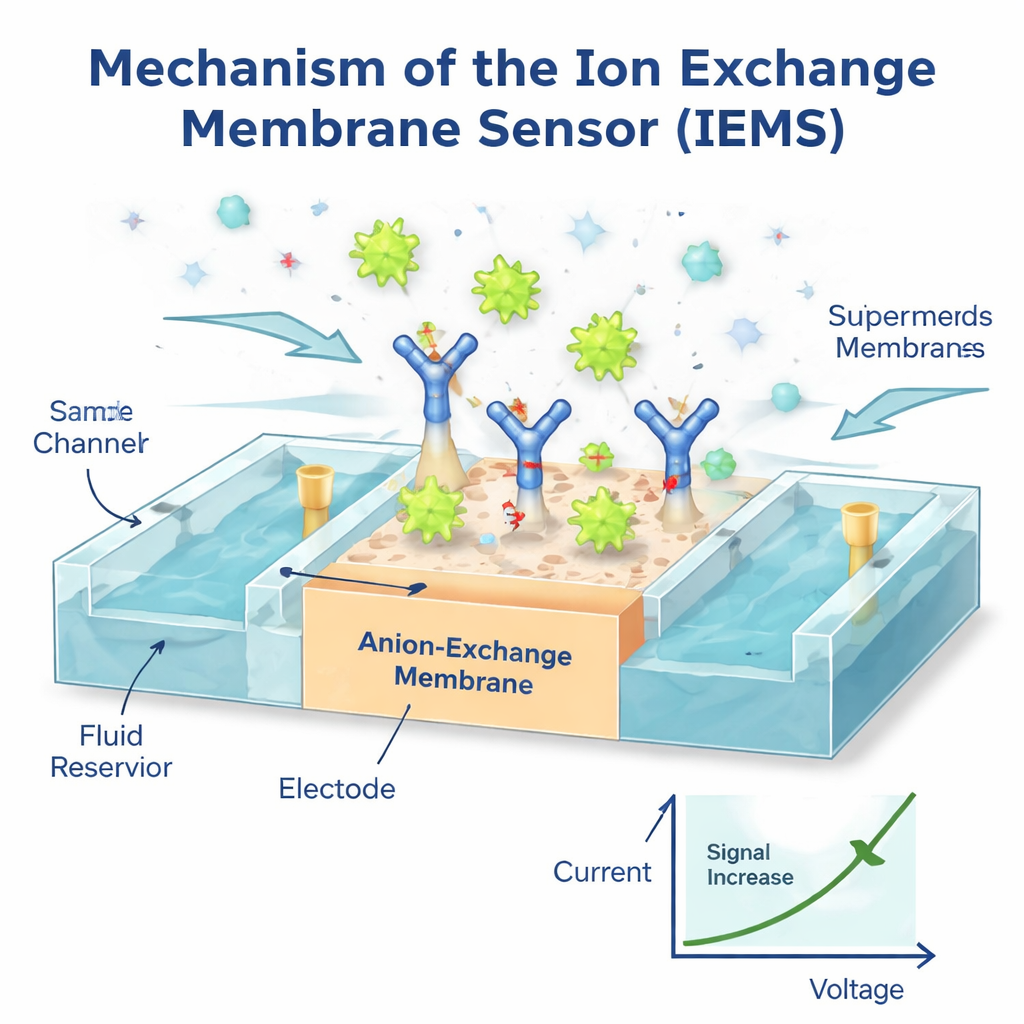
Aby wykorzystać te unikalne właściwości, autorzy stworzyli Sensor Membrany Wymiany Jonowej (IEMS), małe urządzenie wykrywające zmiany prądu elektrycznego w miarę, jak na jego powierzchni wiążą się naładowane cząstki. Pokryli specjalną membranę przeciwciałami, które wyłapują wybrane białko, na przykład marker związany z nowotworem, z przepływającej próbki krwi. Ponieważ supermery są tak silnie naładowane, a większość innych cząstek i wolnych białek słabo naładowana, tylko wychwycone supermery znacząco zmieniają charakterystykę prądowo-napięciową membrany. W efekcie powstaje silny, selektywny sygnał elektryczny odzwierciedlający liczbę supermerów niosących dany marker. Dzięki temu układowi zespół mógł wykryć już milion supermerów na mililitr w zakresie stężeń rozciągającym się tysiąckrotnie, wszystko w około 30 minut i wykorzystując tylko 50 mikrolitrów próbki — bez długotrwałej oczyszczającej procedury. Testy, w których dodano znane ilości supermerów do zdrowej plazmy, wykazały niemal całkowite odzyskanie, a pomiary zgadzały się z wynikami wolniejszych, zaawansowanych instrumentów optycznych.
Przewaga nad istniejącymi markerami nanocząstek
Posługując się zarówno tradycyjnymi, jak i szybkimymi metodami, badacze porównali supermery bezpośrednio z egzomerami i małymi pęcherzykami pozakomórkowymi w próbkach krwi osób z rakiem jelita grubego oraz zdrowych ochotników. Skoncentrowali się na kilku białkach występujących we wszystkich trzech typach cząstek, w tym na znanych markerach nowotworowych, takich jak CEA i GPC1. Dla niemal każdego wspólnego białka sygnał niesiony przez supermery lepiej lub przynajmniej równie dobrze rozróżniał pacjentów z rakiem od osób zdrowych, podczas gdy egzomery często miały niewielką wartość diagnostyczną. Specyficzne dla supermerów białka, takie jak HSPA13, ENO2 i DDR1, okazały się szczególnie wymowne: były praktycznie nieobecne w zdrowej plazmie, a wyraźnie podwyższone w raku jelita grubego, co zapewniało doskonałe rozróżnienie między grupami. Co godne uwagi, u dwóch pacjentów badanych przed i po operacji usunięcia guza poziomy supermerów gwałtownie spadły po zabiegu, podczas gdy sygnały z tradycyjnych pęcherzyków zmieniły się bardzo niewiele, co sugeruje, że supermery ściśle odzwierciedlają obciążenie guzem.
Co to może oznaczać dla przyszłych testów nowotworowych
Aby sprawdzić nowy sensor w realistycznych warunkach, zespół użył IEMS do pomiaru supermerów niosących różne markery w plazmie pochodzącej od chorych na raka jelita grubego, raka trzustki, glejaka oraz od dawców zdrowych. Szybkie, nie wymagające izolacji odczyty zgadzały się ściśle z wynikami znacznie wolniejszego ultrawirowania połączonego z analizą optyczną, potwierdzając, że szybkość nie odbywa się kosztem dokładności. W raku jelita grubego pomiary oparte na supermerach przewyższały całkowite stężenia CEA we krwi, długo stosowanego klinicznego markera. W sumie wyniki sugerują, że supermery to nie kolejna mikroskopijna ciekawostka, lecz potężne i dostępne źródło informacji o nowotworze. Jeśli zostaną zweryfikowane w większych i bardziej zróżnicowanych grupach pacjentów, pomiar supermerów niosących markery przy użyciu kompaktowych sensorów reagujących na ładunek mógłby stać się praktycznym sposobem przesiewania raka jelita grubego, monitorowania leczenia i ewentualnego dopasowywania terapii przy znacznie krótszym czasie, mniejszej objętości próbki i mniejszej złożoności niż obecne metody.
Cytowanie: Kumar, S., Sinclair, J.A., Shi, T. et al. Surface markers on supermeres outperform extracellular vesicles in colorectal cancer diagnosis. Sci Rep 16, 5989 (2026). https://doi.org/10.1038/s41598-026-36626-8
Słowa kluczowe: rak jelita grubego, biomarkery we krwi, nanocząstki pozakomórkowe, supermery, technologia biosensorów