Clear Sky Science · pl
Połączone działanie azotanów i środków przeciwbakteryjnych na hodowle poddziąsłowe in vitro
Dlaczego Twoje dziąsła i lekarstwa działające w jelitach są powiązane
Krwawiące dziąsła i choroby przyzębia zwykle obwinia się o „złe” bakterie. Aby z nimi walczyć, dentyści często sięgają po silne płukanki i antybiotyki. To badanie stawia szersze pytanie: co jeśli niektóre z tych terapii po cichu uszkadzają pożyteczne bakterie, których potrzebujemy, podczas gdy prosty składnik odżywczy obecny w zielonych warzywach rzeczywiście przesuwa mikrobiotę jamy ustnej w stronę zdrowia?
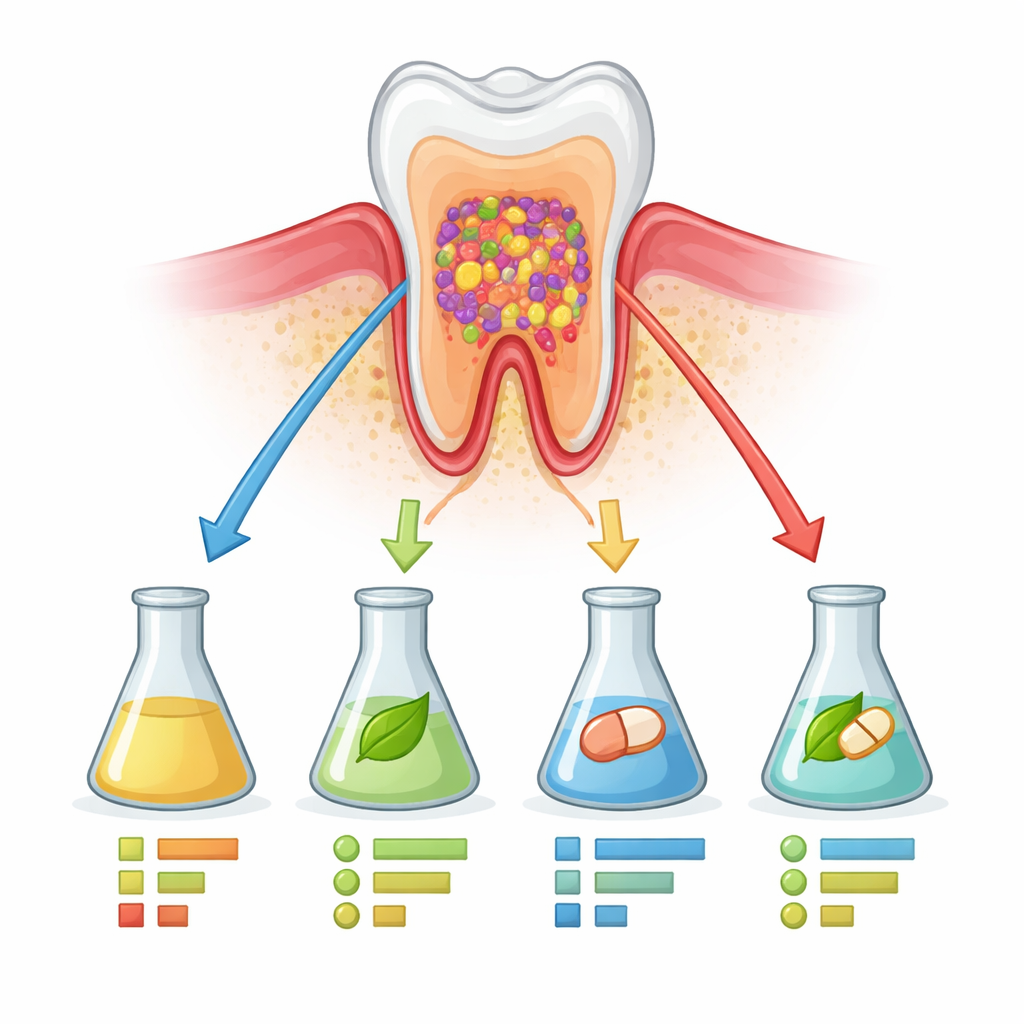
Choroba przyzębia jako problem społecznościowy
Periodontitis to przewlekła infekcja wokół zębów, która niszczy tkanki utrzymujące zęby na miejscu i jest powiązana z chorobami serca, cukrzycą, a nawet schorzeniami mózgu. Zamiast być wywoływana przez jeden patogen, powstaje wtedy, gdy cała społeczność bakterii jamy ustnej przesuwa się w stronę szkodliwego stanu, zwanego dysbiozą. Współczesne leczenie nadal w dużym stopniu opiera się na szeroko działających lekach: antybiotykach takich jak amoksycylina i metronidazol oraz środkach antyseptycznych do płukania, jak chlorheksydyna. Te produkty mogą zabijać sprawców problemów — ale też eliminować przyjazne bakterie i mogą sprzyjać oporności na leki.
Bliższe spojrzenie na biofilmy z próbek pacjentów
Aby zobaczyć, co te terapie naprawdę robią bakteriom przyzębia, badacze zebrali płytkę nazębną z głębokich kieszonek przyzębnych od 12 osób z periodontitis. W laboratorium hodowali te próbki jako cienkie warstwy bakterii, czyli biofilmy, przez osiem godzin w ośmiu różnych warunkach: bez leczenia, z samym azotanem, z każdym lekiem osobno oraz z każdym lekiem w połączeniu z azotanem. Azotan, naturalny związek obfity w szpinaku, sałacie i burakach, może być przekształcany przez niektóre bakterie jamy ustnej w tlenek azotu — gaz, który pomaga rozluźniać naczynia krwionośne i może spowalniać wzrost drobnoustrojów związanych z chorobą. Zespół mierzył, ile biofilmu powstało, jak dobrze przekształcano azotan oraz które gatunki bakterii dominowały przy każdym leczeniu.
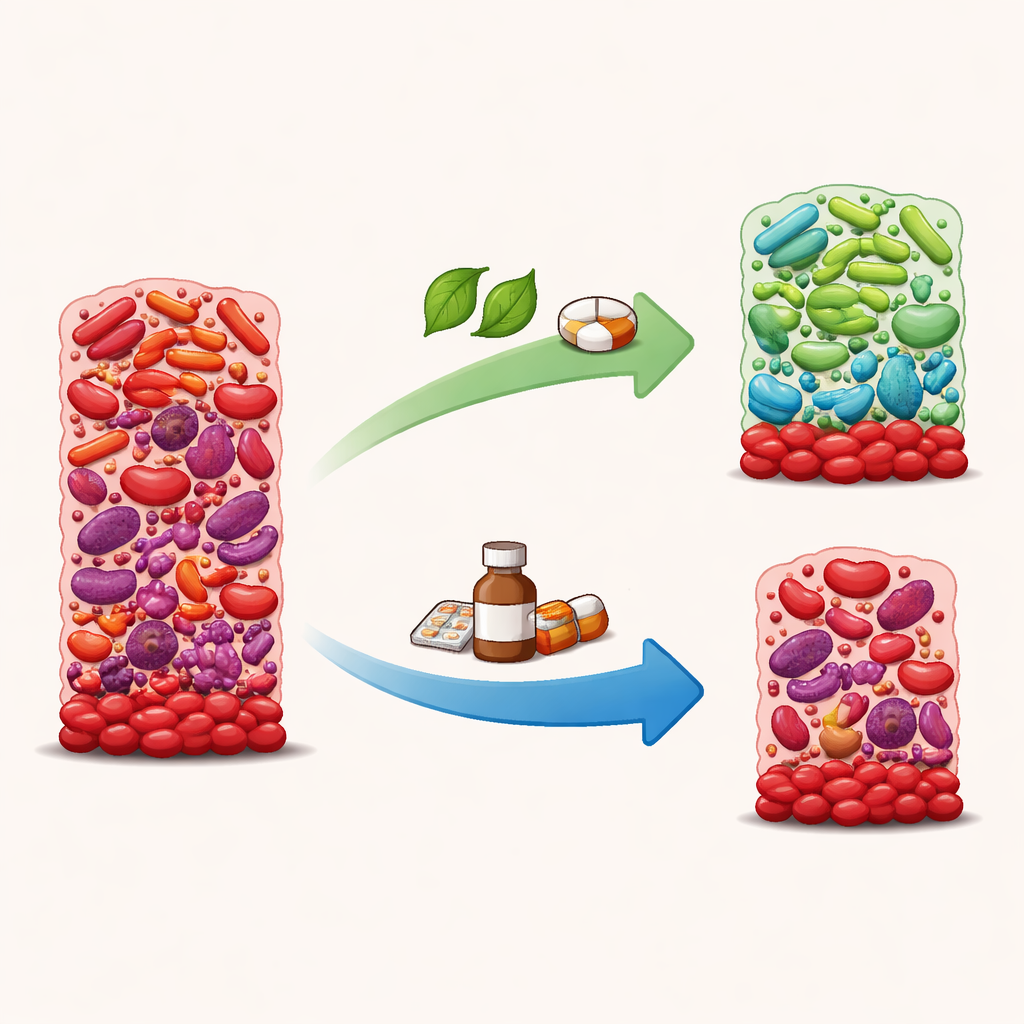
Leki zmniejszające wzrost, które mogą pogorszyć równowagę
Niskie dawki chlorheksydyny i amoksycyliny zmniejszyły wzrost biofilmu mniej więcej o połowę i silnie ograniczyły zdolność bakterii do przetwarzania azotanu. Jednak nie był to selektywny „dobry porządek”. Sekwencjonowanie DNA wykazało, że w tych warunkach bakterie związane ze zdrowiem, takie jak Rothia, Gemella i Kingella, miały tendencję do spadku, podczas gdy kilka gatunków powiązanych z chorobą przyzębia — w tym Fusobacterium, Treponema i Eubacterium — utrzymywało się lub stawało się bardziej dominujących. Indeks oceniający, jak „chorobowo” wygląda społeczność bakteryjna, był wyższy przy zastosowaniu chlorheksydyny i amoksycyliny niż przy azotanie, co sugeruje, że te leki mogą przestawiać biofilm w kierunku bardziej szkodliwego, niezrównoważonego stanu, nawet jeśli tłumią ogólny wzrost.
Paliwo z zielonych warzyw i łagodniejszy antybiotyk
Azotan opowiedział inną historię. Gdy płytka była hodowana z samym azotanem, wzrosły bakterie wyspecjalizowane w przekształcaniu azotanu w użyteczne produkty, takie jak Neisseria i niektóre gatunki Aggregatibacter. Wskaźnik dysbiozy spadł w porównaniu z warunkami przy chlorheksydynie lub amoksycylinie, co wskazywało na zdrowszą społeczność. Metronidazol, w stężeniu podobnym do tego, które rzeczywiście dociera do kieszonek przyzębnych u pacjentów, samodzielnie nie obniżył znacząco wzrostu ani wykorzystania azotanu. Jednak w połączeniu z azotanem wydawał się przechylać równowagę w korzystną stronę: gatunki związane z chorobą, takie jak Fusobacterium i Treponema, zmniejszały się, podczas gdy wykorzystujące azotan Neisseria i Kingella wzrastały. To połączenie wyglądało na takie, które przycinało najgorszych sprawców bez niszczenia kluczowych funkcji.
Co to oznacza dla codziennej opieki
Dla osób z chorobami przyzębia te wyniki sugerują, że „najszybsze” nie zawsze znaczy „najlepsze” jeśli chodzi o środki przeciwbakteryjne. W tym modelu laboratoryjnym niskie dawki chlorheksydyny i amoksycyliny spowolniły wzrost bakterii, ale także osłabiły naturalną drogę opartą na azotanie, która wspiera zdrowie jamy ustnej i całego organizmu, i wiązały się z bardziej chorobowymi wzorcami mikrobiologicznymi. Azotan, zwłaszcza w połączeniu z metronidazolem, sprzyjał bakteriom powiązanym ze zdrowszymi dziąsłami i zachowywał metabolizm azotanu. Choć prawdziwe jamy ustne są bardziej złożone niż naczynia laboratoryjne, praca ta wspiera ideę łagodniejszych, przyjaznych dla mikrobiomu strategii — takich jak diety bogate w azotany i starannie dobrane antybiotyki — do leczenia chorób przyzębia bez osłabiania tych bakterii, które pomagają nam zachować zdrowie.
Cytowanie: Moran, S.P., Nadal-Ruiz, M., Mira, A. et al. Combined effects of nitrate and antimicrobial compounds on in vitro subgingival biofilms. Sci Rep 16, 6686 (2026). https://doi.org/10.1038/s41598-026-36588-x
Słowa kluczowe: choroby dziąseł, mikrobiom jamy ustnej, azotan, Płyn do płukania ust, antybiotyki