Clear Sky Science · pl
Diagnozowanie choroby Alzheimera z wysoką dokładnością za pomocą modelowania sieci Petri układów sygnałowych
Dlaczego wczesne wykrycie chorób mózgu jest ważne dla nas wszystkich
Choroba Alzheimera stopniowo niszczy pamięć i niezależność, często na długo zanim pojawią się wyraźne objawy. Obecne narzędzia diagnostyczne, takie jak skany mózgu czy testy poznawcze, mogą być kosztowne, trudno dostępne i mało czułe we wczesnych stadiach. W tym badaniu przedstawiono nowy sposób odczytywania „okablowania” molekularnego organizmu przy użyciu próbek krwi lub mózgu oraz matematycznego schematu zwanego siecią Petri. Cel jest prosty, lecz istotny: z bardzo wysoką dokładnością ustalić, czy wzorzec aktywności genów u danej osoby bardziej przypomina zdrową osobę, czy osobę z chorobą Alzheimera — najlepiej na tyle wcześnie, by móc zmienić przebieg choroby.
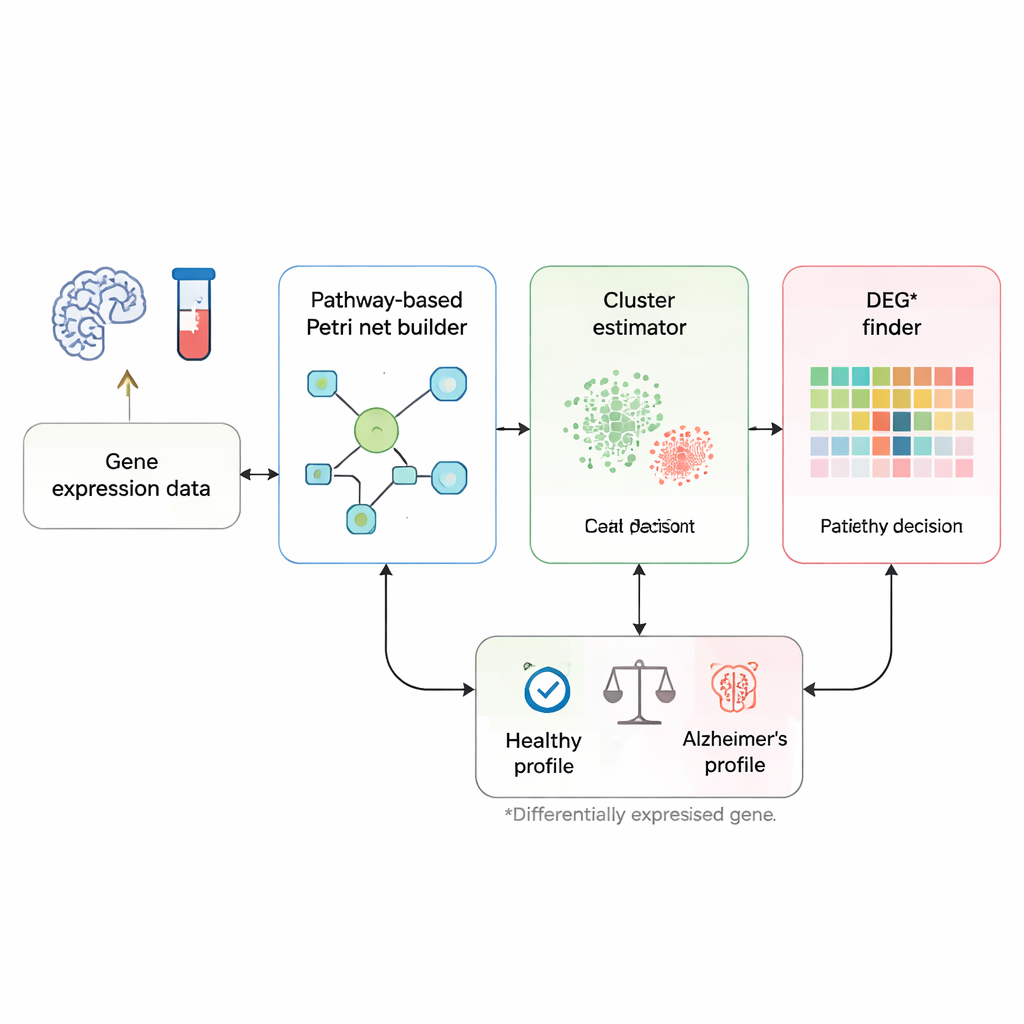
Odczytywanie choroby w „obwodach” sygnałowych organizmu
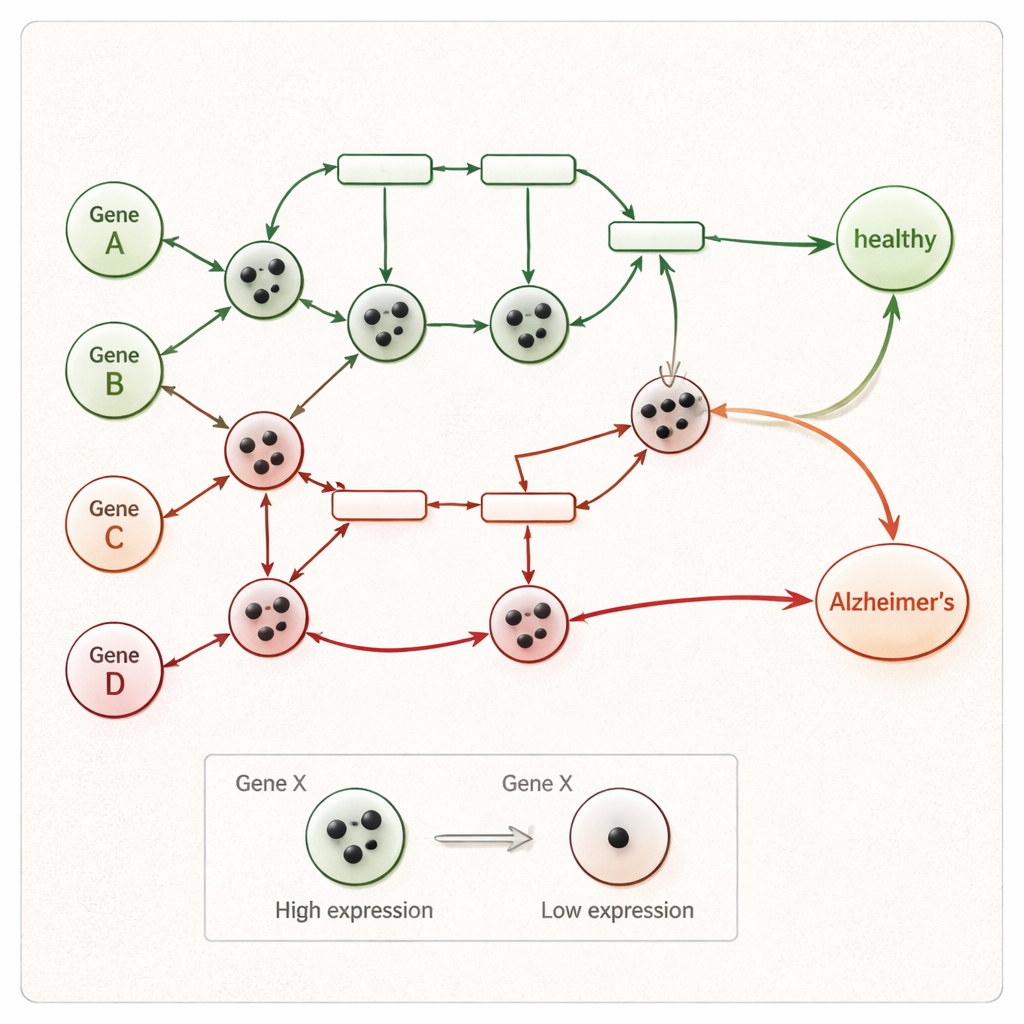
Zamiast traktować każdy gen jako izolowany marker, badacze skupiają się na tym, jak geny komunikują się ze sobą wzdłuż znanych biologicznych szlaków sygnałowych powiązanych z chorobą Alzheimera. Wyjściem jest skuratorowana mapa szlaku z bazy KEGG, która wymienia geny oraz relacje aktywujące lub hamujące między nimi. Ten szlak jest przekształcany w sieć Petri — rodzaj diagramu przepływu, w którym koła oznaczają geny, prostokąty interakcje, a małe tokeny sygnały poruszające się po sieci. Gdy token przemieszcza się od jednego końca szlaku do specjalnych „węzłów choroby”, reprezentuje to łańcuch zdarzeń genowych, które mogą prowadzić do śmierci komórek mózgowych i demencji.
Z próbki krwi do odpowiedzi tak lub nie
Metoda zaczyna się od profili ekspresji genów: pomiarów wskazujących, jak aktywne są tysiące genów w krwi lub tkance mózgowej danej osoby. Najpierw niestandardowy „estymator klastrów” porównuje nową próbkę z wcześniej oznakowanymi próbkami zdrowymi i chorymi, koncentrując się na genach już znanych z różnic między tymi grupami. Dla każdego takiego genu narzędzie sprawdza, które próbki treningowe mają najbardziej podobne poziomy ekspresji i wykorzystuje rodzaj głosowania sąsiedztwa, by nadać nowej próbce wstępną etykietę: prawdopodobnie zdrowa lub prawdopodobnie chora. Ten krok tworzy dwie robocze grupy, czyli klastry próbek: jedną reprezentującą typowe wzorce zdrowe i drugą reprezentującą typowe wzorce Alzheimera.
Wyszukiwanie najbardziej informatywnych genów dla każdej osoby
Następnie następuje bardziej spersonalizowany etap. Dla danej osoby metoda analizuje gen po genie, by zobaczyć, gdzie ich poziomy ekspresji rzeczywiście się wyróżniają. Dla każdego genu porównuje wartość tej osoby z zakresem obserwowanym zarówno w klastrze zdrowych, jak i w klastrze chorych, używając odpornych statystyk, które zmniejszają wpływ głośnych wartości odstających. Jeśli ekspresja genu wyraźnie mieści się w zakresie „chorobowym” i poza zakresem zdrowym, zostaje oznaczona jako DEG* — szczególnie informacyjny gen dla tej osoby. Geny DEG* otrzymują początkowe tokeny w sieci Petri, wskazując miejsca, gdzie nieprawidłowa aktywność pojawia się najwcześniej w obwodzie sygnałowym.
Puszczenie sieci w ruch aż do diagnozy
Gdy tokeny są umieszczone, sieć Petri działa krok po kroku. W każdym kroku każda interakcja, której geny wejściowe mają wystarczającą liczbę tokenów, „odpala”, przesuwając tokeny do genów położonych w dół ścieżki, przy jednoczesnym uwzględnieniu reguł aktywacji i inhibicji. Proces trwa, dopóki nie będą możliwe dalsze przesunięcia. Jeśli na końcu przynajmniej jeden token dotrze do końcowego węzła choroby w sieci — reprezentującego procesy takie jak obumieranie neuronów czy neurodegeneracja — próbka jest klasyfikowana jako Alzheimera; w przeciwnym razie oznacza się ją jako zdrową. Ponieważ każdy krok odpalenia jest rejestrowany, badacze mogą prześledzić jasną ścieżkę od nietypowej aktywności genów danej osoby aż do wyniku: zdrowy lub chorobowy, zamiast polegać na nieprzejrzystej statystycznej ocenie.
Jak dokładne jest to podejście w praktyce?
Zespół przetestował swój system na kilku dużych, publicznie dostępnych zestawach danych ekspresji genów zarówno z krwi, jak i tkanki mózgowej. W dwóch powszechnie używanych zestawach danych z krwi ich metoda prawidłowo odróżniała pacjentów z Alzheimerem od osób zdrowych w około 98–99% przypadków, znacznie przewyższając wcześniejsze podejścia uczenia maszynowego, które często osiągały jedynie 65–81% dokładności. Wykazali też silne wyniki w dodatkowych zestawach danych z mózgu i krwi, nawet gdy liczba próbek była niewielka. Co ważne, w przeciwieństwie do wielu konkurentów, ich metoda nie odrzucała hałaśliwych lub trudnych do interpretacji próbek; zamiast tego jej wewnętrzna konstrukcja radzi sobie ze zmiennością, utrzymując wszystkie dane w analizie.
Co to oznacza dla przyszłych testów na Alzheimera
Dla laika główne przesłanie jest takie, że badanie przekształca złożoną genetykę i diagramy ścieżek w jasny, etapowy proces decyzyjny, który może odczytywać wczesne sygnały choroby Alzheimera z prostej próbki, potencjalnie nawet tylko krwi. Modelując, jak nieprawidłowe geny współdziałają, a nie tylko jak zachowują się pojedynczo, ramy sieci Petri oferują zarówno wysoką dokładność diagnostyczną, jak i zrozumiałą „opowieść” o tym, jak choroba może przebiegać u konkretnej osoby. Choć praca ta pozostaje badawcza i nie jest jeszcze testem klinicznym, wskazuje drogę ku przyszłym narzędziom, które mogłyby wykrywać Alzheimera wcześniej, wspierać wybór terapii i ostatecznie zostać dostosowane do innych chorób mózgu oraz nowotworów, wykorzystując tę samą zasadę.
Cytowanie: Ebrahimian, H., Asadzadeh, F., Rahgozar, M. et al. Diagnosis of Alzheimer’s disease with high accuracy via Petri net modeling of signaling pathways. Sci Rep 16, 6457 (2026). https://doi.org/10.1038/s41598-026-36585-0
Słowa kluczowe: Diagnostyka Alzheimera, ekspresja genów, szlaki sygnałowe, modelowanie sieci Petri, biomarkery we krwi