Clear Sky Science · pl
Mikrośrodowisko guza w raku przełyku i jego związek z cechami klinicznymi oraz odpowiedzią na leczenie neoadiuwantowe
Dlaczego otoczenie guza ma znaczenie
Rak przełyku jest jednym z najbardziej śmiertelnych nowotworów na świecie, a nawet przy współczesnej chemioterapii i radioterapii wielu pacjentów nie reaguje tak dobrze, jak byśmy oczekiwali. W tym badaniu zadano pozornie proste, lecz istotne pytanie: co dzieje się w „sąsiedztwie” guza — w jego mikrośrodowisku — i czy jego skład może pomóc wyjaśnić, dlaczego u niektórych pacjentów leczenie działa, a u innych nie? Dokładna analiza komórek odpornościowych i powiązanych markerów przed i po terapii pozwala badaczom zacząć mapować, jak organizm i guz wchodzą w interakcje i jak ten ukryty dialog może wskazać drogę do bardziej spersonalizowanych terapii w przyszłości.
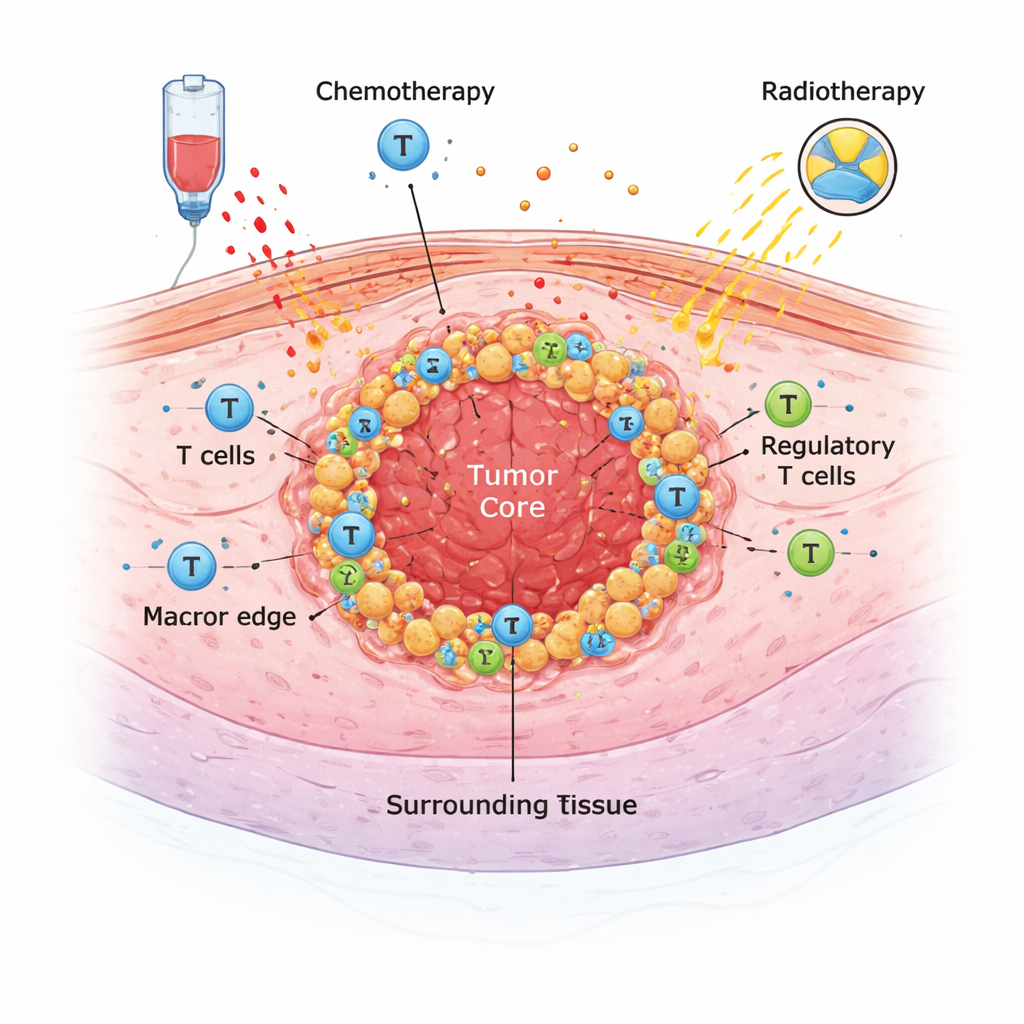
Ukryty ekosystem wokół guza
Guzy lity nie rozwijają się w izolacji. Funkcjonują w złożonym ekosystemie komórek odpornościowych, komórek wspierających i molekuł sygnałowych znanym jako mikrośrodowisko guza. W niniejszym badaniu lekarze i patolodzy z Lozanny zbadali próbki guzów od 68 pacjentów, którzy przeszli operację z powodu raka przełyku w latach 2009–2021. Większość otrzymała przedoperacyjne intensywne leczenie — chemioterapię, chemioradioterapię lub obie metody — w celu zmniejszenia guza. Zastosowano specjalne barwienia na preparatach tkankowych, policzono kilka kluczowych typów komórek odpornościowych (w tym ogólne komórki T, cytotoksyczne komórki T oraz różne rodzaje makrofagów) i zmierzono markery mogące przewidywać odpowiedź na immunoterapię, takie jak PD-L1 i HER2.
Kto był badany i co mierzono
Pacjenci w tej serii to głównie mężczyźni po sześćdziesiątce, a większość miała gruczolakoraka — typ raka przełyku często związany z przewlekłym refluksem żołądkowo-przełykowym i przełykiem Barretta. Mniejsza grupa miała raka płaskonabłonkowego, inny typ wywodzący się z płaskich komórek wyściełających przełyk. Badacze starannie powiązali obserwacje mikroskopowe z danymi klinicznymi takimi jak stopień zaawansowania choroby, palenie tytoniu, utrata masy ciała oraz rodzaj leczenia przedoperacyjnego. Monitorowali też, jak całkowicie każdy guz zareagował na terapię, stosując system ocen, który rozróżnia całkowite zniknięcie komórek nowotworowych od niewielkiej lub braku odpowiedzi.
Styl życia, typ guza i słabsza obecność odporności
Kilka codziennych i związanych z chorobą czynników okazało się powiązanych z niższą obecnością komórek odpornościowych wokół guza. Pacjenci aktywnie palący mieli ogólnie mniej makrofagów oraz mniej tzw. makrofagów typu M2, często kojarzonych ze wspieraniem guza i supresją odporności. Osoby z bardziej zaawansowanymi guzami, większą utratą masy ciała przed operacją lub z rakiem płaskonabłonkowym miały zwykle mniej komórek T i makrofagów naciekających guz. Natomiast guzy o wysokim wyniku PD-L1 — markerze często używanym do kwalifikacji do immunoterapii — były „gorętsze”, z większą liczbą komórek T i makrofagów; wcześniej jednak związano taki wzorzec z gorszymi wynikami, prawdopodobnie dlatego, że guz aktywnie wykorzystuje PD-L1 do wyciszania ataku immunologicznego.
Jak leczenie przekształca okolice guza
Leczenie neoadiuwantowe (przedoperacyjne) istotnie przebudowało mikrośrodowisko guza. Zarówno chemioterapia, jak i chemioradioterapia zwiększały liczbę makrofagów, w tym komórek o cechach M2, jednocześnie wyraźnie zmniejszając liczbę regulatorowych komórek T (Treg), grupy, która normalnie tłumi odpowiedzi immunologiczne. Ogólna liczba komórek T i cytotoksycznych komórek T zmieniała się mniej konsekwentnie. Co ciekawe, chemioradioterapia miała tendencję do obniżania poziomów PD-L1 w komórkach guza i otaczających komórkach, zmniejszając odsetek pacjentów z wysokimi wynikami PD-L1 po leczeniu. Sugeruje to, że standardowe leczenie może sprawić, iż guzy będą wyglądać mniej dogodnie do terapii blokujących PD-1/PD-L1, jeżeli oceniamy je jedynie na podstawie pojedynczego obrazu po chemioradioterapii.
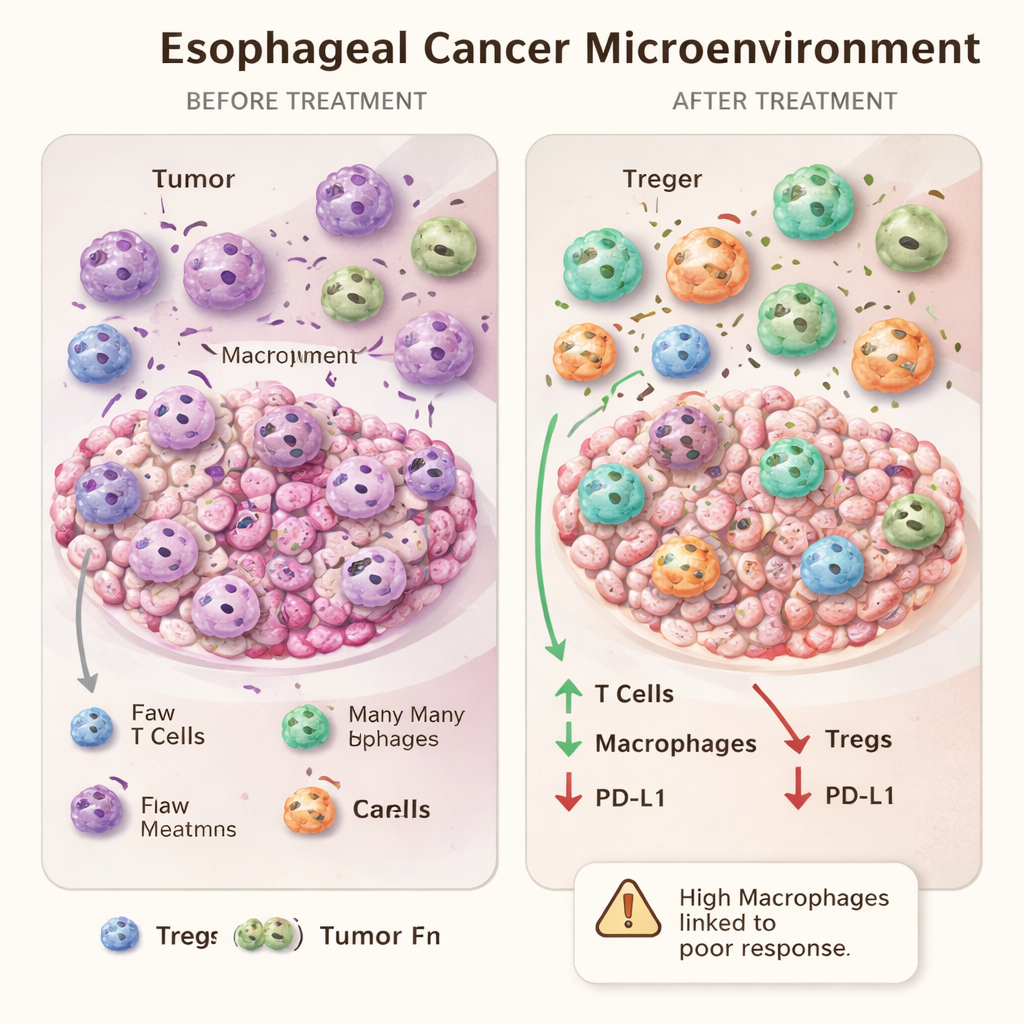
Kiedy większa liczba komórek odpornościowych może sygnalizować oporność
Jedno z najbardziej intrygujących odkryć wynikło z porównania skrajności odpowiedzi na leczenie. Pacjenci, u których guzy całkowicie zniknęły w obrazie mikroskopowym, nie różnili się na początku od słabo reagujących pacjentów pod względem komórek odpornościowych otaczających nowotwór. Jednak po leczeniu osoby o słabej odpowiedzi miały wyższe liczby makrofagów w obrębie guzów niż osoby z całkowitą odpowiedzią. Zamiast być prostym wskaźnikiem silnej odpowiedzi immunologicznej, obfitość makrofagów po terapii może oznaczać wyczerpaną lub spolaryzowaną odpowiedź, którą guz nauczył się wykorzystywać. Wspiera to pogląd, że niektóre makrofagi, szczególnie o fenotypie M2, mogą sprzyjać przetrwaniu guza i oporności na leczenie.
Co to oznacza dla przyszłej opieki
Dla pacjentów i klinicystów sedno sprawy jest takie, że biologia otaczająca guz przełyku — jego mikrośrodowisko — jest kształtowana przez palenie, typ guza, zaawansowanie choroby oraz przez same terapie. Standardowa chemia i chemioradioterapia nie tylko zmniejszają guzy; rekrutują i przebudowują także komórki odpornościowe w sposób, który może sprzyjać lub utrudniać długoterminową kontrolę choroby. Badanie sugeruje, że liczenie określonych komórek odpornościowych, zwłaszcza makrofagów, przed i po terapii mogłoby pewnego dnia pomóc zidentyfikować, kto prawdopodobnie będzie oporny na leczenie i kto może odnieść korzyść z dodatkowych leków ukierunkowanych na te komórki lub szlak PD-1/PD-L1. Choć potrzebne są dalsze, większe badania, praca ta przybliża nas do dopasowywania leczenia raka przełyku nie tylko do genetyki guza, lecz także do dynamicznego ekosystemu, który go otacza.
Cytowanie: Fasquelle, F., Teixeira Farinha, H., Sempoux, C. et al. The tumor microenvironment in esophageal cancer and its association with clinical features and neoadjuvant treatment response. Sci Rep 16, 5664 (2026). https://doi.org/10.1038/s41598-026-36537-8
Słowa kluczowe: rak przełyku, mikrośrodowisko guza, komórki odpornościowe, chemioterapia i radioterapia, immunoterapia