Clear Sky Science · pl
Modyfikacje m6A gospodarza kształtują mikrobiotę, która wywołuje komórkowo specyficzny ferroptoza jako przyczynową drogę do przewlekłych chorób układu oddechowego
Dlaczego twoje mikroby są ważne dla płuc
Przewlekłe problemy z oddychaniem, takie jak astma i przewlekła obturacyjna choroba płuc (POChP), zwykle przypisuje się paleniu, zanieczyszczeniom lub alergiom. To badanie wskazuje na innego, mniej oczywistego uczestnika: biliony mikroorganizmów żyjących w naszych jelitach i na skórze. Na podstawie danych genetycznych na dużą skalę autorzy pokazują, że niektóre mikroby mogą nie tylko towarzyszyć chorobom płuc, lecz także przyczyniać się do ich powstawania — działając przez subtelne chemiczne modyfikacje w naszych komórkach i formę uszkodzenia zależnego od żelaza. Zrozumienie tej ukrytej sieci może w przyszłości doprowadzić do nowych sposobów zapobiegania lub leczenia przewlekłych chorób układu oddechowego poprzez ukierunkowanie mikrobioty i powiązanych szlaków molekularnych ku zdrowszym stanom.
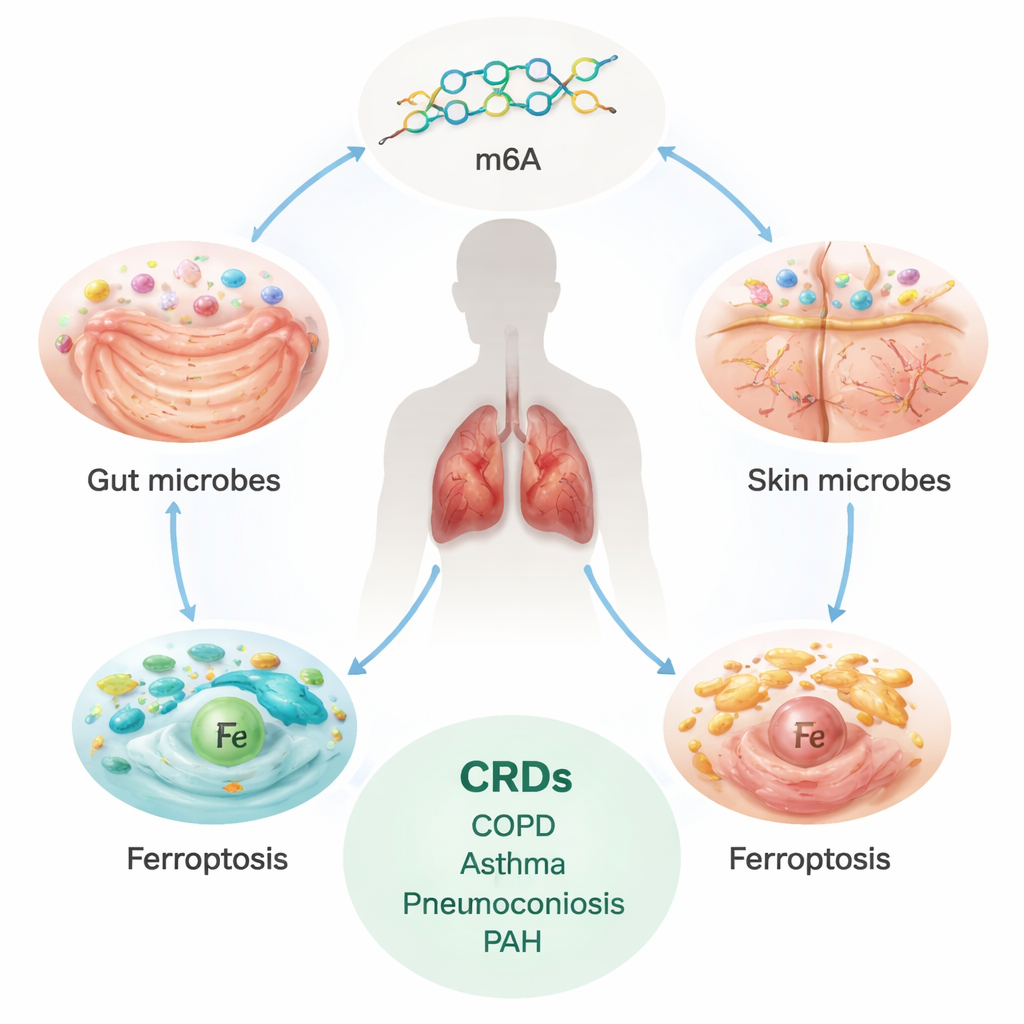
Ukryte obciążenie przewlekłymi chorobami płuc
Przewlekłe choroby układu oddechowego, w tym POChP, astma, choroby śródmiąższowe płuc (ILD), pylice oraz nadciśnienie płucne tętnicze (PAH), dotykają setek milionów ludzi na całym świecie i powodują miliony zgonów rocznie. Choroby te często postępują wolno, lecz nieubłaganie, prowadząc do bliznowacenia lub przebudowy płuc i naczyń krwionośnych, co skutkuje dusznością. Obecne leczenie głównie łagodzi objawy; nie zatrzymuje w pełni ani nie odwraca podstawowych uszkodzeń. To skłoniło naukowców do poszukiwania głębszych, podstawowych przyczyn, zwłaszcza takich, które można modyfikować zanim rozwinie się ciężka choroba.
Mikrobialni sąsiedzi w jelitach i na skórze
Wiemy już, że jelita i skóra są siedliskiem złożonych społeczności mikrobiologicznych, które kształtują układ odpornościowy, wpływają na metabolizm i utrzymują bariery obronne. Czy jednak te mikroby faktycznie napędzają choroby płuc, czy po prostu zmieniają się, gdy ludzie chorują? Aby rozróżnić przyczynę od skutku, badacze zastosowali metodę zwaną randomizacją Mendla, która wykorzystuje naturalne różnice genetyczne między ludźmi jako rodzaj dożywotniego „doświadczenia”. Połączyli dane genetyczne dotyczące setek typów mikroorganizmów jelitowych i skórnych z danymi o pięciu głównych przewlekłych chorobach płuc z dużych badań europejskich, sprawdzając, czy dziedziczne tendencje do wyższych lub niższych poziomów konkretnych mikroorganizmów wiążą się z ryzykiem każdej z chorób.
Mikroby, które pomagają lub szkodzą płucom
Analiza wykryła dziesiątki mikroorganizmów jelitowych, które albo zwiększały, albo zmniejszały ryzyko poszczególnych chorób oddechowych, często w wzorcach specyficznych dla danej choroby. Na przykład niektóre bakterie jelitowe wydawały się chronić przed POChP, astmą lub PAH, podczas gdy inne podnosiły prawdopodobieństwo ILD lub POChP. Mikroby skórne wykazywały skromniejsze, lecz nadal wykrywalne powiązania — niektóre gatunki związane były z wyższym ryzykiem, inne z niższym, w zależności od schorzenia. Zespół odwrócił też kierunek analizy, znajdując, że genetyczne ryzyko POChP, astmy i innych chorób płuc przewidywało zmiany w mikrobiocie jelitowej i skórnej. Ten dwukierunkowy przepływ sugeruje sprzężenie zwrotne: mikroby mogą kształtować choroby płuc, a choroby płuc mogą przekształcać nasze ekosystemy mikrobiologiczne.
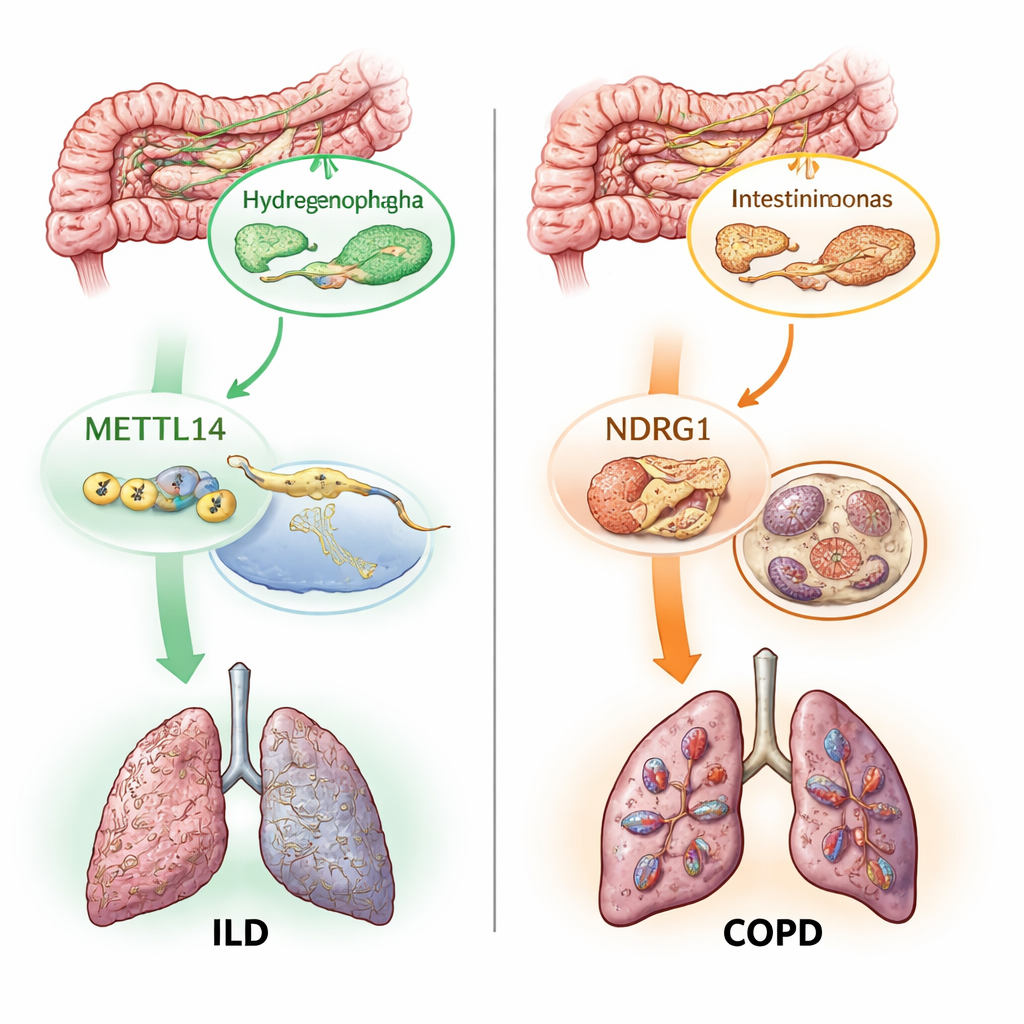
Dwa molekularne przełączniki: markery RNA i żelazozależna śmierć komórki
Później autorzy zbadali, jak te mikroskopijne partnerstwa mogą wpływać na tkanki płuc. Skupili się na dwóch procesach molekularnych już podejrzewanych o udział w uszkodzeniu płuc. Pierwszy, zwany modyfikacją m6A, to drobna chemiczna etykieta dodawana do RNA, która reguluje, jak geny są włączane i wyłączane. Drugi, ferroptoza, to forma śmierci komórki zależna od żelaza, napędzana niekontrolowaną utleniającą degradacją tłuszczów w błonach komórkowych. Korzystając z genetycznych przybliżeń dla 19 genów związanych z m6A i setek genów związanych z ferroptozą, badacze sprawdzili, czy zmiany w tych szlakach mają przyczynowy związek z chorobami płuc. Stwierdzili, że jeden gen „piszący” m6A, METTL14, wiązał się z niższym ryzykiem ILD, a kilka genów ferroptozy, w tym NDRG1, wiązało się z wyższym ryzykiem POChP, ILD i astmy.
Łączenie punktów: od mikrobioty do komórek do choroby
Najbardziej nowatorską częścią pracy było wyśledzenie, jak te elementy łączą się w łańcuchy przyczynowo-skutkowe. Analizy mediacyjne statystycznie zasugerowały, że pewna ochronna rola METTL14 w ILD przebiega częściowo przez zmiany, jakie wywołuje w konkretnym mikrobie jelitowym o nazwie Hydrogenophaga. W innym szlaku konkretny bakterium jelitowe, Intestinimonas massiliensis, wydawało się wpływać na ryzyko POChP częściowo przez aktywację NDRG1 i programu śmierci ferroptozy. Zespół następnie sprawdził dane z ludzkich tkanek płucnych i potwierdził, że zarówno METTL14, jak i NDRG1 są wyrażane inaczej w próbkach chorych w porównaniu ze zdrowymi. Wreszcie, korzystając z map genetycznych pojedynczych komórek układu odpornościowego, zlokalizowali szkodliwy wpływ NDRG1 na POChP do jednej podgrupy komórek odpornościowych — typu monocytów — co sugeruje, że przyszłe leki celujące w ten gen mogą wymagać działania zależnego od konkretnego typu komórek.
Co to oznacza dla przyszłych terapii
Dla osób niebędących specjalistami główne przesłanie jest takie, że zdrowie płuc nie zależy wyłącznie od tego, czym oddychamy, lecz także od mikrobiomów żyjących w nas i na nas oraz od molekularnych przełączników, które za ich pośrednictwem przełączane są wewnątrz naszych komórek. To badanie nie może doświadczalnie udowodnić każdego kroku i jest ograniczone głównie do osób pochodzenia europejskiego, ale dostarcza mocnych genetycznych wskazówek, że mikroby jelitowe, markery RNA takie jak m6A oraz żelazozależna śmierć komórkowa tworzą powiązaną ścieżkę prowadzącą do przewlekłego uszkodzenia płuc. W dłuższej perspektywie ten kierunek badań mógłby zainspirować nowe strategie łączące terapie oparte na mikrobiomie z lekami celującymi METTL14, NDRG1 lub ferroptozę — dążącymi nie tylko do łagodzenia objawów, lecz do przerwania obwodów biologicznych, które powodują postęp chorób układu oddechowego.
Cytowanie: Zhang, J., Liu, X., Liu, X. et al. Host m6A modifications shape microbiota that drives cell specific ferroptosis as a causal pathway to chronic respiratory diseases. Sci Rep 16, 5809 (2026). https://doi.org/10.1038/s41598-026-36513-2
Słowa kluczowe: mikrobiom jelitowy, przewlekła choroba płuc, astma i POChP, epigenetyka RNA, szlaki śmierci komórkowej