Clear Sky Science · pl
Powiązanie statusu mutacji RAS z wynikami klinicznymi u pacjentów z przerzutowym rakiem jelita grubego leczonych trifluridyną/tipiracilem lub regorafenibem
Dlaczego to badanie ma znaczenie dla pacjentów i ich rodzin
Przerzutowy rak jelita grubego — rak okrężnicy lub odbytnicy, który się rozprzestrzenił — jest jedną z głównych przyczyn zgonów z powodu nowotworów na świecie. Gdy standardowe leki przestają działać, pacjenci i lekarze stoją przed trudnymi decyzjami, co wypróbować dalej. To badanie stawia bardzo praktyczne pytanie: czy proste testy genetyczne guza mogą pomóc dopasować pacjentów do dwóch szeroko stosowanych leków ostatniej linii, trifluridyny/tipiracylu i regorafenibu, tak aby ludzie żyli dłużej i mieli lepszą jakość życia?
Patrząc na geny, by prowadzić trudne decyzje terapeutyczne
Współczesna opieka onkologiczna często zaczyna się od badania DNA guza. Jedna z kluczowych rodzin genów, nazywana RAS, pomaga kontrolować, jak komórki rosną i dzielą się. Zmiany, czyli mutacje w tych genach, mogą sprawić, że komórki nowotworowe będą niekontrolowanie rosnąć i oporne na pewne leki. Badacze przejrzeli dokumentację medyczną 263 dorosłych pacjentów z przerzutowym rakiem jelita grubego leczonych w tajwańskim ośrodku onkologicznym w latach 2018–2023. Wszyscy przeszli już standardową chemioterapię i terapie ukierunkowane, po czym otrzymali albo trifluridynę/tipiracyl samodzielnie, trifluridynę/tipiracyl z dodatkowym lekiem ukierunkowanym, albo regorafenib. Przed rozpoczęciem terapii u każdego pacjenta zbadano geny RAS i przypisano go do jednej z trzech grup: RAS prawidłowy (RAS wild‑type), powszechna mutacja w jednym miejscu genu KRAS (KRAS G12) lub inne, rzadsze mutacje RAS.
Trzy drogi leczenia w warunkach rzeczywistych
Trifluridyna/tipiracyl to doustna chemioterapia, a regorafenib to lek doustny blokujący kilka sygnałów związanych z wzrostem komórek nowotworowych i naczyń krwionośnych. Część pacjentów w tym badaniu otrzymała trifluridynę/tipiracyl samodzielnie, inni przyjmowali ją w połączeniu z dodatkowym lekiem ukierunkowanym blokującym naczynia guza lub sygnały wzrostowe. Ponieważ był to przegląd danych z praktyki klinicznej, a nie randomizowane badanie, lekarze wybierali terapię na podstawie wcześniejszych działań niepożądanych, rozległości guza i ogólnego stanu pacjenta. Badacze śledzili następnie, jak długo pacjenci żyli bez progresji choroby (czas wolny od progresji) i jak długo przeżywali ogółem, a także jak często guzy się zmniejszały lub przynajmniej przestawały rosnąć.
Różnice genetyczne kształtują, który lek działa lepiej
W całej grupie kombinacja trifluridyny/tipiracylu z lekiem ukierunkowanym wyraźnie wypadała najlepiej. Pacjenci na tej kombinacji zwykle mieli około pięciu miesięcy do progresji choroby i mediana przeżycia ogólnego wynosiła nieco ponad 15 miesięcy od rozpoczęcia leczenia — dłużej niż u osób otrzymujących trifluridynę/tipiracył samodzielnie lub regorafenib. Guzy częściej ulegały zmniejszeniu lub stabilizacji przy terapii skojarzonej. Gdy badacze przyjrzeli się dokładniej grupom według statusu RAS, pojawiły się istotne wzorce. U pacjentów z guzami o prawidłowym RAS lub z jedną z rzadszych mutacji RAS trifluridyna/tipiracyl nadal przewyższała regorafenib pod względem przeżycia. Jednak u pacjentów z powszechną mutacją KRAS G12 regorafenib zapewniał lepsze przeżycie niż trifluridyna/tipiracyl samodzielnie, choć terapia skojarzona nadal dawała najlepsze wyniki.
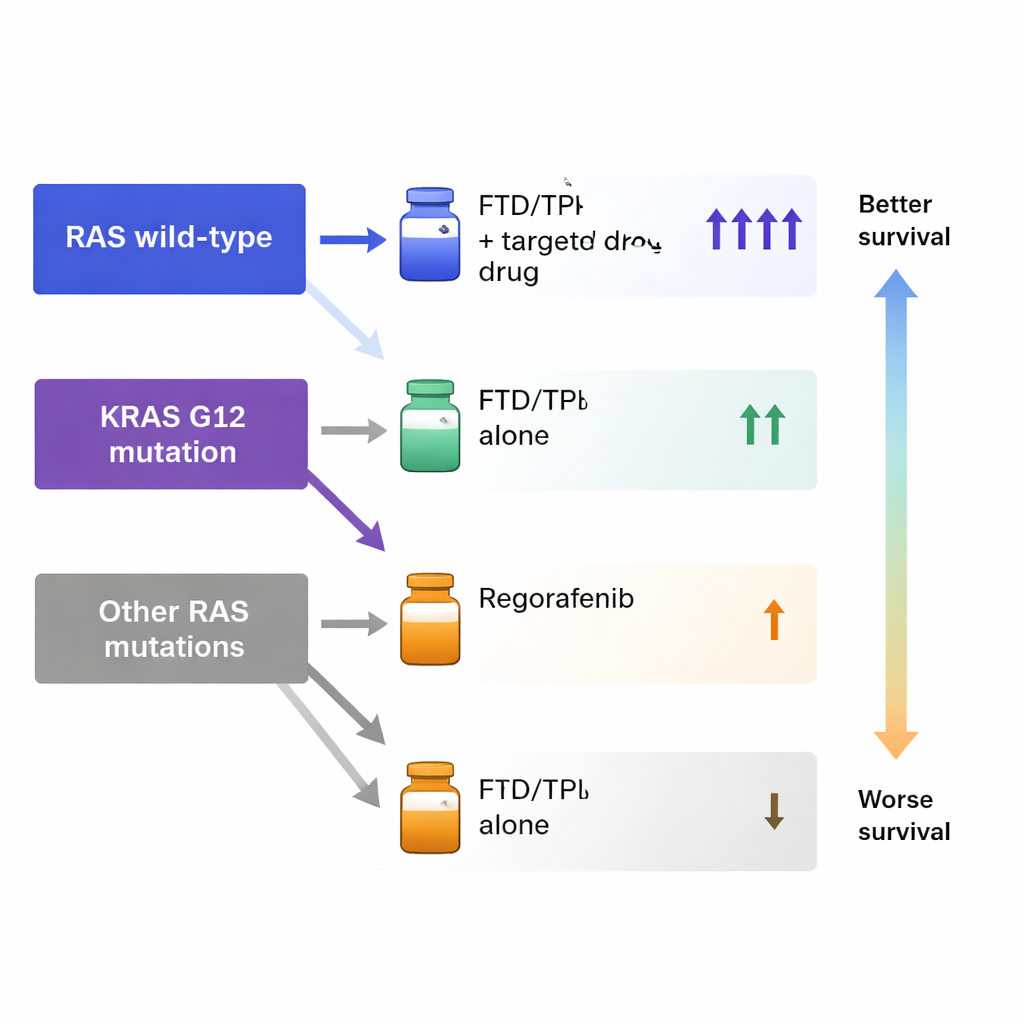
Co to znaczy dla precyzyjnej opieki onkologicznej
Wyniki sugerują, że stosunkowo prosty test genetyczny — rutynowo wykonywany u wielu chorych na raka jelita grubego — może pomóc w wyborze między dwiema trudnymi opcjami leczenia w zaawansowanym stadium choroby. Zamiast traktować trifluridynę/tipiracyl i regorafenib jako zamienne po niepowodzeniu terapii standardowej, lekarze mogliby skłaniać się ku trifluridynie/tipiracylowi, zwłaszcza w połączeniu z lekiem ukierunkowanym, dla większości pacjentów. Dla podgrupy z mutacją KRAS G12 regorafenib może być lepszą opcją jako pojedynczy lek, jeśli terapia skojarzona nie jest możliwa. Badanie sugeruje także, że inne cechy kliniczne, takie jak pierwotne stadium choroby i pewne markery naprawy DNA, mogą dodatkowo doprecyzować te decyzje.
Wniosek dla osób niebędących specjalistami
Dla osób żyjących z zaawansowanym rakiem jelita grubego to badanie przynosi ostrożnie optymistyczne wieści: genetyczny odcisk palca guza, szczególnie zmiany w genach RAS, może pomóc wskazać lek najprawdopodobniej kupujący więcej czasu. W tej analizie dodanie leku ukierunkowanego do trifluridyny/tipiracylu wiązało się z najdłuższym przeżyciem u prawie wszystkich pacjentów, niezależnie od statusu RAS. Wśród chorych z konkretną mutacją KRAS G12 regorafenib wydawał się korzystniejszym wyborem niż trifluridyna/tipiracyl samodzielnie. Ponieważ było to retrospektywne badanie z jednego ośrodka, jego wyniki wymagają potwierdzenia w większych, randomizowanych badaniach. Mimo to daje praktyczną, opartą na genach mapę postępowania, którą lekarze mogą rozważyć dziś przy dostosowywaniu ostatnich linii leczenia przerzutowego raka jelita grubego.
Cytowanie: Hsieh, MC., Rau, KM., Liu, KW. et al. Association of RAS mutational status with clinical outcomes in metastatic colorectal cancer treated with trifluridine/tipiracil or regorafenib. Sci Rep 16, 5294 (2026). https://doi.org/10.1038/s41598-026-36509-y
Słowa kluczowe: przerzutowy rak jelita grubego, mutacja RAS, KRAS G12, trifluridyna tipiracyl, regorafenib