Clear Sky Science · pl
Identyfikacja kluczowych genów bakteryjnych i celów terapeutycznych u pacjentów z nadciśnieniem i cukrzycą typu 2 poprzez analizę bioinformatyczną
Dlaczego jelito ma znaczenie dla ciśnienia krwi i poziomu cukru
Wysokie ciśnienie krwi i cukrzyca typu 2 często występują razem, zwiększając ryzyko zawałów serca, udarów i chorób nerek. Lekarze tradycyjnie traktowali te schorzenia osobno, koncentrując się na lekach działających na serce, naczynia krwionośne lub insulinę. Niniejsze badanie stawia inne pytanie: czy drobne mikroby żyjące w naszych jelitach — i geny, które ze sobą niosą — mogą jednocześnie napędzać oba problemy i czy mogą ujawnić nowe możliwości leczenia?
Ukryty świat wewnątrz jelita
Naukowcy przeanalizowali próbki kału od 124 dorosłych, porównując 29 osób z nadciśnieniem i cukrzycą typu 2 z 95 zdrowymi ochotnikami. Przy użyciu sekwencjonowania markerów bakteryjnych zbudowali szczegółowy obraz obecnych mikroorganizmów i zróżnicowania każdej społeczności jelitowej. Osoby z oboma schorzeniami miały bogatsze, bardziej równomiernie rozłożone społeczności bakteryjne, które grupowały się oddzielnie od tych u zdrowych osób, co oznacza, że ich ekosystemy jelitowe były wyraźnie zrestrukturyzowane, a nie tylko nieznacznie zaburzone.
Mikrobiologiczny przechył od pomocnych do szkodliwych
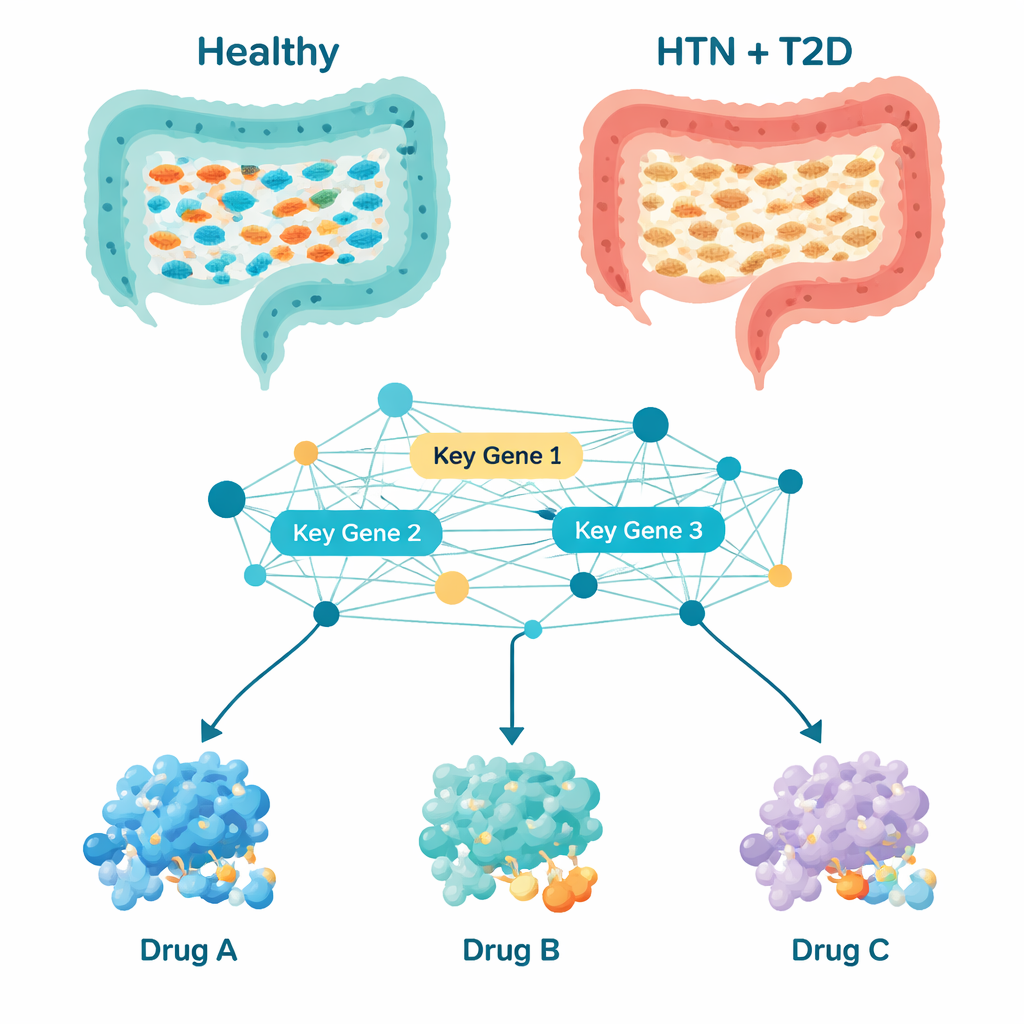
Gdy zespół przyjrzał się, które typy bakterii były najbardziej liczne, ujawnił się wyraźny wzorzec. U zdrowych osób powszechne były bakterie wspomagające produkcję krótkołańcuchowych kwasów tłuszczowych — związków wspierających zdrowie wyściółki jelita oraz kontrolę zapalenia i metabolizmu. Należały do nich grupy takie jak Bacteroides, Prevotella, Roseburia i Akkermansia. U osób z nadciśnieniem i cukrzycą wiele z tych korzystnych mikroorganizmów było uszczuplonych. Jednocześnie częściej występowały bakterie powiązane w innych badaniach z zapaleniem i zaburzeniami metabolicznymi, takie jak Megasphaera, Lactobacillus, Streptococcus i Veillonella. Dziewiętnaście grup bakteryjnych było konsekwentnie różne między pacjentami a zdrowymi kontrolami, co sugeruje skoordynowany przesunięcie w kierunku środowiska jelitowego sprzyjającego przewlekłemu stanowi zapalnemu i obciążeniu metabolicznemu.
Od mikroorganizmów do „pokręteł” molekularnych
Sam rachunek mikroorganizmów nie wyjaśnia, jak wpływają one na organizm, dlatego naukowcy użyli narzędzi obliczeniowych, aby wywnioskować, co bakterie jelitowe prawdopodobnie wykonują. Przewidzieli, które szlaki metaboliczne — łańcuchy reakcji chemicznych — były bardziej lub mniej aktywne u pacjentów. Spośród ponad tysiąca ścieżek 195 wyróżniało się zmianami. Wiele z nich dotyczyło produkcji białek przez bakterie, przetwarzania energii oraz metabolizmu bloków budulcowych, takich jak nukleotydy i aminokwasy. Budując sieć interakcji odpowiadających białek bakteryjnych, zespół zidentyfikował dziesięć „genów-hubów” znajdujących się w kluczowych punktach tej sieci. Geny te, o nazwach takich jak gltB, gyrB, fusA i mdh, pełnią rolę pokręteł regulujących podstawowe funkcje bakteryjne, takie jak produkcja energii, kopiowanie DNA, synteza białek oraz metabolizm kwasów tłuszczowych i nukleotydów. Ponieważ te procesy są ściśle powiązane z zapaleniem, zdrowiem naczyń i kontrolą glukozy, zmiany w tych genach bakteryjnych mogą oddziaływać na ciśnienie krwi i poziom cukru.
Poszukiwanie nowych zastosowań dla istniejących leków
Posiadając listę tych bakteryjnych genów-kontrolerów, badacze przystąpili do komputerowego przesiewu leków. Zgromadzili 189 substancji już badanych w kontekście nadciśnienia, cukrzycy typu 2 lub problemów metabolicznych i wykorzystali dokowanie molekularne — rodzaj trójwymiarowej układanki — aby sprawdzić, które związki mogą najsilniej wiązać się z białkami kodowanymi przez dziesięć kluczowych genów bakteryjnych. Wyróżniły się trzy kandydatury: naringina i neohesperydyna, związki roślinne występujące w owocach cytrusowych, oraz bromokryptyna, lek już zatwierdzony w terapii cukrzycy typu 2. Szczegółowe symulacje na skali 100 miliardowych części sekundy sugerowały, że kompleksy z udziałem neohesperydyny i bromokryptyny są szczególnie stabilne, co oznacza, że leki te mogłyby wiarygodnie wiązać i wpływać na docelowe białka bakteryjne in vivo. Dalsze oceny właściwości zgodnych z farmakologią oraz przewidywań dotyczących wchłaniania, rozmieszczenia i eliminacji wskazały bromokryptynę jako najbardziej praktycznego kandydata w krótszej perspektywie, choć wszystkie trzy wymagają uważnych badań nad bezpieczeństwem i dawkowaniem.
Co to oznacza dla przyszłej opieki
Mówiąc prostym językiem, praca ta odwzorowuje trzyetapowy łańcuch: osoby z jednoczesnym nadciśnieniem i cukrzycą typu 2 mają charakterystyczny mikrobiom jelitowy; ten mikrobiom nosi zestaw genów bakteryjnych, które mogą kierować metabolizmem i naczyniami w niekorzystnym kierunku; i niektóre istniejące leki wydają się być zdolne do celowania w te geny bakteryjne. Badanie nie udowadnia, że zmiana tych mikrobów lub ich genów wyleczy chorobę, ani nie testuje żadnych terapii na pacjentach. Jednak kładzie fundament pod diagnostykę i terapie oparte na mikrobiomie, w których lekarze pewnego dnia mogliby modyfikować bakterie jelitowe lub stosować dopasowane leki, aby zmniejszyć wspólne obciążenie wynikające z nadciśnienia i cukrzycy.
Cytowanie: Rahat, M.T.I., Sumi, M.S.A., Nurejannath, M. et al. Identification of bacterial key genes and therapeutic targets in hypertensive patients with type 2 diabetes through bioinformatics analysis. Sci Rep 16, 6431 (2026). https://doi.org/10.1038/s41598-026-36467-5
Słowa kluczowe: mikrobiom jelitowy, nadciśnienie, cukrzyca typu 2, geny bakteryjne, repurposing leków