Clear Sky Science · pl
Modelowanie sieci neuronowej i optymalizacja elektrochemicznego biosensora do wykrywania raka piersi opartego na miR-155 w osoczu
Dlaczego ma to znaczenie dla wczesnych badań przesiewowych w kierunku raka
Lekarze i naukowcy poszukują prostych badań krwi, które potrafią wykryć raka na długo przed pojawieniem się objawów. Obiecującym wskaźnikiem we krwi jest niewielki fragment genetyczny zwany miR-155, powiązany z rakiem piersi oraz z szeregiem schorzeń immunologicznych i zapalnych. Zbudowanie sensora, który niezawodnie zmierzy tak słaby sygnał, jest trudne i zwykle wymaga miesięcy metod prób i błędów w laboratorium. To badanie pokazuje, jak połączenie inteligentnych modeli komputerowych z elektrochemicznym biosensorem może przyspieszyć, obniżyć koszty i zwiększyć skuteczność tego procesu, przybliżając praktyczne testy wczesnego wykrywania do zastosowań klinicznych.
Jak kropla krwi staje się sygnałem ostrzegawczym
Praca koncentruje się na elektrochemicznym biosensorze, który mierzy poziomy miR-155 w osoczu, ciekłej części krwi. Serce urządzenia stanowi maleńka złota elektroda, której powierzchnia jest starannie przygotowywana w kilku etapach. Najpierw do metalu przytwierdzane są krótkie nici DNA zaprojektowane tak, by rozpoznawać miR-155. Następnie drobna cząsteczka wypełnia luki, by zapobiec przyczepianiu się obcych substancji. Gdy dodany zostanie próbka pacjenta, obecne w niej miR-155 przyłącza się do nici DNA, a barwnik przypominający farbę, zwany Oracet Blue, wnika w te sparowane struktury. Na koniec skan elektryczny mierzy przenoszony ładunek, generując prąd, którego wielkość odzwierciedla ilość miR-155 w próbce. 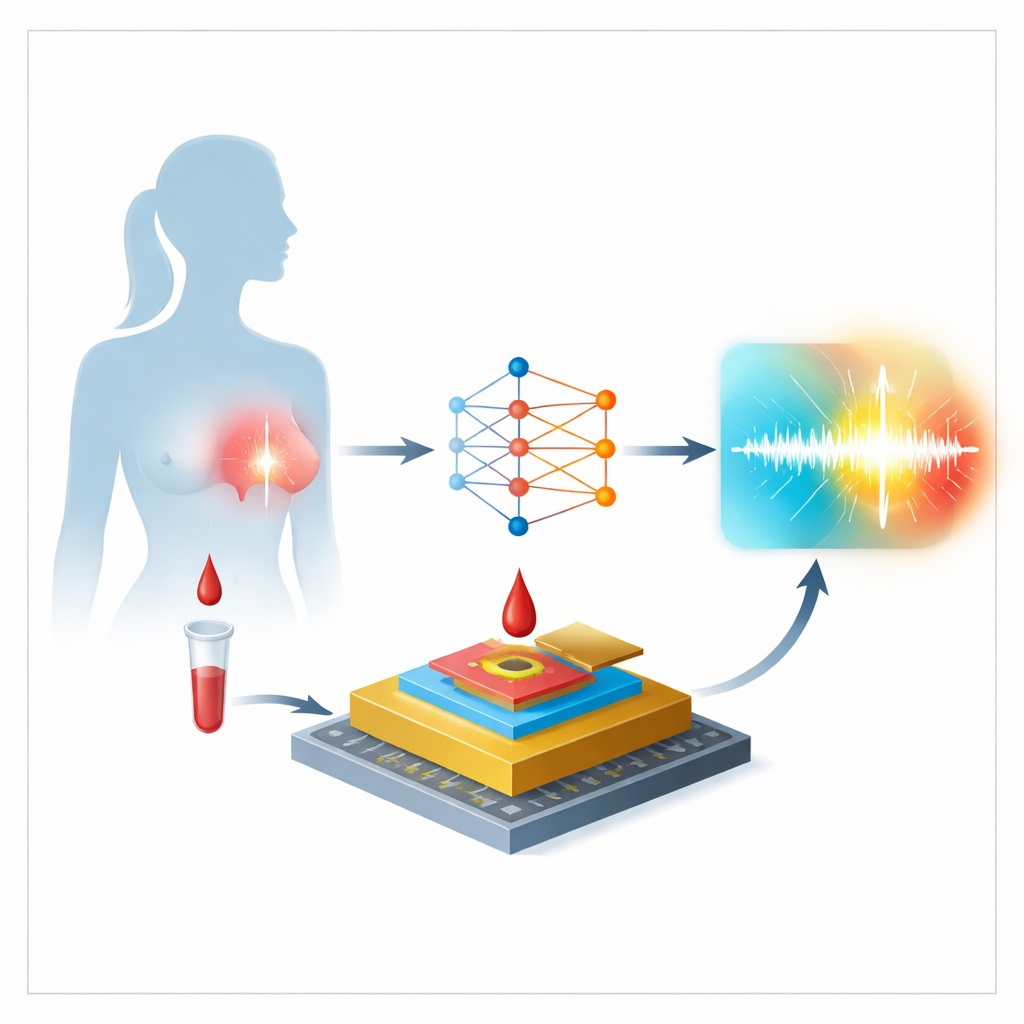
Dlaczego tradycyjne strojenie jest powolne i marnotrawne
Chociaż podstawowa idea sensoryczna jest prosta, wydajność biosensora w dużym stopniu zależy od sposobu jego wykonania. Sześć kluczowych etapów ma znaczenie: stężenie sondy DNA, czas, w którym ma ona szansę się związać, długość inkubacji z cząsteczką blokującą, czas przeznaczony na związanie docelowego miRNA oraz zarówno ilość, jak i czas oczekiwania dla Oracet Blue. W wcześniejszych pracach badacze zmieniali po jednym lub dwóch z tych parametrów, przeprowadzali nowe eksperymenty i powoli dążyli do lepszej konfiguracji. Podejście to zużywa drogie materiały, wymaga dużych nakładów czasu badacza i może pominąć najlepsze kombinacje, zwłaszcza gdy zachowanie układu jest silnie nieliniowe — niewielkie zmiany czasu lub stężenia mogą nagle podwoić lub zmniejszyć sygnał o połowę.
Pozwolić komputerom nauczyć się najlepszej receptury
Aby przełamać to wąskie gardło, autorzy sięgnęli po uczenie maszynowe, używając dwóch stylów modelowania: sztucznych sieci neuronowych (ANN) i adaptacyjnego systemu neuro-rozmytego (ANFIS). Skompilowali dane z 51 różnych sposobów wytwarzania tego samego sensora miR-155, z których każdy definiowany był unikalną kombinacją sześciu kluczowych kroków, i zapisali uzyskany prąd elektryczny. ANN nauczyła się mapować wybory produkcyjne bezpośrednio na odpowiedź sensora, wykorzystując zwartą sieć z jedną warstwą ukrytą i 13 jednostkami wewnętrznymi. Podejście ANFIS łączyło reguły rozmyte (takie jak „niskie” lub „wysokie” poziomy) z treningiem w stylu sieci neuronowej i używało również zabiegu statystycznego zmniejszającego nakładanie się wejść. Po starannym treningu i testach ANN okazała się bardziej dokładna i łatwiejsza w obsłudze, lepiej chwytając złożone interakcje między krokami niż bardziej regułowy model rozmyty.
Przeszukiwanie przestrzeni projektowej za pomocą ewolucji cyfrowej
Gdy ANN potrafiła wiernie naśladować biosensor, zespół połączył ją z algorytmem genetycznym, metodą poszukiwań inspirowaną ewolucją. Ten cyfrowy optymalizator rozpoczynał od wielu losowych receptur budowy sensora i wielokrotnie je „krzyżował” i mutował, zachowując te, które według ANN miały dać silniejsze sygnały. W tym wirtualnym środowisku nie było potrzeby prowadzenia nowych prac laboratoryjnych: komputer mógł eksplorować niezliczone możliwości in silico. Zwycięska receptura była zaskakująca. W porównaniu z najlepszymi warunkami, które badacze faktycznie testowali przy stole laboratoryjnym, zoptymalizowana kombinacja użyła ogólnie mniej sondy DNA i mniej Oracet Blue, skróciła kilka etapów inkubacji, a mimo to przewidywano, że ponad dwukrotnie zwiększy wyjściowy prąd sensora — z 98 do 223 nanoamperów — wzmacniając sygnał i ułatwiając jego odróżnienie od szumu tła. 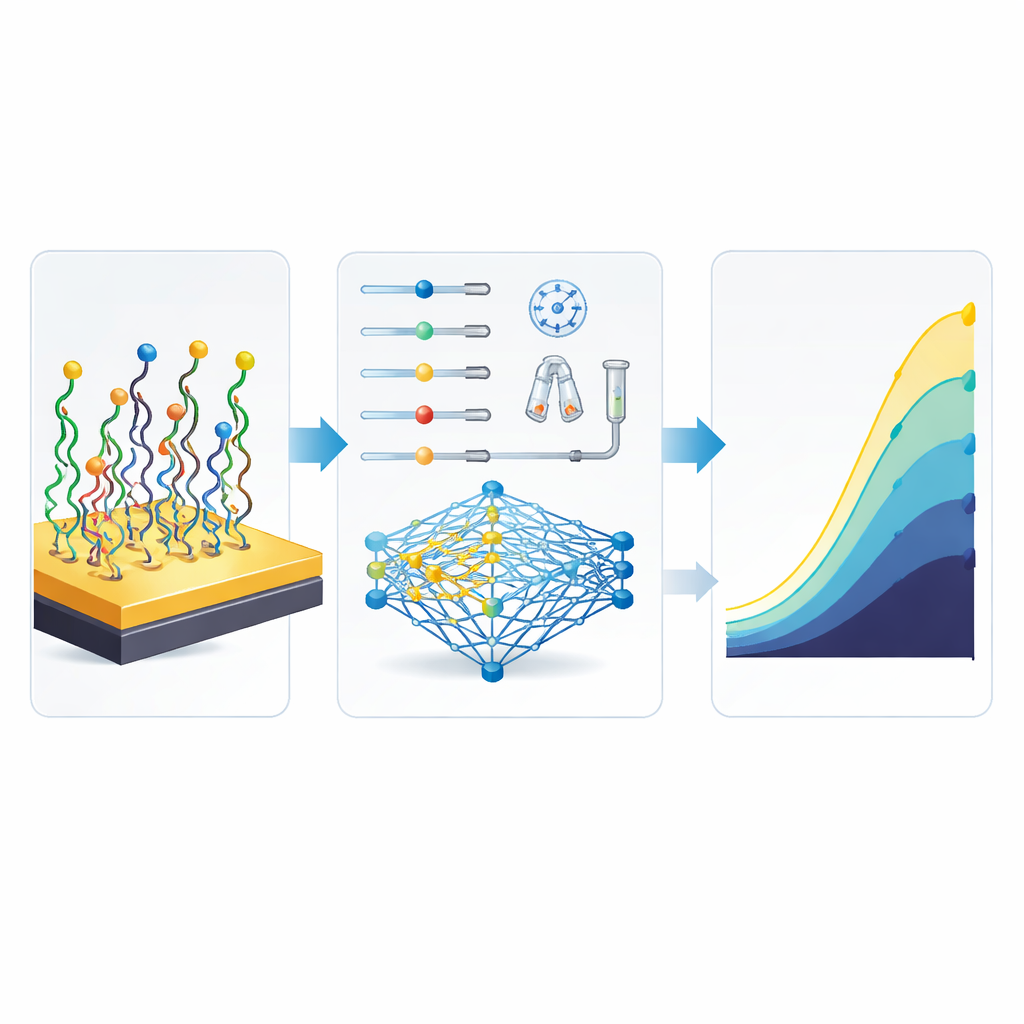
Co to oznacza dla przyszłych testów krwi
Dla osoby niebędącej specjalistą kluczowym przesłaniem jest to, że autorzy zmienili strojenie biosensorów z procesu opartego na domysłach w proces prowadzony danymi. Pozwalając sieci neuronowej nauczyć się, jak kroki produkcyjne wpływają na końcowy sygnał elektryczny, a następnie używając algorytmu ewolucyjnego do poszukiwania najlepszej receptury, znaleźli warunki, które powinny dać jaśniejszy, bardziej niezawodny odczyt miR-155 przy mniejszym marnowaniu czasu i materiałów. Chociaż zoptymalizowane ustawienia nadal wymagają pełnego potwierdzenia eksperymentalnego, a badanie skupia się na jednym typie markera raka piersi, ta sama strategia może zostać zastosowana do wielu innych biosensorów. W dłuższej perspektywie tego rodzaju inteligentne projektowanie mogłoby pomóc wprowadzić szybkie, tanie testy krwi do rutynowego użytku klinicznego w celu wczesnego wykrywania raka i innych chorób.
Cytowanie: Imani, A., Hosseinpour, S., Azimzadeh, M. et al. Artificial neural network modeling and optimization of an electrochemical biosensor for plasma miR-155-based breast cancer detection. Sci Rep 16, 7893 (2026). https://doi.org/10.1038/s41598-026-36466-6
Słowa kluczowe: biosensor raka piersi, wykrywanie microRNA-155, sensor elektrochemiczny, sztuczne sieci neuronowe, optymalizacja algorytmem genetycznym