Clear Sky Science · pl
ATF4 reguluje dysfunkcję mitochondriów i mitofagię, przyczyniając się do apoptozy komórek śródbłonka rogówki
Dlaczego „szybka” oka może mętnieć
Nasze rogówki — przezroczyste „szyby” oczu — zachowują przejrzystość dzięki cienkiej, pracowitej warstwie komórek na ich wewnętrznej powierzchni. W dystrofii śródbłonka rogówki typu Fuchsa (FECD) miliony ludzi stopniowo tracą te komórki, co prowadzi do obrzęku, zamglonego widzenia i często przeszczepów rogówki. To badanie stawia podstawowe, ale kluczowe pytanie: co sprawia, że te komórki podejmują decyzję o śmierci, i czy wyłączenie jednego molekularnego „włącznika” może je uratować?
Delikatna warstwa komórek, która utrzymuje przejrzystość
Śródbłonek rogówki to jednowarstwowa siatka sześciokątnych komórek, która nieustannie wypompowuje płyn z rogówki, aby zachować jej przejrzystość. W FECD komórki te ulegają stresowi i stopniowo zanikają, podczas gdy na błonie podstawnej gromadzą się grudki nieprawidłowego materiału, zwane guttae. Ponieważ nie ma zatwierdzonych leków na FECD, a głównym leczeniem są przeszczepy rogówki, naukowcy próbują zrozumieć dokładnie, jak stres wewnątrz tych komórek popycha je ku śmierci. Wcześniejsze prace wskazywały oddzielnie na napięcia w dwóch kluczowych przedziałach komórkowych — retikulum endoplazmatycznym (fabryce fałdowania białek) i mitochondriach (elektrowniach komórki) — ale nie było jasne, jak te dwie odpowiedzi na stres ze sobą rozmawiają.
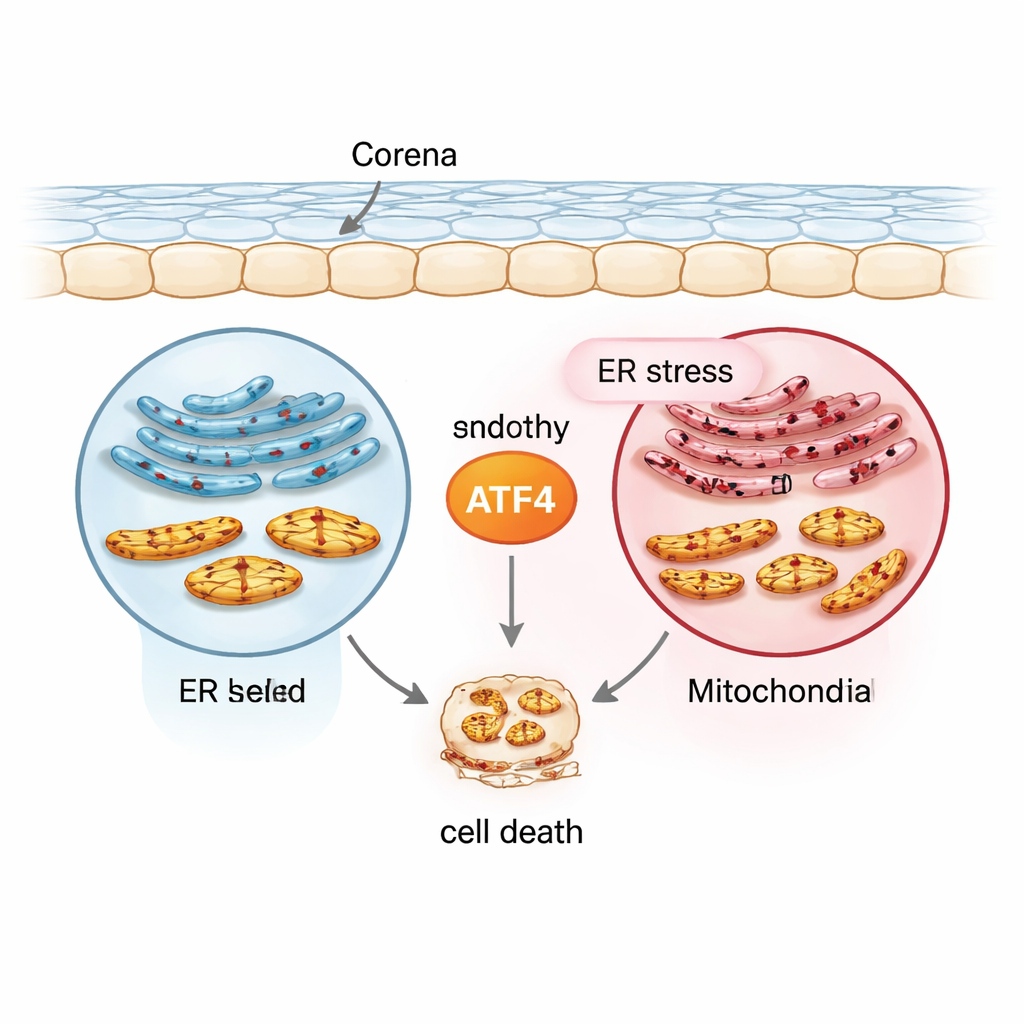
Wysłannik stresu w centrum uwagi: ATF4
Zespół skupił się na białku zwanym ATF4, czynniku transkrypcyjnym, który włącza lub wyłącza wiele genów odpowiedzi na stres. Używając normalnej linii ludzkich komórek śródbłonka rogówki (21T), linii przypominającej FECD z ekspansją powtórzeń TCF4 związaną z chorobą (F35T), pierwotnych ludzkich komórek śródbłonka oraz modeli mysim poddanych działaniu promieniowania UVA, stworzyli zakres warunków naśladujących przewlekły stres. Wywołali stres retikulum endoplazmatycznego za pomocą leku tunicamycyny i zmierzyli poziomy ATF4 oraz innych markerów. W porównaniu z komórkami normalnymi, komórki przypominające FECD miały wyższe poziomy ATF4 i związanych białek stresowych na początku, a ATF4 wzrastał jeszcze bardziej przy przewlekłym stresie zarówno w hodowlach, jak i w ludzkich tkankach rogówki. Ten wzorzec umieszcza ATF4 na skrzyżowaniu między wczesnymi odpowiedziami ochronnymi a późniejszymi sygnałami prowadzącymi do autodestrukcji.
Od awarii zasilania do programowanej śmierci
Następnie badacze przyjrzeli się, jak ten stres wpływa na mitochondria. W komórkach przypominających FECD mitochondria wytwarzały mniej ATP, traciły potencjał elektromotoryczny błony i rozpadały się z długich, sieciopodobnych kształtów na wiele małych fragmentów. Zmiany te nasilały się, gdy stres retikulum endoplazmatycznego był przedłużony. Jednocześnie klasyczne białka śmierci komórkowej — takie jak aktywowane kaspazy i białko naprawy DNA PARP w jego pociętej, pro‑śmierci formie — stawały się bardziej obfite, podczas gdy ochronne białka, takie jak Bcl‑2, malały. Razem te zmiany wskazują, że zestresowane komórki śródbłonka rogówki w FECD są popychane ku apoptozie napędzanej przez mitochondria, uporządkowanej, ale nieodwracalnej formie zaprogramowanej śmierci komórkowej.
System sprzątający zawodzi przy przewlekłym stresie
Zazwyczaj silnie uszkodzone mitochondria są usuwane przez proces recyklingu zwany mitofagią, w którym są oznaczane i otaczane małymi pęcherzykami do utylizacji. Zespół wykazał, że wczesne „inicjujące” cząsteczki mitofagii (Parkin i LC3) były włączone zarówno w komórkach normalnych, jak i przypominających FECD, zwłaszcza po stresie. Jednak kluczowe białka wspomagające były zmniejszone, a mikroskopia elektronowa pokazała nagromadzenie częściowo strawionych mitochondriów uwięzionych w pęcherzykach. Sugeruje to, że choć proces sprzątania się rozpoczynał, nie kończył się pomyślnie, pozostawiając komórki z zalegającymi uszkodzonymi „elektrowniami”, które dodatkowo napędzają stres i śmierć zamiast regeneracji.
Wyłączenie ATF4 ratuje komórki
Aby sprawdzić, czy ATF4 napędza tę spiralę, badacze użyli małych interferujących RNA do częściowego wyciszenia ATF4 w hodowanych komórkach śródbłonka rogówki. Przy tym samym przewlekłym stresie komórki z obniżonym poziomem ATF4 wykazywały niższe poziomy białek promujących śmierć, zdrowszy potencjał błony mitochondrialnej, mniejsze fragmentowanie i lepszą przeżywalność w testach żywotności. Co ważne, liczba zablokowanych struktur mitofagii zmalała, co sugeruje, że obniżenie ATF4 pomaga przywrócić bardziej efektywną równowagę między uszkodzeniem a oczyszczaniem. U myszy zaprojektowanych tak, by miały tylko jedną czynną kopię genu ATF4, ekspozycja na UVA powodowała mniejszą aktywację partnerskiego białka pro‑śmierci CHOP i zachowywała więcej komórek śródbłonka o normalnym kształcie w porównaniu z myszami w pełni posiadającymi ATF4.
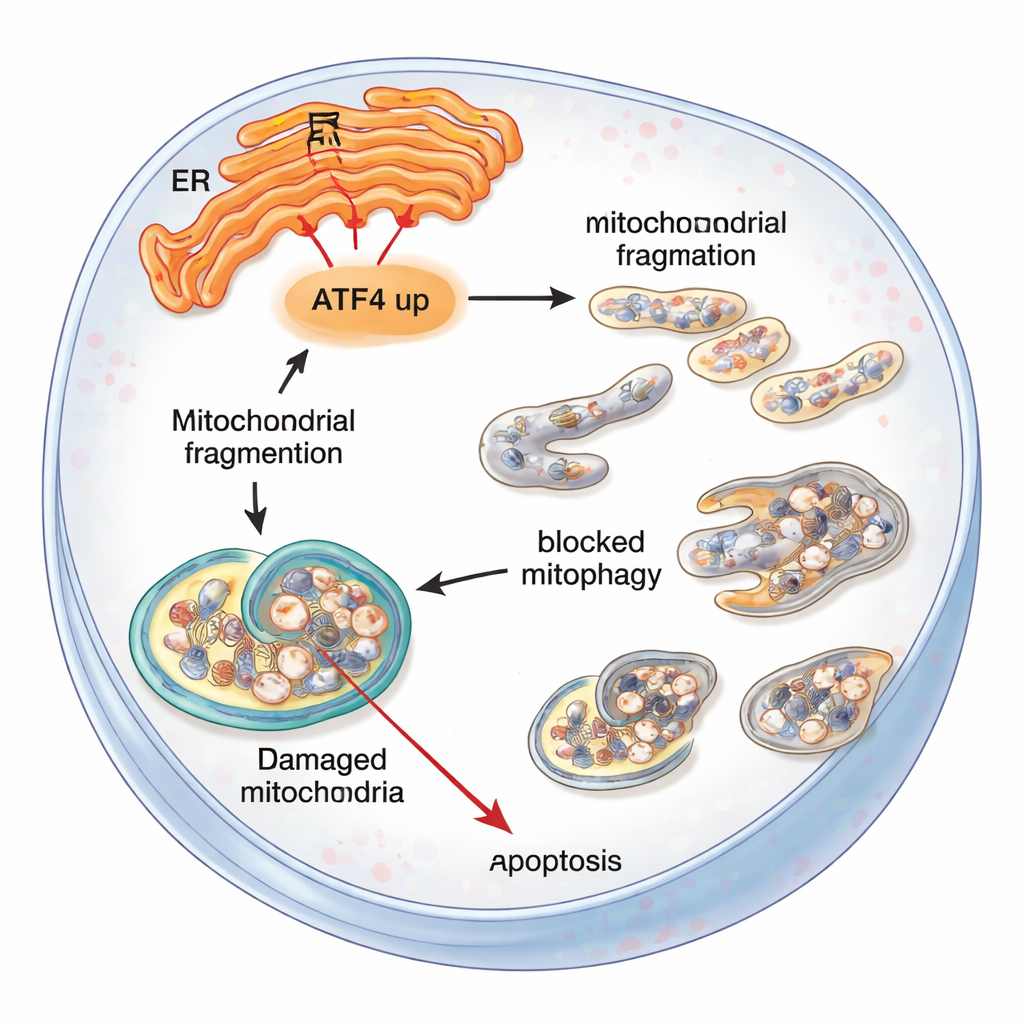
Co to oznacza dla osób z FECD
Dla osób niebędących specjalistami przekaz jest taki, że jeden wysłannik stresu, ATF4, może przesunąć komórki śródbłonka rogówki od radzenia sobie do załamywania się. Gdy stres retikulum endoplazmatycznego jest długotrwały, ATF4 przyczynia się do zaburzenia funkcji mitochondriów, blokuje mechanizm sprzątania komórkowego i ostatecznie sprzyja autodestrukcji tych kluczowych komórek. Zmniejszenie aktywności ATF4 — genetycznie u myszy lub za pomocą ukierunkowanych narzędzi molekularnych w komórkach — chroni mitochondria, poprawia usuwanie odpadów i utrzymuje więcej komórek przy życiu. Choć prace te pozostają na etapie badań laboratoryjnych i zwierzęcych, wskazują ATF4 i powiązane szlaki stresowe jako obiecujące cele terapeutyczne, które w przyszłości mogłyby opóźnić lub zapobiec postępowi dystrofii Fuchsa i zmniejszyć potrzebę przeszczepów rogówki.
Cytowanie: Qureshi, S., Kim, S.Y., Lee, S. et al. ATF4 regulates mitochondrial dysfunction and mitophagy, contributing to corneal endothelial apoptosis. Sci Rep 16, 5960 (2026). https://doi.org/10.1038/s41598-026-36453-x
Słowa kluczowe: Fuchs dystrofia śródbłonka rogówki, śródbłonek rogówki, stres mitochondrialny, mitofagia, ATF4