Clear Sky Science · pl
Całościowe podejście do identyfikacji nowych sieci interakcji miRNA–mRNA w kardiomiopatii związanej z LMNA
Dlaczego mali regulatorzy serca mają znaczenie
Kardiomiopatia rozstrzeniowa to poważne schorzenie, w którym serce się powiększa i osłabia, często prowadząc do niewydolności serca, zagrażających życiu zaburzeń rytmu, a nawet nagłej śmierci. U wielu rodzin choroba ma podłoże dziedziczne, a zmiany w genie o nazwie LMNA są częstą przyczyną. To badanie stawia pozornie proste pytanie o dużych konsekwencjach: w sercach uszkodzonych przez mutacje LMNA, które geny są włączane lub wyłączane i które maleńkie cząsteczki RNA ciągną za te dźwignie? Mapując te molekularne rozmowy w szczegółach, praca wskazuje nowe sposoby przewidywania, monitorowania, a być może pewnego dnia leczenia tej agresywnej postaci choroby serca.
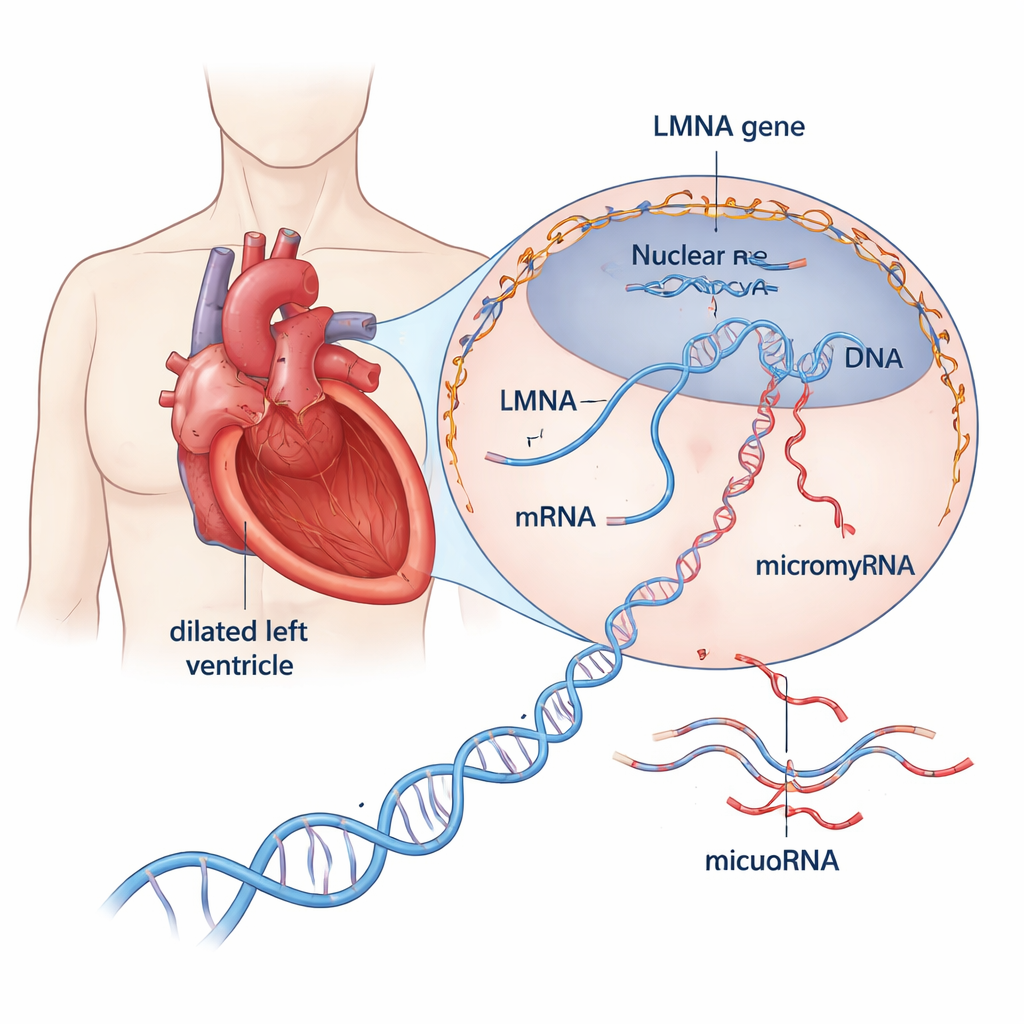
Bliższe spojrzenie na groźną chorobę serca
Kardiomiopatia rozstrzeniowa rozciąga i ścieńcza główną komorę pompującą serca, osłabiając jego zdolność do tłoczenia krwi po całym ciele. Około jednej trzeciej do połowy przypadków wcześniej określanych jako „idiopatyczne” okazuje się mieć podłoże genetyczne. Spośród ponad 30 zaangażowanych genów wyróżnia się LMNA: szkodliwe warianty w tym genie odpowiadają za około 10% przypadków dziedzicznych i wiążą się z szybkim postępem choroby, wczesnymi zaburzeniami rytmu oraz wysokim ryzykiem nagłej śmierci sercowej. LMNA koduje białka strukturalne tworzące rusztowanie wokół DNA komórki, pomagające utrzymać kształt jądra i wpływające na to, które geny są aktywne. Jednak to, w jaki sposób wadliwe białka LMNA popychają serca w kierunku niewydolności, pozostawało słabo poznane.
Śledząc komunikaty wewnątrz serc mysich
Aby to zbadać, naukowcy użyli modelu myszy niosącego znaną mutację LMNA (R249W), która rozwija postać kardiomiopatii rozstrzeniowej przypominającą chorobę u ludzi. W 50. tygodniu życia — gdy myszy wykazywały powiększone komory, osłabioną funkcję pompową i bliznowate włóknienie — zespół pobrał tkankę serca i przeanalizował dwa typy RNA: mRNA, które niesie instrukcje tworzenia białek, oraz mikroRNA (miRNA), krótkie niekodujące cząsteczki, które subtelnie regulują aktywność genów przez blokowanie lub degradację określonych mRNA. Przy użyciu sekwencjonowania wysokoprzepustowego i rygorystycznych filtrów statystycznych zidentyfikowali 2 148 genów, których aktywność zmieniła się w sercach mutantów, oraz 53 miRNA, które były albo zwiększone, albo zmniejszone w porównaniu z zdrowymi myszami.
Co zmienia się w chorych komórkach serca
Gdy badacze pogrupowali zmienione geny według szlaków biologicznych, wyłoniło się kilka motywów. Wiele zmienionych genów było związanych z kurczliwością komórek mięśnia sercowego, przyleganiem komórek do siebie i do macierzy zewnątrzkomórkowej, przewodzeniem impulsów elektrycznych w sercu oraz przetwarzaniem tłuszczów w celu wytwarzania energii. Odkrycia te dobrze pasują do obrazu klinicznego choroby związanej z LMNA: sztywniej, włóknistej tkanki; zaburzonego przewodzenia sprzyjającego arytmii; oraz zaburzonej równowagi energetycznej. Analizy szlaków z użyciem uznanych baz danych potwierdziły wzbogacenie w procesy remodelingu macierzy zewnątrzkomórkowej, kanały jonowe zależne od napięcia, komunikację przypominającą synaptyczną w sercu oraz metabolizm kwasów tłuszczowych — co sugeruje, że mutacja LMNA zaburza wiele ze sobą powiązanych systemów, a nie pojedynczy defekt.
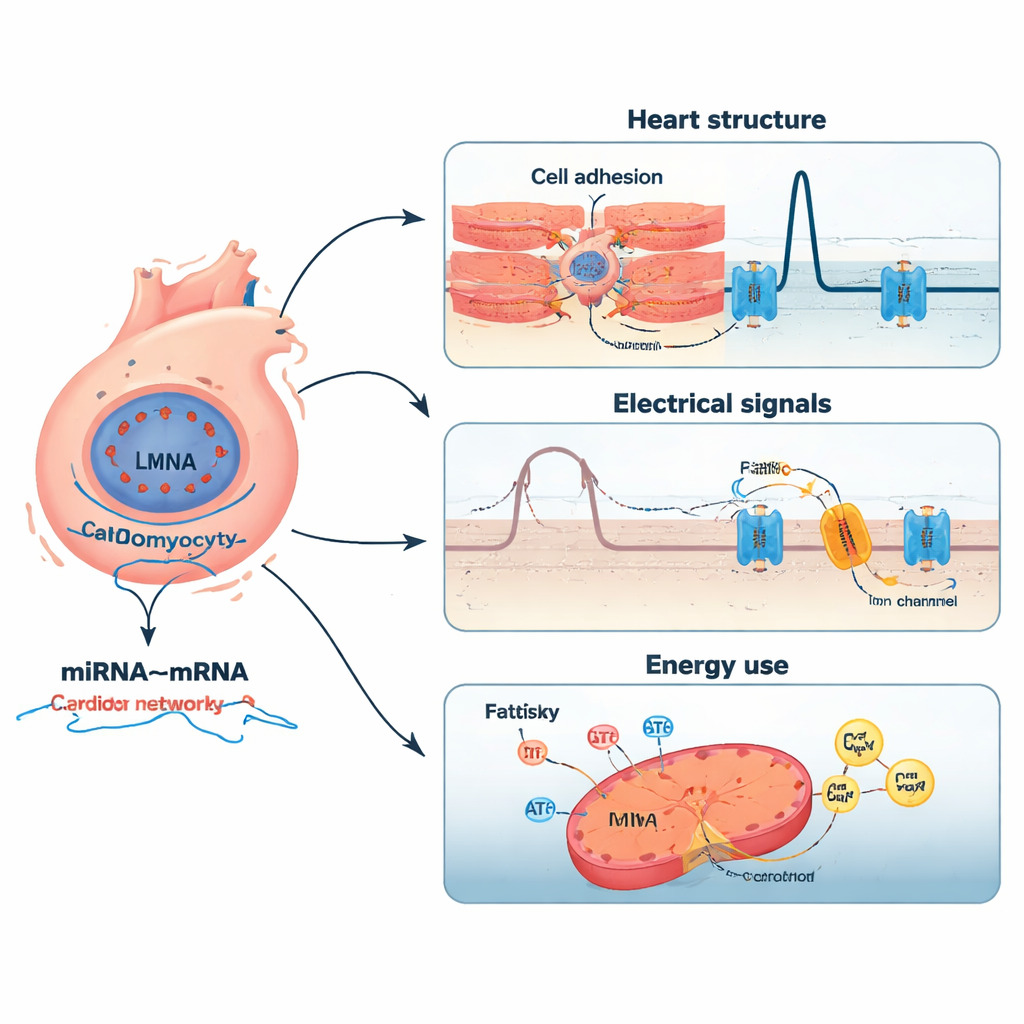
Sieci małych przełączników i ich celów
Badanie poszło dalej, łącząc miRNA z ich prawdopodobnymi celami mRNA. Korzystając z analiz korelacyjnych i weryfikując wyniki względem dużych baz danych eksperymentalnie potwierdzonych interakcji, autorzy zbudowali sieć wysokiego zaufania obejmującą 2 197 par miRNA–mRNA z udziałem 12 kluczowych miRNA. Niektóre miRNA były bardziej aktywne i wydawały się tłumić geny istotne dla rozwoju serca, gospodarki wapniowej i odpowiedzi na stres oksydacyjny. Inne były mniej aktywne, potencjalnie uwalniając hamulce na geny zaangażowane w adhezję komórek, zapalenie i przebudowę strukturalnego rusztowania serca. Na przykład jedno miRNA (miR-183-5p) powiązano z receptorem w szlaku sygnalizacji Wnt, który wpływa na komunikację międzykomórkową, podczas gdy inne (miR-3473a) łączyło się z kanałem uwalniającym wapń centralnym dla rytmu serca. Razem te sieci pokazują, jak subtelne przesunięcia w małych regulatorach RNA mogą wzmocnić wpływ mutacji LMNA.
Od map molekularnych do przyszłych terapii
Dla osób niezwiązanych bezpośrednio z dziedziną sedno jest takie, że to badanie dostarcza szczegółowej mapy tego, jak mutacja LMNA przekształca wewnętrzne okablowanie serca na poziomie kontroli genów. Zamiast jednego „złego genu”, choroba odzwierciedla kaskadę zmienionych komunikatów — wiele z nich zorganizowanych przez miRNA — które wpływają na strukturę serca, stabilność elektryczną i wykorzystanie energii. Choć praca została wykonana na myszach i w dużej mierze opiera się na analizach komputerowych, wyróżnia konkretne pary miRNA–gen jako obiecujących kandydatów na przyszłe markery we krwi lub terapie celowane. W dłuższej perspektywie dostrojenie tych małych przełączników RNA może pomóc lekarzom lepiej przewidzieć, kto jest w największym ryzyku, precyzyjniej monitorować postęp choroby i projektować bardziej spersonalizowane leczenie dla rodzin dotkniętych kardiomiopatią związaną z LMNA.
Cytowanie: Córdoba-Caballero, J., Martínez, F.B., Campuzano, O. et al. An integrative approach to identify novel miRNA-mRNA interaction networks in LMNA-cardiomyopathy. Sci Rep 16, 6110 (2026). https://doi.org/10.1038/s41598-026-36439-9
Słowa kluczowe: kardiomiopatia rozstrzeniowa, gen LMNA, mikroRNA, regulacja genów, niewydolność serca