Clear Sky Science · pl
Aktywność przeciwnowotworowa QAL333 i modelowanie predykcyjne: zintegrowana analiza transkryptomiczno-bioinformatyczna ujawnia wybiórczą cytotoksyczność i determinanty wrażliwości
Dlaczego ten nowy kandydat na lek ma znaczenie
Leki przeciwnowotworowe często działają dobrze u niektórych pacjentów, a zawiodą u innych, w dużej mierze dlatego, że guzy różnią się swoim wewnętrznym „okablowaniem”. W badaniu zaprezentowano nowo zaprojektowany związek QAL333, który wydaje się uderzać znacznie silniej w niektóre nowotwory jelita grubego niż w inne, przy jednoczesnym oszczędzaniu wielu normalnych komórek. Równie ważne jest to, że autorzy pokazują, jak wzorce aktywności genów w komórkach nowotworowych mogą pomóc przewidzieć, kto najprawdopodobniej skorzysta, sugerując bardziej precyzyjne, spersonalizowane strategie leczenia.
Skoncentrowany cios w określone typy guzów
Zespół rozpoczął od testowania QAL333, cząsteczki syntetycznej spokrewnionej z rodziną związków już znanych z działania uszkadzającego komórki nowotworowe, na szerokim panelu 15 ludzkich linii komórkowych nowotworowych i trzech linii nie-nowotworowych. Stwierdzili, że komórki raka jelita grubego, szczególnie linia nazwana SW620, były wysoce wrażliwe — lek zabijał je przy stosunkowo niskich dawkach. Natomiast komórki potrójnie ujemnego raka piersi były znacznie bardziej oporne i wymagały dawek ponad dziesięciokrotnie wyższych, trudnych do bezpiecznego osiągnięcia. Co ciekawe, nie wszystkie komórki nie-nowotworowe reagowały tak samo: niektóre były wrażliwe, inne, jak powszechnie używana linia komórek nerkowych, okazały się zaskakująco oporne. Ten wzorzec wskazywał, że efekty QAL333 zależą bardziej od wewnętrznej biologii komórki niż od etykiety „nowotworowa” czy „normalna”.
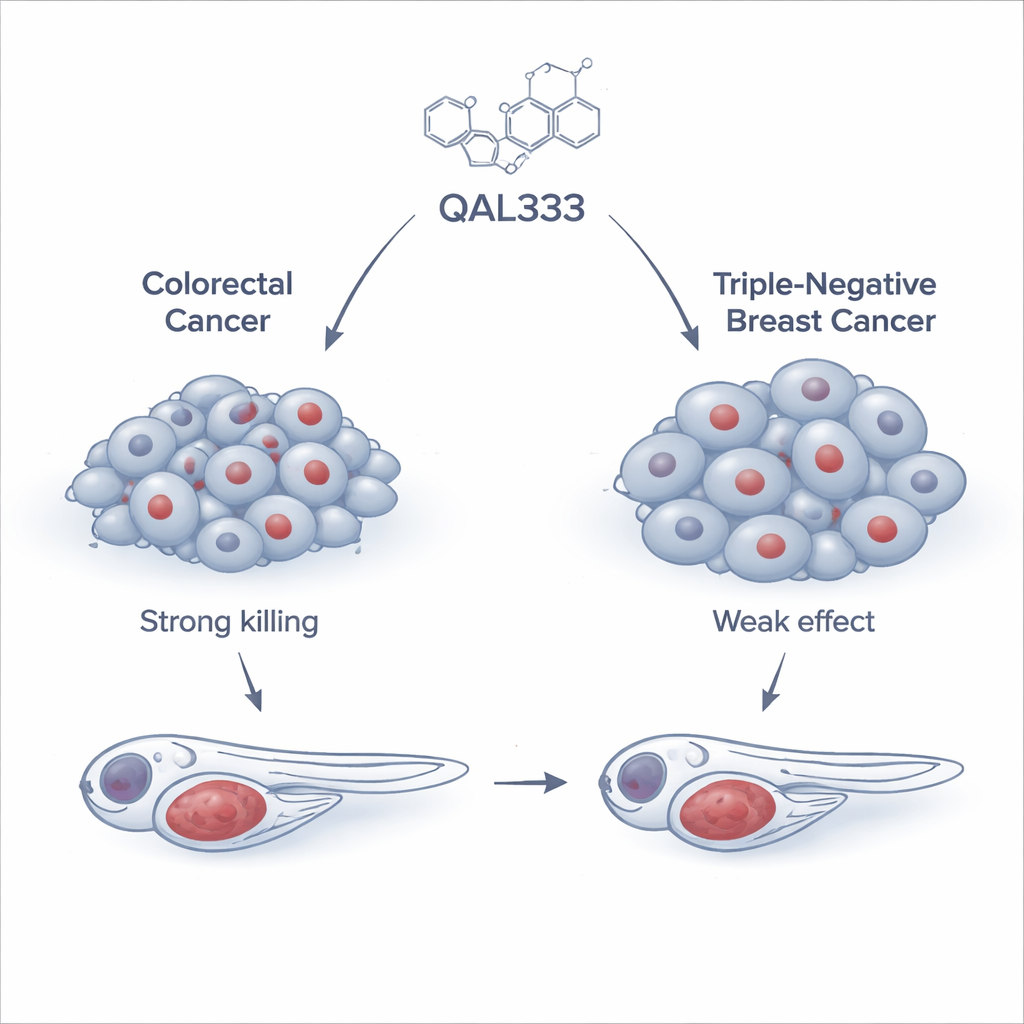
Testowanie leku w organizmach żywych
Aby sprawdzić, czy obiecujące wyniki z hodowli komórek utrzymają się w organizmie żywym, badacze zwrócili się do danio pręgowanego, małej przezroczystej ryby szeroko stosowanej do modelowania chorób człowieka. Implantowali fluorescencyjnie znakowane ludzkie komórki nowotworowe do embrionów danio i leczyli je QAL333. U ryb niosących komórki raka jelita grubego lek wyraźnie spowolnił wzrost guza, zbliżając się do efektu standardowej kombinacji chemioterapeutyków stosowanej w klinice. Natomiast guzy utworzone z komórek potrójnie ujemnego raka piersi prawie nie reagowały, choć standardowy lek stosowany w raku piersi, paklitaksel, działał dobrze w tym samym modelu. Testy in vivo wzmocniły przekonanie, że siła QAL333 leży w podzbiorze guzów, a nie w uniwersalnym działaniu przeciw wszystkim nowotworom.
Zaglądanie do wnętrza komórek, by zrozumieć mechanizm działania QAL333
Aby zrozumieć, dlaczego niektóre komórki umierają, a inne opierają się, naukowcy mierzyli, jak tysiące genów zmieniają poziomy aktywności po leczeniu QAL333. W wrażliwych komórkach raka jelita grubego kluczowe geny napędzające cykl podziałowy i wzrost komórki zostały wyciszone, a główne szlaki przeżycia osłabione. Zmienione zostały sygnały związane ze stresem oksydacyjnym oraz forma śmierci komórkowej odmienna od klasycznie rozumianej apoptozy, co sugeruje, że QAL333 przeciąża już kruche systemy zarządzające uszkodzeniami w tych komórkach. Komórki opornego raka piersi, przeciwnie, włączają programy stresowe i zapalne kontrolowane przez czynniki takie jak NF-κB, które są znane z pomagania komórkom w radzeniu sobie ze szkodliwymi warunkami. To porównanie „side-by-side” stworzyło obraz, w którym QAL333 przytłacza słabe obrony w niektórych komórkach, podczas gdy inne uruchamiają skuteczną odpowiedź przeciwną.
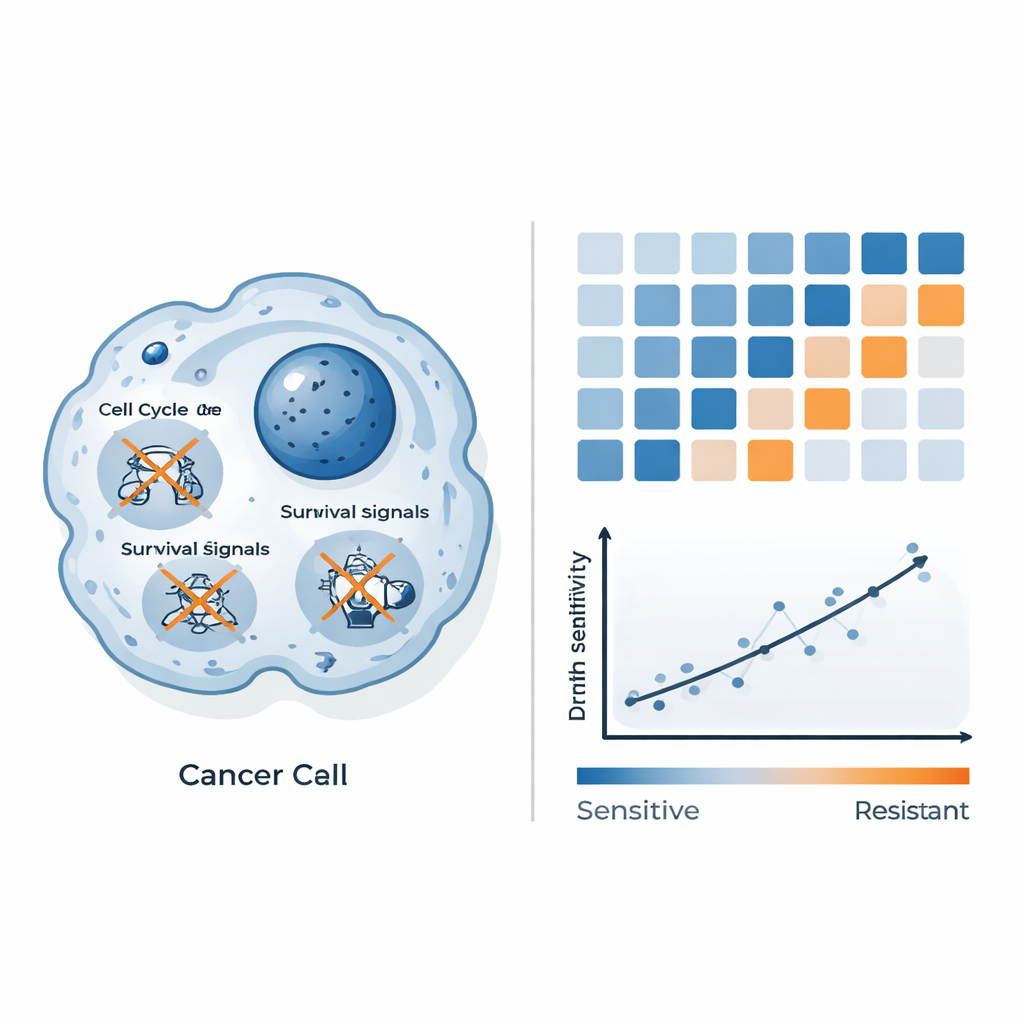
Wykorzystanie wzorców genowych do przewidywania odpowiedzi
Ponad katalogowaniem zmian genów, badacze zapytali, czy te wzorce można przekształcić w praktyczne narzędzie przewidywania. Połączyli dane o stanie wyjściowym aktywności genów z panelu linii komórkowych z ich zmierzoną wrażliwością na lek i użyli uczenia maszynowego do wyszukania najbardziej informatywnych sygnałów. Zamiast polegać na pojedynczych genach, pogrupowali geny w szlaki biologiczne i stworzyli złożony „wynik szlakowy” zbudowany z trzech systemów: jak komórki przetwarzają energię i związki chemiczne (szlaki metaboliczne), jak organizują swoje otoczenie (proteoglikany i powiązane struktury w nowotworze) oraz jak zaaranżowany jest ich cytoszkielet. Ten złożony wskaźnik silnie korelował z tym, ile QAL333 było potrzebne do zabicia każdej linii komórkowej: niższe wyniki wiązały się z wyższą wrażliwością, a wyższe — z opornością. Innymi słowy, sposób, w jaki sieci te są dostrojone wewnątrz guza, może prognozować, jak dobrze QAL333 zadziała.
Niespodziewane wskazówki dotyczące szerszych efektów biologicznych
Choć głównym celem był nowotwór, QAL333 wykazał także zdolność do zakłócania „kworum-sensing”, systemu komunikacji bakterii służącego koordynacji zachowań, takich jak tworzenie biofilmu. Przy bardzo małych dawkach związek zmniejszał tworzenie biofilmu przez bakterię wywołującą choroby dziąseł i tłumił niektóre sygnały zapalne w komórkach układu odpornościowego. Autorzy traktują te obserwacje jako wczesne, eksploracyjne wyniki, lecz sugerują one, że QAL333 lub związane cząsteczki mogą kiedyś znaleźć zastosowanie poza leczeniem raka, na przykład w infekcjach, gdzie społeczności bakteryjne są trudne do zwalczenia.
Co to może znaczyć dla przyszłych pacjentów
Podsumowując, badanie pozycjonuje QAL333 jako wybiórczego kandydata na lek, który uderza w wrażliwe guzy jelita grubego przy jednoczesnym oszczędzaniu wielu innych typów komórek, a jednocześnie dostarcza mapy drogowej pozwalającej przewidzieć, które guzy najpewniej zareagują. Jeśli potwierdzą to bardziej zaawansowane modele zwierzęce, a ostatecznie badania kliniczne, prosty test ekspresji genów mógłby pomóc lekarzom zdecydować, kiedy QAL333 jest odpowiednim wyborem, wpisując się w szerszy cel dopasowywania leczenia raka do specyficznego „okablowania” każdego guza. Jednocześnie praca podkreśla, że nawet obiecujące leki mają ograniczenia: raki piersi i inne oporne guzy mogą wymagać sprytnych kombinacji terapii lub zupełnie innych strategii.
Cytowanie: Kim, H.H., Im, S., Kim, J. et al. QAL333’s antitumor activity and predictive modeling: integrated transcriptomic-bioinformatic analysis reveals selective cytotoxicity and sensitivity determinants. Sci Rep 16, 5648 (2026). https://doi.org/10.1038/s41598-026-36430-4
Słowa kluczowe: rak jelita grubego, terapia celowana, ekspresja genów, modelowanie wrażliwości na leki, ksenograft u danio pręgowanego