Clear Sky Science · pl
Kwas pseudolarowy B promuje ferroptozę komórek raka płuca zależną od zwiększenia poziomu Survivin przez JNK/ERK
Związek roślinny uderza w guzy płuc
Rak płuca pozostaje jednym z najgroźniejszych nowotworów na świecie, a wielu pacjentów albo nie reaguje na nowoczesne leki, albo doświadcza poważnych skutków ubocznych. W tym badaniu przeanalizowano naturalną substancję zwaną kwasem pseudolarowym B, wyizolowaną z kory tradycyjnego chińskiego drzewa, by sprawdzić, czy może selektywnie zabijać komórki raka płuca, oszczędzając zdrową tkankę płucną. Naukowcy odkrywają nieoczekiwany sposób, w jaki związek ten niszczy komórki nowotworowe, wywołując specyficzną formę śmierci komórkowej zależną od żelaza i uszkodzeń lipidów wewnątrz komórek.
Dlaczego cząsteczka z kory drzewa ma znaczenie
Lekarze pilnie potrzebują nowych terapii, które pokonają guzy oporne na leki, nie szkodząc komórkom normalnym. Leki pochodzenia roślinnego dały nam już ważne środki przeciwnowotworowe, takie jak paklitaksel i winkrystyna. Kwas pseudolarowy B wykazywał działanie przeciwnowotworowe w kilku typach nowotworów, lecz mechanizmy jego działania w raku płuca były dotąd niejasne i czasami sprzeczne. W niniejszym badaniu naukowcy testowali kwas pseudolarowy B na ludzkich komórkach raka płuca i na normalnych komórkach oskrzelowych in vitro, a następnie na myszach z wszczepionymi ludzkimi guzami płuc, aby dokładnie odwzorować sposób działania tej naturalnej substancji.
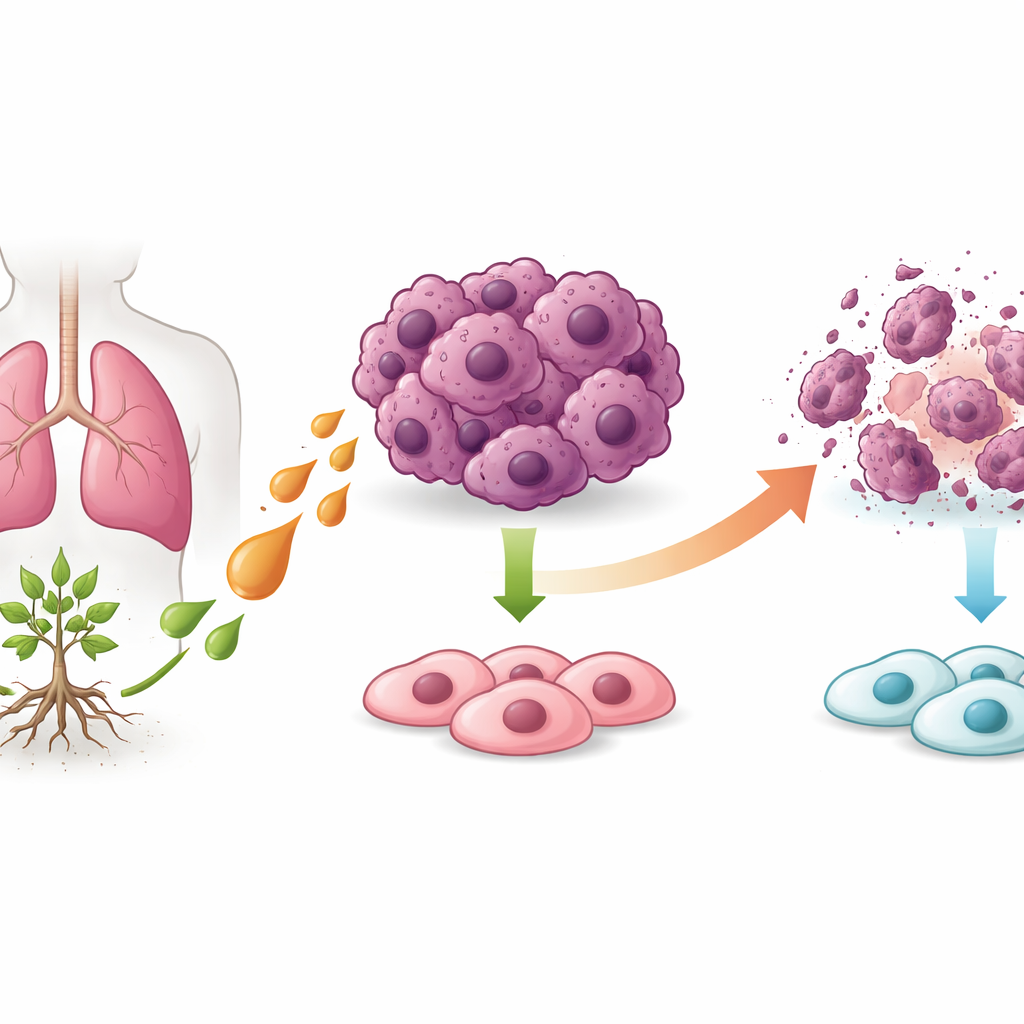
Selektywne uderzenie w komórki nowotworowe
W hodowlach komórkowych kwas pseudolarowy B znacząco hamował wzrost dwóch różnych linii komórek raka płuca, podczas gdy miał niewielki wpływ na normalne komórki oskrzelowe. Leczone komórki nowotworowe przestały się dzielić, utraciły zdolność do tworzenia gęstych kolonii i wykazywały wyraźne oznaki uszkodzenia. Co ciekawe, klasyczna forma samobójczej śmierci komórki, czyli apoptoza, odgrywała tylko niewielką rolę: blokowanie kluczowych enzymów odpowiedzialnych za apoptozę ani zahamowanie autofagii nie ratowało komórek. Jednocześnie białka znane jako „inhibitory apoptozy”, które zwykle pomagają komórkom nowotworowym przetrwać, były wyraźnie zmniejszone, co sugeruje, że lek popycha komórki w kierunku innej ścieżki śmierci.
Śmierć komórkowa napędzana żelazem w obrębie guza
Analiza aktywności genów w skali całego genomu wykazała, że wiele zmienionych genów wskazuje na ferroptozę — regulowaną formę śmierci komórkowej napędzaną żelazem i degradacją lipidów błonowych. Przyglądając się wnętrzu komórek, badacze zaobserwowali typowe cechy ferroptozy: skurczone, uszkodzone mitochondria; wysokie poziomy reaktywnych form tlenu; zwiększoną zawartość jonów żelaza(II); oraz większe utlenienie lipidów w błonach komórkowych. Kluczowe białka ochronne, które zwykle chronią przed ferroptozą, takie jak SLC7A11 i GPX4, były zmniejszone zarówno na poziomie białka, jak i RNA. Gdy naukowcy dodali chelator żelaza blokujący ferroptozę, śmierć komórek, akumulacja żelaza i uszkodzenia lipidów zostały w dużym stopniu odwrócone, co potwierdza, że kwas pseudolarowy B zabija komórki raka płuca głównie przez ferroptozę.
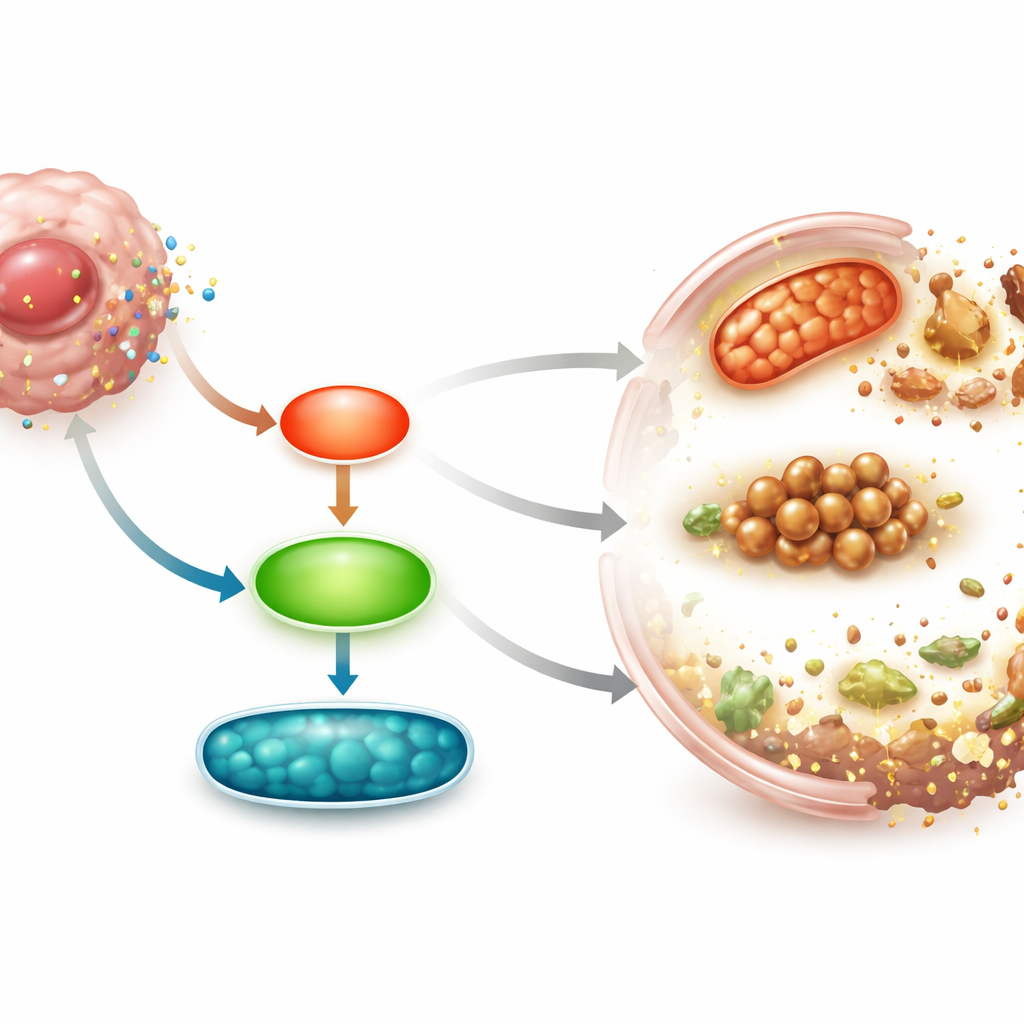
Nieoczekiwany pomocnik: Survivin i sygnały komórkowe
Niespodzianką była dynamika białka Survivin, członka rodziny inhibitorów apoptozy. Podczas gdy większość tych białek przeżycia była zmniejszona po leczeniu, poziom Survivin zwiększył się wyraźnie na poziomie białka, mimo że jego RNA nie uległo zmianie. Gdy naukowcy zablokowali Survivin przy pomocy małocząsteczkowego inhibitora lub poprzez wyciszenie genowe RNA, kwas pseudolarowy B stracił dużą część swojej mocy zabijającej: komórki raka płuca lepiej przeżywały, spadły poziomy żelaza i uszkodzeń lipidów, a ochronne białka przeciwferroptozowe wróciły do poziomów wyjściowych. Dalsza analiza szlaków sygnałowych wykazała, że po terapii aktywacja dwóch ścieżek wewnątrzkomórkowych, znanych jako JNK i ERK, wzrosła. Hamowanie tych sygnałów zmniejszało ferroptozę, przywracało białka przeżycia i obniżało poziom Survivin, co pokazuje, że kwas pseudolarowy B wywołuje ferroptozę przez oś JNK/ERK–Survivin.
Z naczyń hodowlanych do żywych guzów
Aby sprawdzić, czy te efekty utrzymują się in vivo, zespół wszczepił ludzkie komórki raka płuca myszom, aby wyrosły małe guzy. Codzienne leczenie kwasem pseudolarowym B znacząco spowolniło wzrost guzów, nie powodując przy tym widocznej utraty masy ciała ani innych objawów toksyczności. Próbki guzów od leczonych zwierząt wykazywały wysokie poziomy markera uszkodzeń lipidów, zwiększony poziom Survivin i mniej komórek dzielących się — wszystko zgodne z toczącą się ferroptozą i osłabieniem guza. Wyniki in vivo odpowiadały obserwacjom z eksperymentów laboratoryjnych i wspierały tezę, że związek roślinny może ograniczać wzrost nowotworu przez wywoływanie śmierci komórkowej zależnej od żelaza.
Co to oznacza dla przyszłych terapii
Podsumowując, badanie pokazuje, że kwas pseudolarowy B może selektywnie zabijać komórki raka płuca, popychając je do ferroptozy — formy śmierci komórkowej zasilanej przez żelazo i uszkodzenia błon — zamiast polegać głównie na klasycznej apoptozie. Efekt ten zależy od łańcucha sygnałowego obejmującego białka JNK i ERK oraz nieoczekiwanego wzrostu białka przeżycia Survivin, które w tym kontekście staje się niezbędne do przebiegu ferroptozy. Choć przed zastosowaniem tego związku u pacjentów wciąż wiele pracy, wyniki sugerują, że świadome wykorzystanie ferroptozy, być może przy pomocy molekuł pochodzenia roślinnego, może otworzyć nowe drogi leczenia opornych raków płuca.
Cytowanie: Li, Y., Yu, C., Yang, S. et al. Pseudolaric acid B promotes lung cancer cells ferroptosis depending on JNK/ERK-mediated upregulation of survivin. Sci Rep 16, 8294 (2026). https://doi.org/10.1038/s41598-026-36423-3
Słowa kluczowe: rak płuca, kwas pseudolarowy B, ferroptoza, Survivin, szlaki sygnałowe MAPK