Clear Sky Science · pl
Od modelowania QSAR in silico do testu MTT in vitro: eksperymentalna walidacja nowych związków uPAR dla potrójnie ujemnego raka piersi (TNBC) i raka skóry
Dlaczego te badania są ważne
Nowotwory takie jak potrójnie ujemny rak piersi i niektóre raki skóry są wyjątkowo trudne w leczeniu, ponieważ szybko się rozprzestrzeniają i często opierają się standardowym terapiom. W tej pracy badano obiecujący nowy cel na powierzchni komórek nowotworowych — zwany uPAR — i pokazano, jak połączenie projektowania leków wspomaganego komputerowo z eksperymentami laboratoryjnymi może ujawnić nowe kandydaty na leki, które mogą spowolnić lub zatrzymać rozprzestrzenianie się tych agresywnych guzów.
Drzwi, które pomagają nowotworowi się rozsiać
Aby guz stał się śmiertelny, jego komórki muszą oderwać się od pierwotnego miejsca, rozpuścić otaczającą tkankę, wejść do krwiobiegu i skolonizować odległe narządy. uPAR jest kluczowym wspomagaczem tego procesu. Znajduje się na powierzchni komórki nowotworowej i współdziała z partnerami białkowymi, aktywując enzymy rozkładające strukturę podporową otoczenia, co ułatwia komórkom poruszanie się i inwazję. uPAR występuje w szczególnie wysokich ilościach w komórkach potrójnie ujemnego raka piersi i w niektórych rakach skóry, a jego obfitość wiąże się z szybszym wzrostem, większą inwazyjnością i gorszym rokowaniem pacjentów. Z tego powodu uPAR jest atrakcyjnym — choć jak dotąd niedostatecznie wykorzystanym — celem dla leków przeciwnowotworowych.
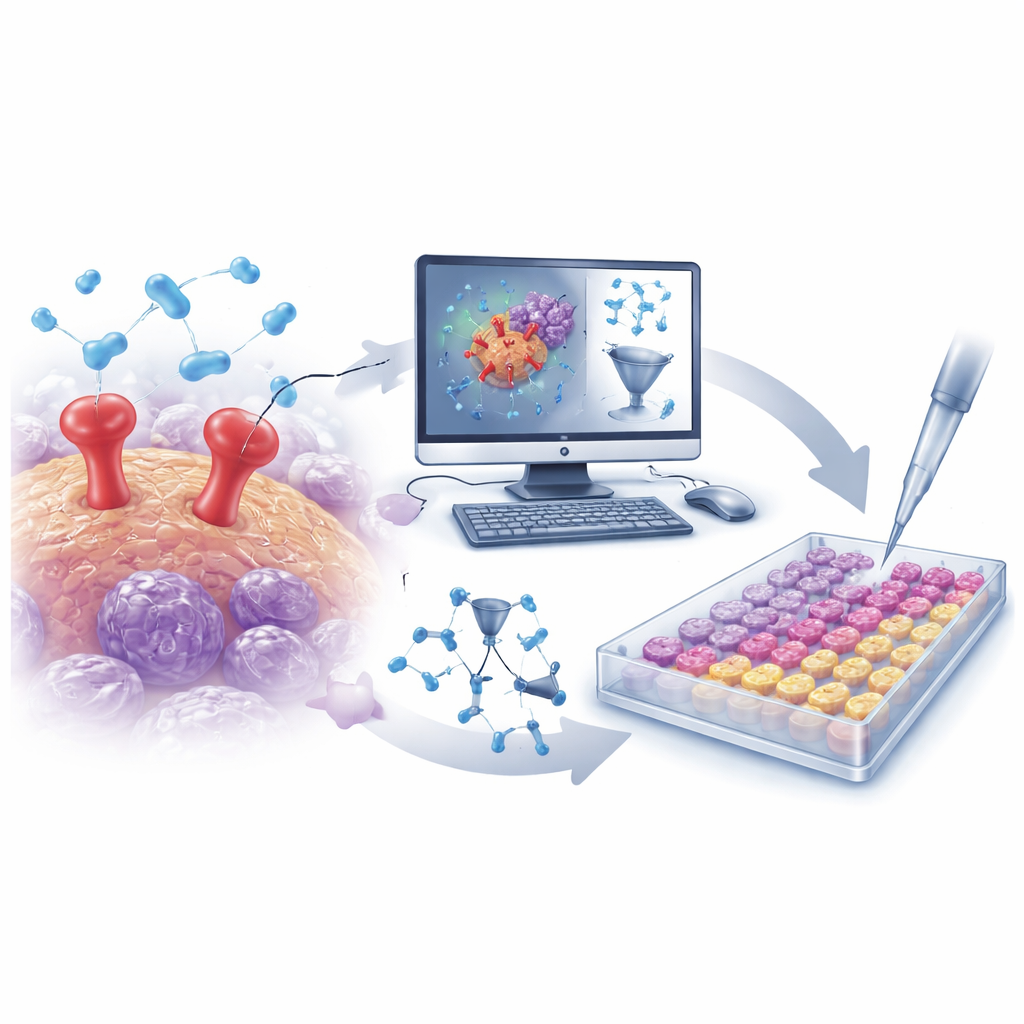
Eksploracja dużych zestawów chemicznych za pomocą inteligentnych algorytmów
Badacze rozpoczęli od zgromadzenia obszernego zbioru ponad 500 znanych molekuł blokujących uPAR z publicznej bazy danych. Struktury każdej molekuły zostały przetłumaczone na tysiące numerycznych deskryptorów opisujących cechy takie jak rozmiar, kształt, rozmieszczenie ładunku i elastyczność. Na podstawie tych danych zespół zbudował model ilościowo-strukturalnej zależności aktywności (QSAR) — rodzaj narzędzia matematycznego, które uczy się, które cechy strukturalne zwykle zwiększają aktywność jako inhibitor uPAR. Po starannej walidacji zapobiegającej przeuczeniu model wykazał wysoką zdolność przewidywania dla nieznanych związków, uwypuklając kilka kluczowych cech, które wzmacniały lub osłabiały blokowanie uPAR. Te spostrzeżenia skierowały poszukiwania nowych, lepiej zaprojektowanych molekuł.
Od skanów wirtualnych do prawdziwych probówek
Wyposażony w wytrenowany model QSAR, zespół przeprowadził wirtualne przesiewanie wyspecjalizowanej biblioteki około 30 000 molekuł ukierunkowanych na proteazy. Model szybko zawęził tę ogromną pulę do małego zestawu prawdopodobnych inhibitorów uPAR. Równolegle przeprowadzono symulacje dokowania komputerowego, aby ocenić, jak dobrze każdy kandydat może pasować do miejsca wiązania uPAR, a symulacje dynamiki molekularnej sprawdziły, czy zasymulowane kompleksy pozostaną stabilne w czasie. Z tej połączonej kampanii in silico wyłoniły się dwa wyróżniające się związki: D685‑0061, wskazany przez model QSAR jako wysoce aktywny, oraz C878‑1660, podkreślony przez dokowanie i symulacje jako tworzący szczególnie stabilne interakcje z uPAR.
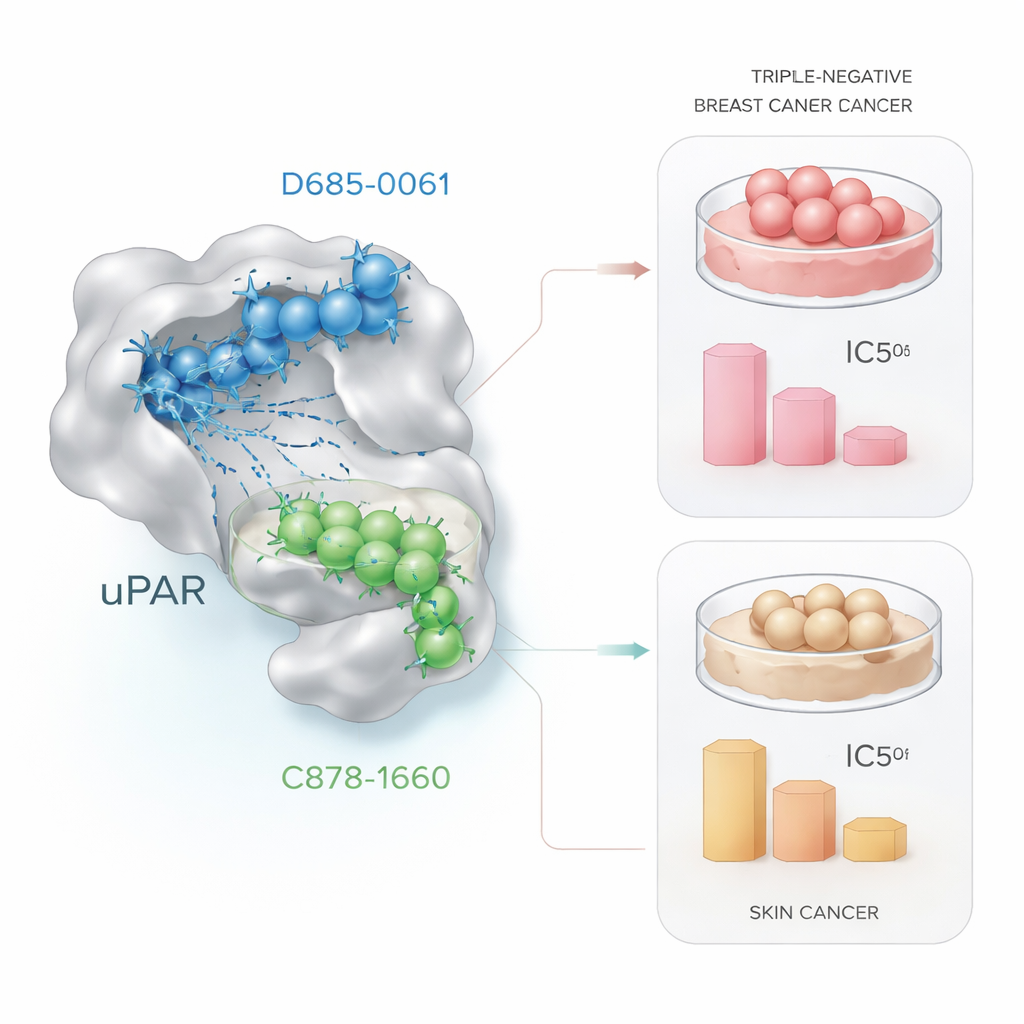
Testowanie kandydatów w komórkach nowotworowych
Obietnice obliczeń mają sens tylko wtedy, gdy przekładają się na realny efekt biologiczny. Aby to sprawdzić, badacze narażali żywe komórki nowotworowe na rosnące dawki dwóch prowadzących związków i mierzyli przeżywalność komórek za pomocą standardowej metody laboratoryjnej zwanej testem MTT. W komórkach potrójnie ujemnego raka piersi (MDA‑MB‑231) D685‑0061 zabijał komórki efektywniej, redukując żywotność o połowę przy około 21 mikromolach, podczas gdy C878‑1660 wymagał mniej więcej czterokrotnie wyższej dawki. Pod mikroskopem komórki traktowane D685‑0061 wykazywały wyraźne cechy programowanej śmierci komórkowej, takie jak zaokrąglanie się, odrywanie od podłoża i fragmentacja. Natomiast w komórkach raka skóry (A431) silniejszym zabójcą okazał się C878‑1660, osiągając 50% śmiertelność przy około 19 mikromolach wobec około 28 mikromoli dla D685‑0061, również z widocznymi uszkodzeniami zależnymi od dawki.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
Ta praca nie dostarcza natychmiastowego nowego leku, ale dostarcza dwóch obiecujących punktów wyjścia i — równie istotne — potężnego planu działania do znajdowania kolejnych. Łącząc modelowanie dużych zbiorów danych, symulacje 3D i staranne badania na komórkach, badanie pokazuje, że uPAR można selektywnie celować za pomocą małych molekuł, które uszkadzają agresywne komórki raka piersi i skóry. D685‑0061 i C878‑1660 służą teraz jako związki wiodące, które chemicy mogą modyfikować, by zwiększyć aktywność, poprawić bezpieczeństwo i właściwości farmakokinetyczne. W dłuższej perspektywie leki opracowane w oparciu o to podejście mogą pomóc zablokować rozprzestrzenianie się nowotworów napędzanych przez uPAR, przekształcając niektóre z dziś najbardziej niebezpiecznych guzów w choroby bardziej możliwe do kontrolowania.
Cytowanie: Badukle, H., Jawarkar, R.D., Shah, U. et al. From in-silico QSAR modeling to in-vitro MTT assay: experimental validation of novel uPAR leads for triple-negative breast cancer (TNBC) and skin cancer. Sci Rep 16, 5786 (2026). https://doi.org/10.1038/s41598-026-36406-4
Słowa kluczowe: inhibitory uPAR, potrójnie ujemny rak piersi, rak skóry, komputerowo wspomagane projektowanie leków, test żywotności komórek MTT