Clear Sky Science · pl
Badanie teorii funkcjonału gęstości nad adsorpcją cyklofosfamidu i purinetholu na kowalentnym framweorku triazynowym (CTF-2) do zastosowań w dostarczaniu leków
Dlaczego inteligentniejsza chemioterapia ma znaczenie
Leki chemioterapeutyczne ratują życie, ale często działają jak reflektor zamiast punktowego światła — atakując komórki zdrowe razem z nowotworowymi. Może to prowadzić do poważnych skutków ubocznych, od zmęczenia i infekcji po uszkodzenia narządów. Omawiane tu badanie bada ultracienki, wysoce porowaty materiał zwany kowalentnym framweorkiem triazynowym (CTF-2) jako „inteligentną gąbkę”, która może bezpieczniej i bardziej efektywnie przenosić dwa od dawna stosowane leki przeciwnowotworowe — cyklofosfamid i purinethol — tam, gdzie są potrzebne, a następnie uwalniać je w warunkach podobnych do guza.
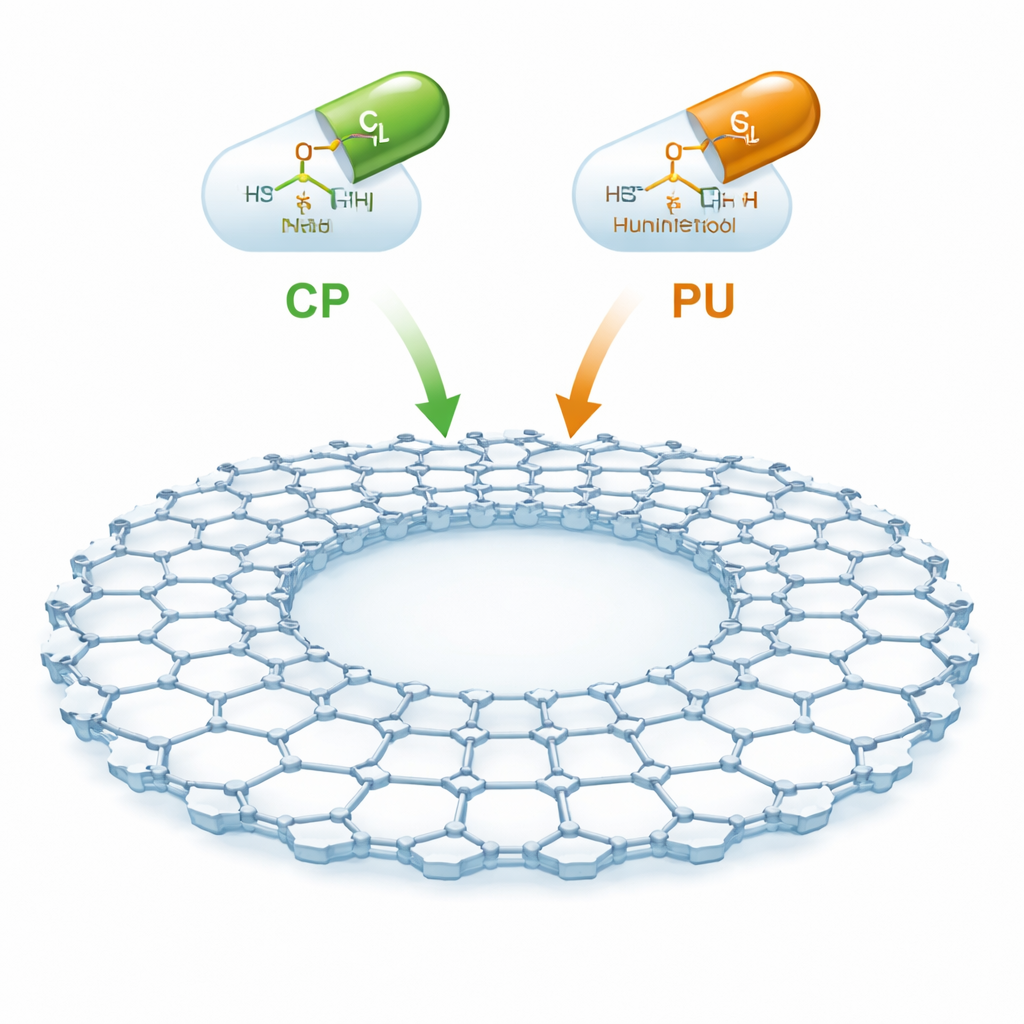
Nowy rodzaj molekularnej gąbki
CTF-2 to materiał syntetyczny zbudowany z pierścieni węgla i azotu połączonych w płaską, arkuszową sieć z dużą centralną pustką i licznymi otwartymi przestrzeniami. Ponieważ jest cienki, stabilny i pełen porów, oferuje ogromną powierzchnię wewnętrzną do wychwytywania cząsteczek leku. Autorzy skupili się na dwóch ważnych lekach przeciwnowotworowych: cyklofosfamidzie, szeroko stosowanym w nowotworach krwi i guzach litych, oraz purinetholu (znanym także jako merkaptopuryna), stosowanym przeciw białaczkom i niektórym zapalnym chorobom jelit. Pomysł polega na delikatnym zakotwiczeniu tych leków na powierzchni CTF-2, aby mogły być przenoszone przez krwiobieg i uwalniane bardziej selektywnie, ograniczając uszkodzenia tkanek zdrowych.
Badanie niewidzialnego komputerowymi eksperymentami
Zamiast pracy w laboratorium mokrym, zespół wykorzystał zaawansowane obliczenia kwantowe (teorię funkcjonału gęstości i pokrewne metody), by sprawdzić, jak mocno każdy lek wiąże się z CTF-2 i co utrzymuje te kompleksy razem. Optymalizowali kształty CTF-2 z każdym lekiem, mierzyli odległości między atomami w miejscach kontaktu i obliczali, ile energii jest zyskiwane, gdy lek przylega do framweorka. Dla cyklofosfamidu obliczona energia adsorpcji wyniosła około −1,04 elektronowolta, nieco silniej niż −0,82 elektronowolta dla purinetholu. Wartości te, które pozostają wyraźnie korzystne nawet po korektach technicznych i symulacji wody jako rozpuszczalnika, wskazują, że oba leki wiążą się wystarczająco mocno, by być załadowanymi, ale nie na tyle silnie, by nie mogły zostać później uwolnione.
Delikatne siły wykonujące ważną pracę
Badanie wykazuje, że „klejem” między lekami a CTF-2 nie jest twarde wiązanie chemiczne, lecz sieć delikatnych oddziaływań niekowalencyjnych. Korzystając ze specjalistycznych analiz gęstości elektronowej — w zasadzie map tego, gdzie znajdują się wspólne elektrony — badacze stwierdzili, że dominują przyciągania van der Waalsa (te same słabe siły, które pozwalają gekonom wspinać się po ścianach) oraz łagodne interakcje elektrostatyczne. Oddziaływania te zachodzą na krótkich, ale niewiązaniowych odległościach między atomami wodoru, azotu, tlenu, siarki i węgla w lekach i w framweorku. Dodatkowe obliczenia rozdzielające całkowite przyciąganie na poszczególne składowe potwierdziły, że siły elektrostatyczne i dyspersyjne (van der Waalsa) dostarczają większości stabilizującego przyciągania, podczas gdy siły odpychające zapobiegają zbyt głębokiemu zatopieniu leku lub nieodwracalnemu wiązaniu.
Sygnały stabilnego załadowania i regulowanego uwalniania
Zespół przeanalizował także, jak elektrony przemieszczają się, gdy leki osiadają na CTF-2, i jak to zmienia podstawowe właściwości elektryczne. Zaobserwowali małe, lecz wyraźne transfery ładunku między każdym lekiem a framweorkiem oraz lekkie zwężenie przerwy energetycznej oddzielającej wypełnione od pustych stanów elektronowych. Sugeruje to, że reaktywność i przewodność materiału są subtelnie dostrajane po załadowaniu — przydatna cecha dla przyszłych zastosowań sensorycznych lub terapii połączonej z diagnostyką. Co kluczowe, gdy zasymulowano bardziej kwaśne środowisko występujące w pobliżu guzów przez dodanie dodatkowych protonów, obliczone wiązanie osłabło, a odległości kontaktowe wzrosły. W prostych słowach, symulacje sugerują, że CTF-2 potrafi utrzymać leki w warunkach przypominających normalną krew, ale ma skłonność do łatwiejszego ich uwalniania w kwaśnych warunkach podobnych do guza — dokładnie takie zachowanie jest pożądane dla ukierunkowanego dostarczania.
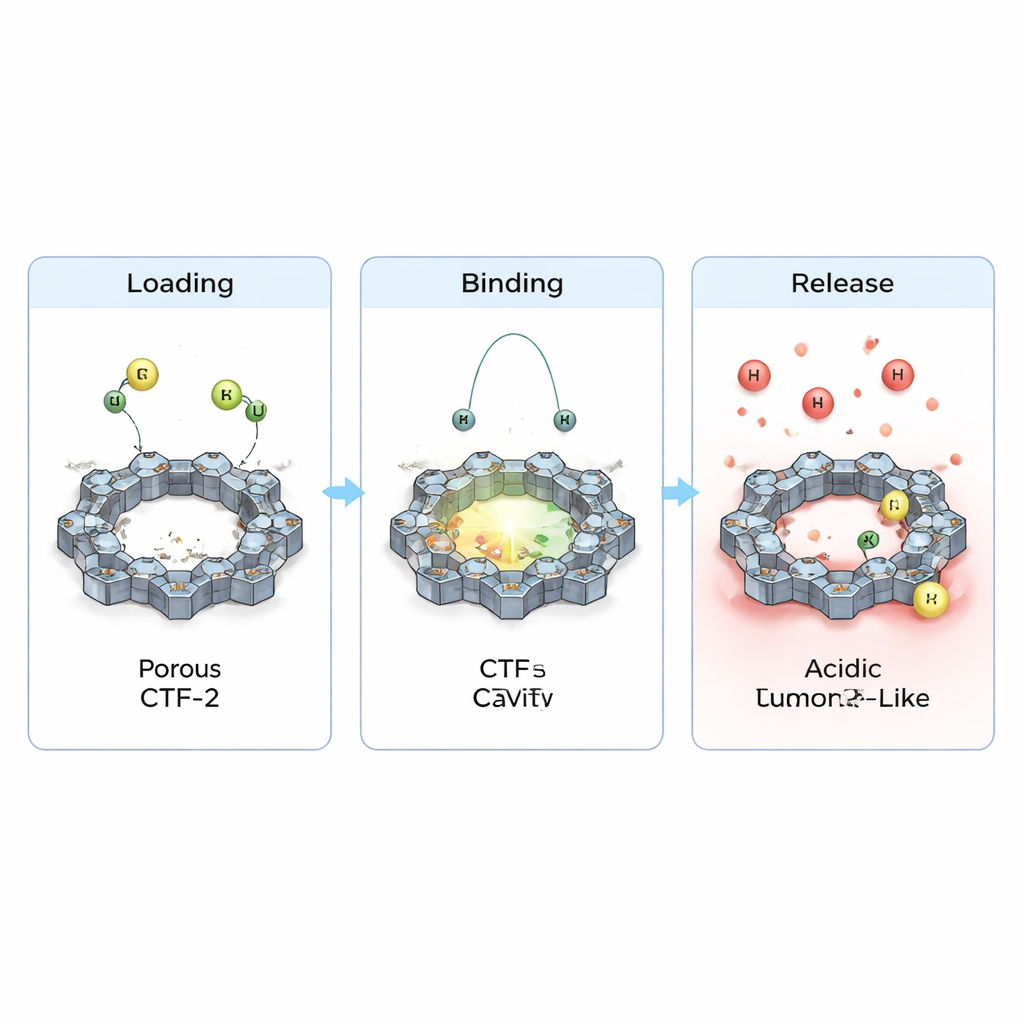
Co to oznacza dla przyszłych terapii przeciwnowotworowych
W sumie te obliczenia przedstawiają CTF-2 jako obiecujący nośnik dla cyklofosfamidu i purinetholu: może stabilnie umieścić je na swojej porowatej powierzchni, chronić podczas krążenia, a następnie uwolnić, gdy lokalna chemia wokół guza się zmieni. Chociaż praca ma charakter teoretyczny i będzie wymagać potwierdzenia eksperymentalnego, sugeruje, że starannie zaprojektowane, bogate w azot framweorki takie jak CTF-2 mogłyby pomóc przekształcić stare, ale skuteczne leki chemioterapeutyczne w inteligentniejsze środki — dostarczając silne dawki tam, gdzie są najbardziej potrzebne, przy jednoczesnym zmniejszeniu szkód ubocznych dla zdrowych komórek.
Cytowanie: Tariq, T., Yar, M., Bayach, I. et al. A density functional theory study of cyclophosphamide and purinethol adsorption on a covalent triazine framework (CTF-2) for drug delivery applications. Sci Rep 16, 6125 (2026). https://doi.org/10.1038/s41598-026-36405-5
Słowa kluczowe: nanonośnik, dostarczanie leków, chemioterapia przeciwnowotworowa, kowalenty framweork triazynowy, modelowanie obliczeniowe