Clear Sky Science · pl
Interaktywny kaskadowy system uczenia głębokiego z możliwością korekty eksperckiej do precyzyjnej segmentacji podregionów prążkowia
Dlaczego mapowanie małych obszarów mózgu ma znaczenie
Prążkowie, niewielka struktura umieszczona głęboko w mózgu, odgrywa centralną rolę w ruchu i motywacji i jest silnie dotknięte w chorobach takich jak choroba Parkinsona. Lekarze często wykorzystują badania PET i MRI do pomiaru zmian chemicznych w tym obszarze, ale prążkowie jest podzielone na wiele drobnych podregionów, które trudno dokładnie zobaczyć i obrysować. W artykule przedstawiono nową metodę wspomagania komputerowego, nazwaną StriaSeg‑iARM, która pomaga specjalistom rysować te granice dokładniej i wydajniej, nawet u osób, których mózgi są zmienione wskutek starzenia się lub choroby.
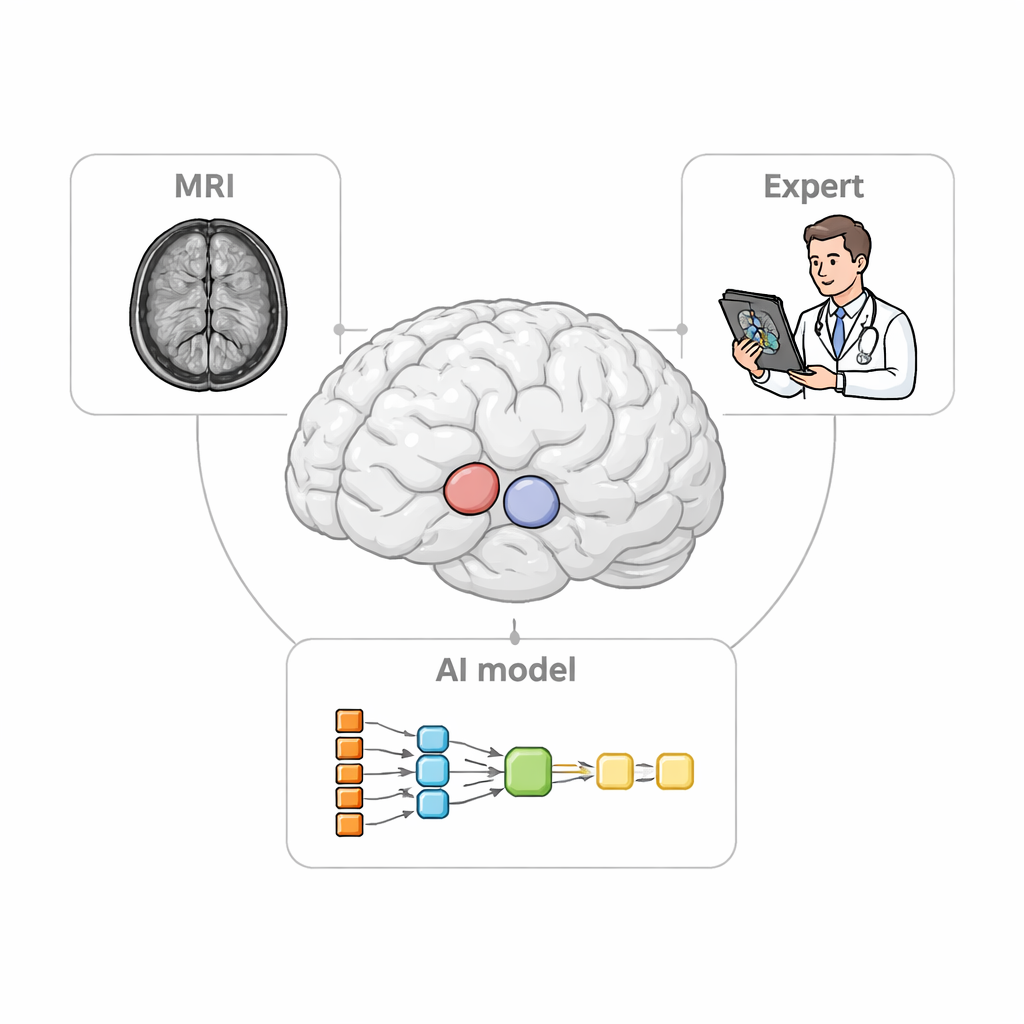
Problem kliniczny widoczny na pierwszy rzut oka
Gdy neurolodzy oceniają stany takie jak choroba Parkinsona, opierają się na skanach PET, aby śledzić, jak sygnały związane z dopaminą różnią się w poszczególnych częściach prążkowia. Aby zrobić to poprawnie, najpierw trzeba zdefiniować małe trójwymiarowe „obszary zainteresowania” na MRI, które służą jako miarki dla danych PET. Ręczne obrysowywanie tych obszarów jest pracochłonne, nużące i może się różnić w zależności od eksperta. Istniejące oprogramowanie potrafi automatycznie odnaleźć tylko większe struktury i często ma problemy u pacjentów z mózgami pomniejszonymi lub zdeformowanymi — co jest powszechne w zaawansowanych chorobach neurodegeneracyjnych. Te ograniczenia mogą zniekształcać rzeczywisty wzorzec uszkodzeń i osłabiać wartość diagnostyczną obrazowania.
Mądrzejszy asystent w dwóch krokach
Naukowcy zaprojektowali StriaSeg‑iARM jako dwustopniowy system uczenia głębokiego, który działa bezpośrednio w przestrzeni mózgu konkretnej osoby, zamiast wymuszać dopasowanie skanu do standardowego szablonu. W pierwszym etapie program lokalizuje ogólne prążkowie na trójwymiarowym MR. W drugim etapie dzieli tę strukturę na 12 anatomicznie zdefiniowanych podregionów po obu stronach mózgu. Między tymi dwoma etapami znajduje się kluczowa innowacja: krok interaktywny, w którym ekspert może szybko sprawdzić i, w razie potrzeby, poprawić zgrubny obrys wygenerowany w pierwszym etapie, zanim zostanie wykonane drobniejsze podzielenie. To podejście łączy szybkość automatyzacji z osądem wytrenowanego obserwatora ludzkiego.
Szkolenie i testy na rzeczywistych mózgach
Aby nauczyć system, czego ma szukać, zespół zgromadził setki skanów MRI z wielu szpitali i różnych typów skanerów oraz przygotował staranne ręczne obrysy 12 podregionów prążkowia. Następnie przetestowali model na dwóch zewnętrznych zestawach danych zawierających zarówno MRI, jak i PET związane z dopaminą: jednym z pacjentami we względnie wczesnym stadium choroby Parkinsona i zdrowymi ochotnikami, a drugim z starszą, poważniej dotkniętą grupą kliniczną z wyraźnym skurczeniem mózgu i mieszanymi diagnozami. W tych wymagających przypadkach StriaSeg‑iARM konsekwentnie lepiej dopasowywał się do ręcznych obrysów ekspertów niż tradycyjne metody oparte na atlasie oraz prostszy jednofazowy model uczenia głębokiego — osiągając większe nakładanie się, bardziej precyzyjne granice i stabilne pomiary objętości.
Bardziej precyzyjne pomiary dla skanów chemii mózgu
Ponieważ celem końcowym jest ilościowe określanie sygnałów PET, autorzy sprawdzili także, jak różne metody segmentacji wpływają na odczyty PET. Używając standardowej miary wiązania znacznika w każdym podregionie, porównali wyniki automatyczne z tymi opartymi na ręcznych obrysach. Metoda atlasowa miała tendencję do niedoszacowywania wiązania, zwłaszcza u pacjentów z poważniejszymi zmianami, podczas gdy podstawowy model uczenia głębokiego wciąż wykazywał zauważalne odchylenia w niektórych regionach. W przeciwieństwie do tego modele kaskadowe — szczególnie gdy zastosowano krok interaktywnej korekty — generowały wartości PET ściśle odzwierciedlające referencję ekspercką, z minimalnym uprzedzeniem i rozrzutem. Zespół wykazał ponadto, że prosty współczynnik niepewności z pierwszego etapu potrafi wskazać około jednej czwartej najtrudniejszych przypadków, gdzie korekta ekspercka jest naprawdę potrzebna, pozostawiając resztę w pełni automatyczną.
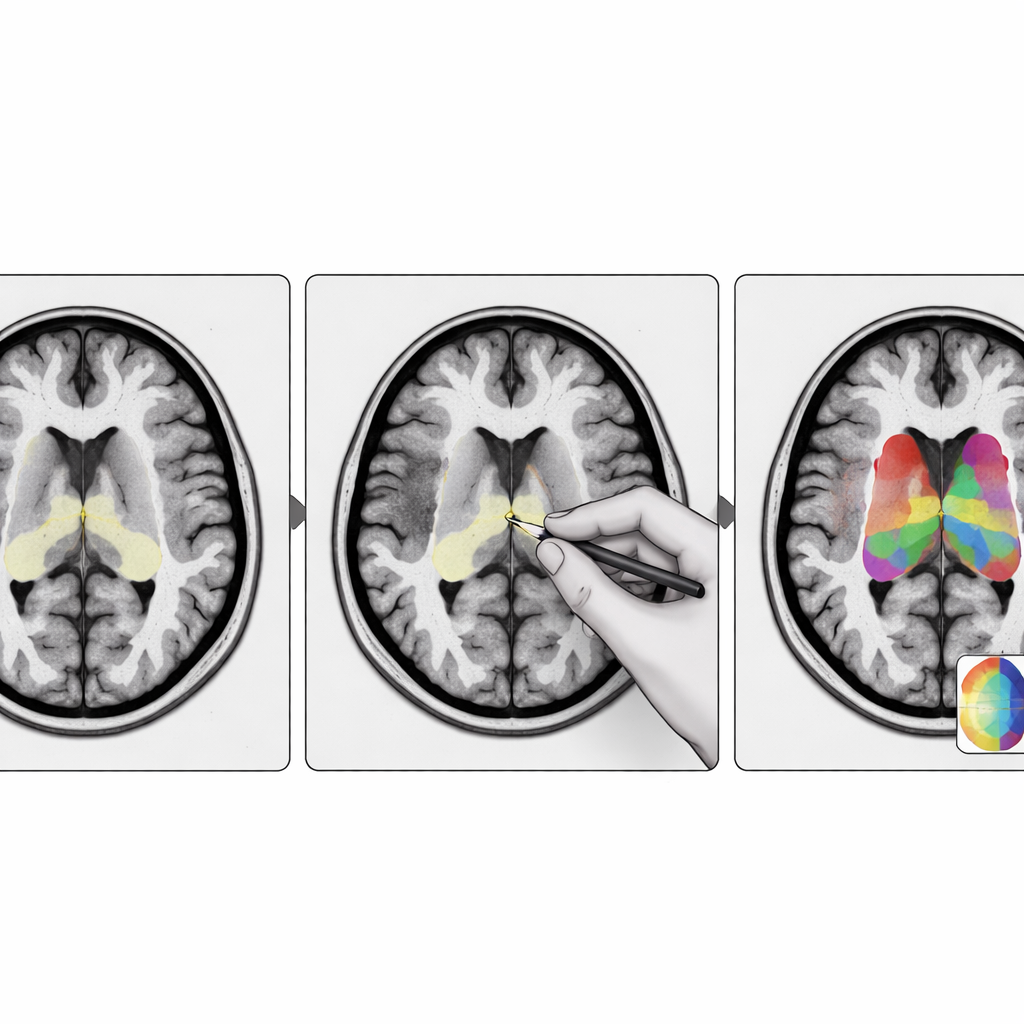
Co to oznacza dla pacjentów i klinicystów
Dla osób niebędących specjalistami najważniejszy wniosek jest taki, że lepsze cyfrowe mapy małych obszarów mózgu mogą uczynić skany chemiczne mózgu bardziej wiarygodnymi. StriaSeg‑iARM dostarcza elastyczne ramy, w których model uczenia głębokiego wykonuje większość pracy, ale specjaliści mogą wciąż włączyć się, by poprawić trudne przypadki bez konieczności retrainingu systemu. To połączenie automatyzacji i nadzoru eksperckiego podnosi precyzję pomiarów używanych do diagnozowania i monitorowania zaburzeń takich jak choroba Parkinsona i może zostać zaadaptowane do innych narządów i chorób, gdzie małe, trudne do zauważenia struktury kryją istotne wskazówki.
Cytowanie: Kim, J., Kim, D., Kim, S. et al. An interactive cascaded deep learning framework with expert refinement for accurate striatal subregion segmentation. Sci Rep 16, 6550 (2026). https://doi.org/10.1038/s41598-026-36399-0
Słowa kluczowe: obrazowanie w chorobie Parkinsona, segmentacja prążkowia, uczenie głębokie w radiologii, MRI PET mózgu, biomarkery neurodegeneracyjne