Clear Sky Science · pl
Szczep Staphylococcus capitis produkujący dwa bakteriocyny, capidermicin i micrococcin P1, wykazuje szerokie spektrum aktywności antybakteryjnej
Dlaczego drobne bakterie skórne mają znaczenie w kontekście superbakteryjnych zagrożeń
Infekcje odporne na antybiotyki rosną na całym świecie, a lekarze mają coraz mniej skutecznych leków. Jednym z obiecujących pomysłów jest wykorzystanie naszych „dobrych” mikrobów do walki z patogenami. To badanie koncentruje się na pospolitej bakterii skóry, Staphylococcus capitis, i pokazuje, że konkretny szczep, oznaczony HBC3, naturalnie wytwarza dwie silne molekuły zabijające drobnoustroje. Wspólnie te substancje potrafią tłumić niebezpieczne szpitalne patogeny, w tym metycylinooporny Staphylococcus aureus (MRSA), co sugeruje, że przyjazne bakterie skóry same w sobie mogą stać się przyszłymi narzędziami przeciw zakażeniom.
Rezydent skóry z ukrytą siłą
S. capitis zwykle spokojnie zasiedla naszą skórę, zwłaszcza skórę głowy, i na ogół nie szkodzi. Naukowcy przebadali 18 szczepów S. capitis pobranych z nosa, by sprawdzić, czy któryś z nich hamuje MRSA, główną przyczynę trudnych do leczenia zakażeń. Jeden szczep, HBC3, wyróżnił się. W testach laboratoryjnych silnie tłumił szeroką gamę bakterii Gram-dodatnich, w tym MRSA, enterokoki oporne na wankomycynę (VRE), Streptococcus pyogenes, Listeria monocytogenes oraz gatunki Bacillus i Clostridium wywołujące poważne choroby. Co warte odnotowania, nie wykazywał działania wobec kilku powszechnych bakterii Gram-ujemnych, takich jak Escherichia coli i Klebsiella pneumoniae, co sugeruje ukierunkowane, a nie bezwzględne zabijanie.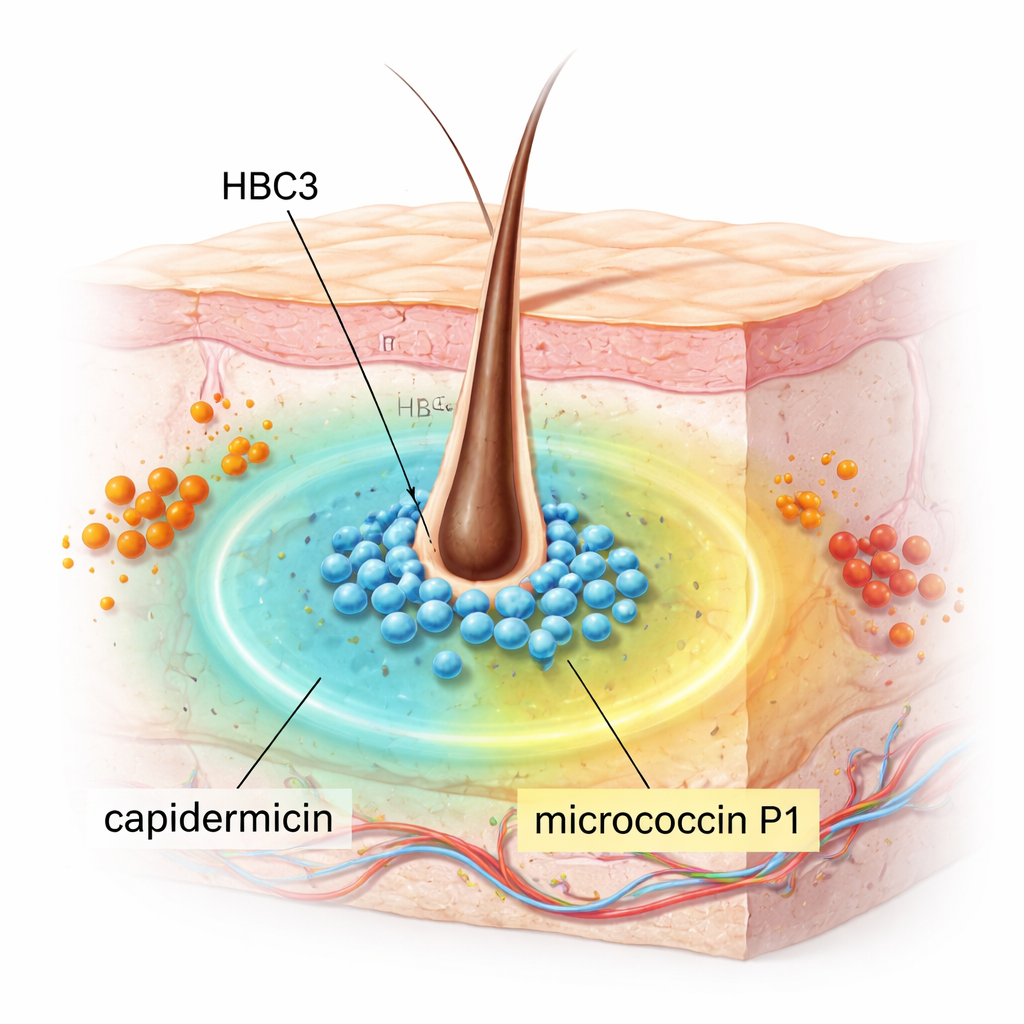
Dwa naturalne antybiotyki na jednym genetycznym „mini-chromosomie”
Aby odkryć, jak HBC3 osiąga ten szeroki efekt antymikrobowy, zespół rozszyfrował cały jego genom. Zidentyfikowali mały kolisty element DNA — plazmid nazwany pHBC3_1 — który zawiera komplet instrukcji do wytwarzania dwóch różnych bakteriocynów — naturalnych peptydów o działaniu zbliżonym do antybiotyków, produkowanych przez bakterie. Jednym z nich jest capidermicin, mały dodatnio naładowany peptyd wcześniej opisany w innych szczepach S. capitis. Drugim jest micrococcin P1 (MP1), tiopeptyd blokujący syntezę białek u bakterii docelowych, wcześniej nieopisywany w S. capitis. Gdy plazmid został usunięty z HBC3, szczep całkowicie utracił aktywność antybakteryjną, co potwierdza, że te geny są niezbędne dla jego zdolności obronnych.
Różne cele, wspólny cel
Poprzez oczyszczenie każdego bakteriocynu osobno, naukowcy przetestowali, jak skutecznie hamują różne drobnoustroje. MP1 wykazał szerokie i silne działanie wobec wielu Gram-dodatnich ziarniaków, w tym MRSA i enterokoków, przy niskich stężeniach. Capidermicin natomiast był najskuteczniejszy wobec Gram-dodatnich pałeczek, takich jak Bacillus coagulans i Listeria, ale przy warunkach użytych w badaniu miał słabe lub żadne działanie wobec gronkowców. Gdy zespół zastosował oba peptydy razem przeciwko B. coagulans, zaobserwowano efekt addytywny: niższe dawki w połączeniu osiągnęły silniejsze zahamowanie wzrostu niż każda substancja osobno. To komplementarne celowanie pozwala HBC3 tłumić szersze spektrum rywali, stosując dwie różne molekularne bronie dostosowane do różnych kształtów komórek i powierzchni bakteryjnych. 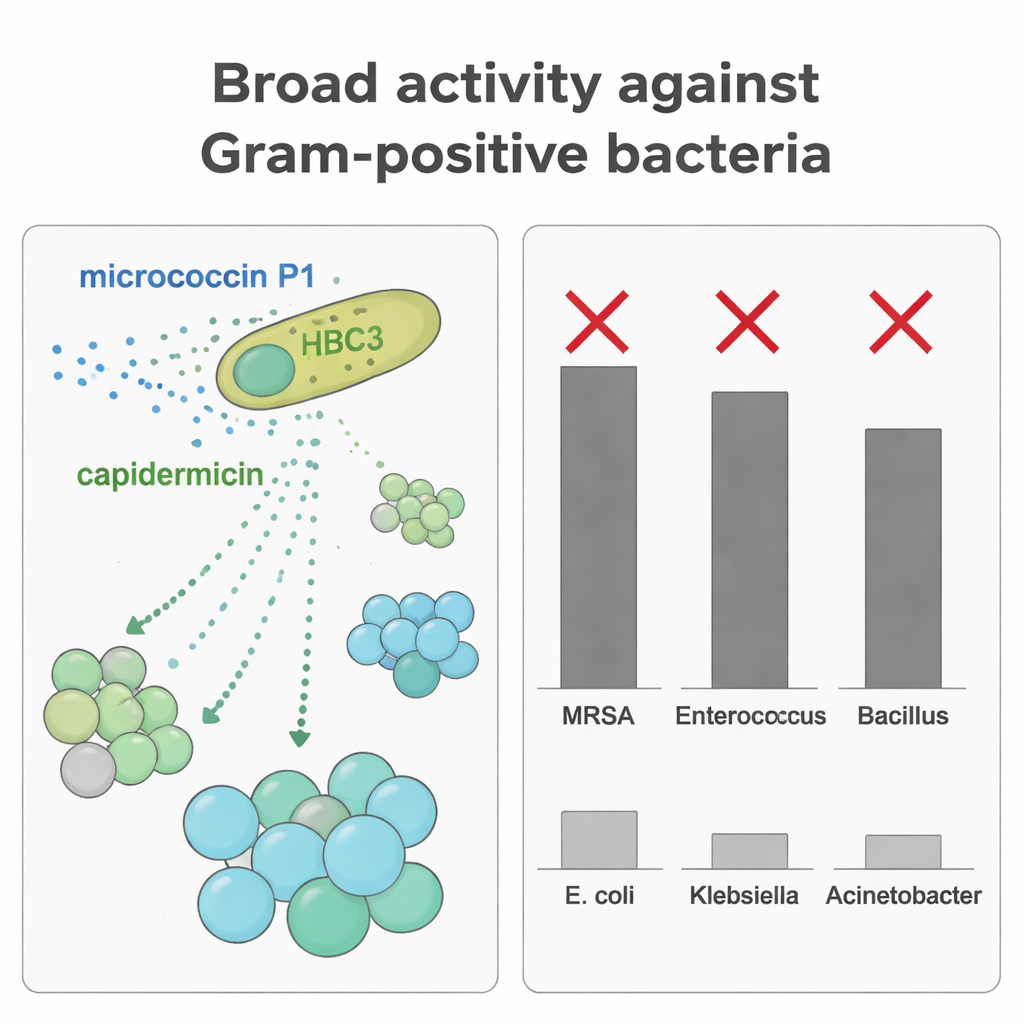
Wygrywanie przestrzeni w zatłoczonych mikrobnych sąsiedztwach
Aby odtworzyć rywalizację w warunkach zbliżonych do naturalnych, badacze współhodowali HBC3 z MRSA, VRE i B. coagulans na tych samych płytkach. Normalny szczep HBC3 niemal całkowicie wyeliminował te patogeny z mieszaniny, podczas gdy wersja pozbawiona plazmidu pozwalała im rozkwitać. Porównania genetyczne sugerują, że plazmid z dwoma bakteriocynami najprawdopodobniej powstał w wyniku przeszłej fuzji i przemieszania osobnych plazmidów, ułatwionej przez ruchome elementy DNA, które mogą przenosić klastry genów między bakteriami. Ten złożony plazmid daje HBC3 wyraźną przewagę w zatłoczonych środowiskach, takich jak skóra czy błony śluzowe, gdzie wiele mikroorganizmów konkuruje o składniki odżywcze i przestrzeń.
Od sprzymierzeńca skóry do potencjalnego probiotyku?
Badanie konkluduje, że S. capitis HBC3 jest wyposażony w rzadkie połączenie dwóch odmiennych bakteriocyn na jednym plazmidzie, co pozwala mu silnie hamować wiele klinicznie istotnych patogenów Gram-dodatnich, w tym szczepy odporne na antybiotyki. Ponieważ sam HBC3 nie należy do znanej linii wysokiego ryzyka i nie wykazuje wykrywalnych genów oporności na leki, może być kandydatem do rozwoju jako ukierunkowany probiotyk lub czynnik dekontaminujący — zaprojektowany na przykład do selektywnego ograniczania S. aureus na skórze lub w nosie przy jednoczesnym oszczędzaniu bardziej nieszkodliwych sąsiadów. Zanim takie zastosowania staną się rzeczywistością, konieczne będą staranne testy bezpieczeństwa, skuteczności u zwierząt i ludzi oraz długoterminowego wpływu na normalną mikrobiotę, ale praca podkreśla, że nasze własne mikroby mogą pomóc przeciwdziałać trwającemu kryzysowi superbakteryjnego zagrożenia.
Cytowanie: Ohdan, K., Suzuki, Y., Kawada-Matsuo, M. et al. Staphylococcus capitis strain producing dual bacteriocins, capidermicin and micrococcin P1, shows broad-spectrum antimicrobial activity. Sci Rep 16, 6835 (2026). https://doi.org/10.1038/s41598-026-36393-6
Słowa kluczowe: bakteriocyny, Staphylococcus capitis, micrococcin P1, capidermicin, oporność na antybiotyki