Clear Sky Science · pl
Wdrożenie podejścia wysokoprzepustowego przesiewania wirtualnego (HTVS) do identyfikacji nowych inhibitorów dehydrogenazy mleczanowej (LDH) o właściwościach przeciwnowotworowych
Dlaczego te badania mają znaczenie dla leczenia raka
Komórki nowotworowe często przebudowują sposoby pozyskiwania energii, a tę zmianę można wykorzystać do zaprojektowania bardziej inteligentnych i selektywnych leków. W badaniu zbadano kluczowy enzym metaboliczny — dehydrogenazę mleczanową (LDH), która pomaga guzom przetrwać w trudnych warunkach i opierać się terapiom. Dzięki zaawansowanym metodom komputerowym i testom laboratoryjnym badacze zidentyfikowali dwa nowe małe związki blokujące LDH, które wykazują obiecujące działanie przeciwnowotworowe w liniach komórkowych raka prostaty.
Dziwny metabolizm komórek nowotworowych
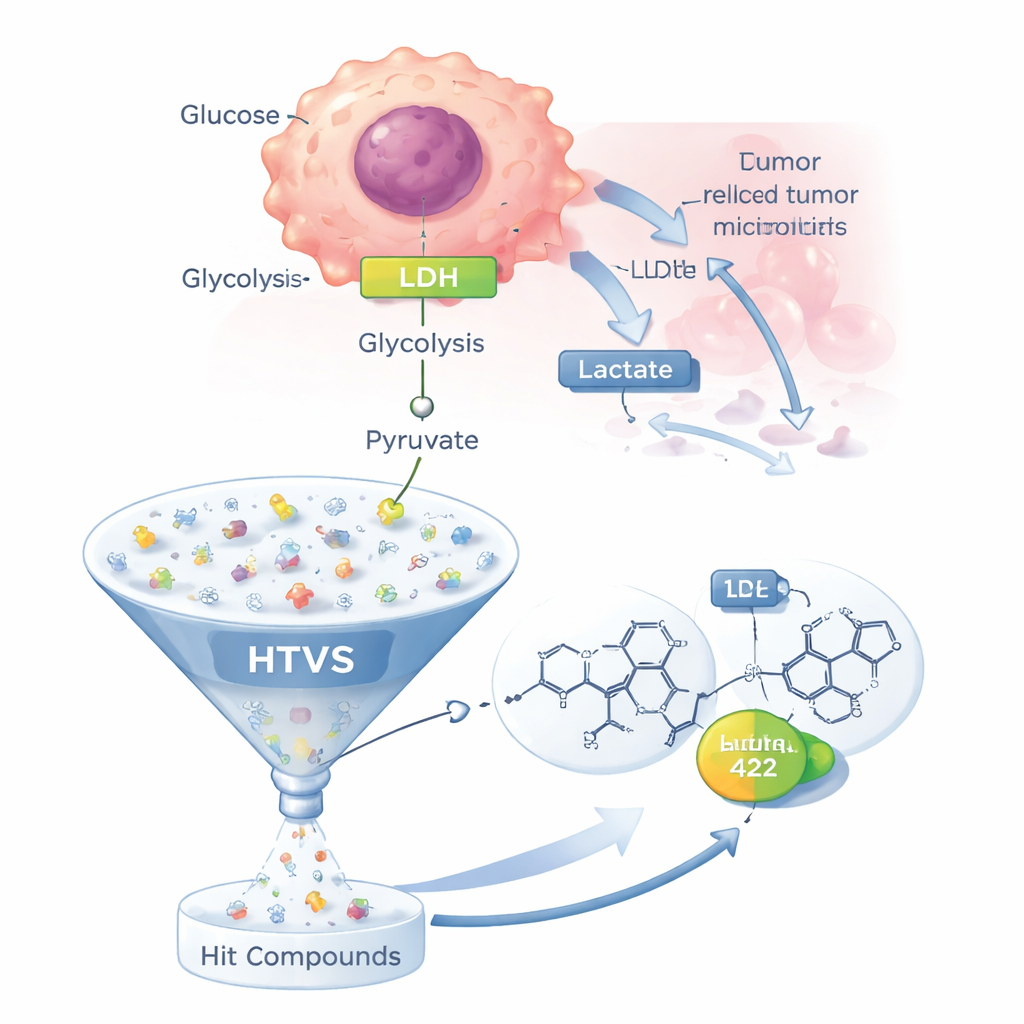
Większość zdrowych komórek efektywnie wykorzystuje tlen w mitochondriach do wytwarzania energii. Wiele komórek nowotworowych jednak polega w dużej mierze na mniej wydajnej ścieżce zwanej glikolizą, nawet gdy tlenu jest pod dostatkiem — zjawisko znane jako efekt Warburga. W tej skróconej ścieżce glukoza rozkładana jest do pirogronianu, który następnie zamiast trafiać do mitochondriów przekształcany jest przez LDH w mleczan. Mleczan jest wypompowywany z komórki, zakwaszając otoczenie guza, co pomaga komórkom nowotworowym unikać śmierci komórkowej, osłabiać atak immunologiczny i osłabiać efekty wielu leków chemioterapeutycznych. Ponieważ LDH leży w centrum tej zmienionej gospodarki metabolicznej, a żaden lek celujący LDH nie został jeszcze zatwierdzony, stał się on priorytetowym celem dla nowych terapii przeciwnowotworowych.
Wykorzystanie komputerów do przesiania pół miliona cząsteczek
Zamiast testować potencjalne leki pojedynczo w laboratorium, zespół zastosował strategię wysokoprzepustowego przesiewania wirtualnego (HTVS). Rozpoczęli od 28 związków blokujących LDH opisanych w literaturze i wyodrębnili z nich „farmakofor” — abstrakcyjny, trójwymiarowy wzorzec cech, który prawdopodobnie dzielą dobre inhibitory LDH. Następnie zastosowali ten model do komercyjnej biblioteki około 500 000 związków o własnościach zbliżonych do leków, pytając, które kandydaty pasują do kluczowych cech. Około 110 000 cząsteczek przeszło ten pierwszy filtr, a dalszy wybór oparty na standardowych zasadach „podobieństwa do leku” zmniejszył listę do 2 337 bardziej realistycznych kandydatów do dokowania w enzymie LDH.
Przybliżenie się do najlepszych wiążących
Następnym krokiem było oszacowanie, jak silnie te kandydaty mogą wpasować się w miejsce aktywne LDH. Przy użyciu kilku poziomów dokowania komputerowego badacze obliczyli, jak każda cząsteczka może wchodzić w interakcje ze specyficznymi aminokwasami we wnęce enzymu. Ten wieloetapowy proces stopniowo zawęził pulę z tysięcy kandydatów do zaledwie 59 obiecujących cząsteczek, a następnie do pięciu wyraźnych „trafień” o szczególnie silnie przewidywanym wiązaniu. Dwa z nich, oznaczone jako związki 15 i 422, wyróżniały się, ponieważ symulacje dynamiki molekularnej sugerowały, że tworzą one wyjątkowo stabilne kompleksy z LDH w czasie, utrzymując kluczowe kontakty z krytycznymi resztami w miejscu aktywnym przy zachowaniu rozsądnej ogólnej struktury białka.
Z przesiewu do żywych komórek nowotworowych
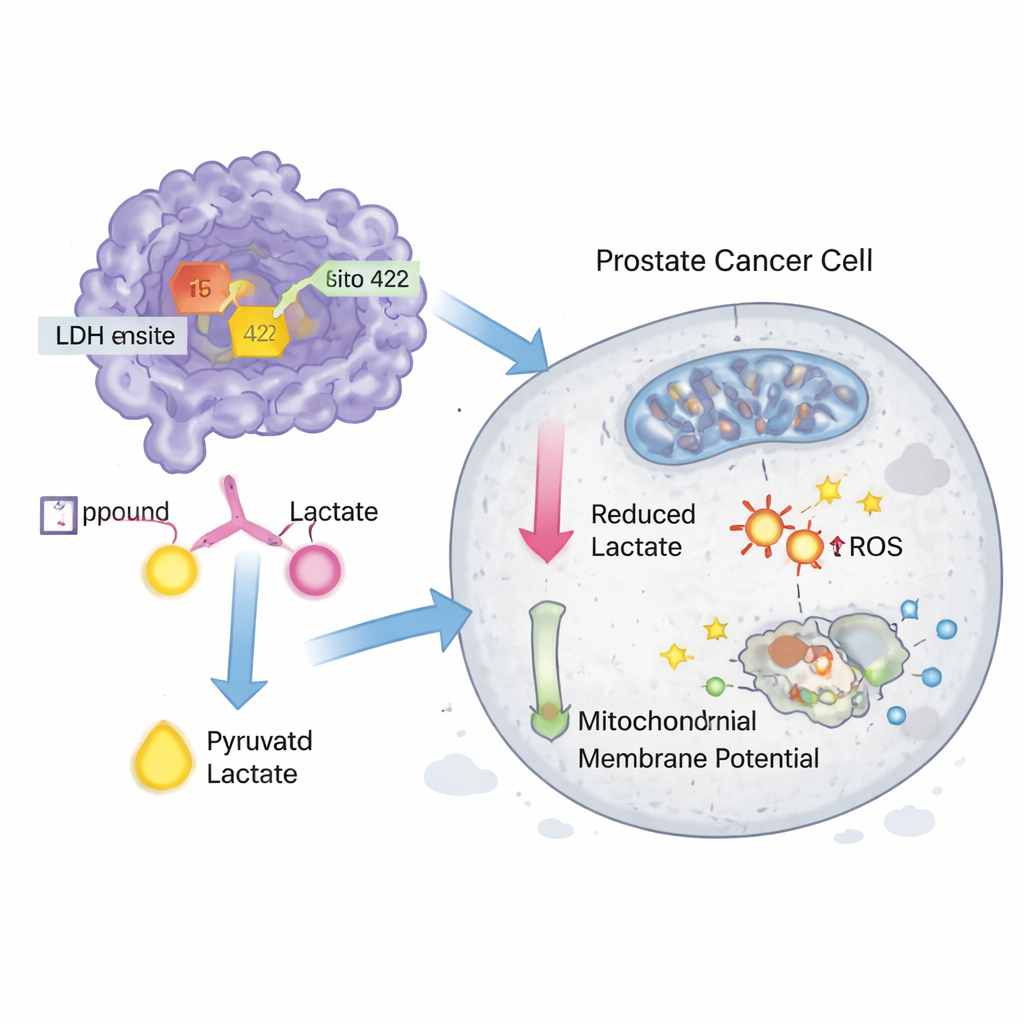
Aby sprawdzić, czy te trafienia mają znaczenie w systemach żywych, naukowcy zakupili związki 15 i 422 i przetestowali je w liniach komórek raka prostaty DU-145 i PC-3. Oba związki hamowały aktywność LDH w komórkach w stężeniach nanomolowych i również bezpośrednio spowalniały aktywność oczyszczonego enzymu LDH, chociaż były nieco mniej silne niż znany eksperymentalny inhibitor GNE‑140. W testach proliferacji związki zmniejszały przeżywalność komórek nowotworowych przy niskich stężeniach mikromolowych, ponownie zbliżając się do wydajności GNE‑140. Dodatkowe eksperymenty wykazały, że leczenie nieznacznie zwiększa stres oksydacyjny, zakłóca potencjał błony mitochondrium — znak uszkodzenia „fabryk energii” — oraz wywołuje zaprogramowaną śmierć komórkową (apoptozę) w komórkach DU‑145, przy czym związek 15 był z tych dwóch bardziej aktywny.
Co to może znaczyć dla przyszłych leków przeciwnowotworowych
Chociaż te cząsteczki nie są gotowymi lekami, stanowią wartościowe punkty wyjścia do projektowania leków. Zarówno związki 15, jak i 422 mają właściwości chemiczne sugerujące lepszą rozpuszczalność, przepuszczalność i ogólne „podobieństwo do leku” niż niektóre istniejące inhibitory LDH, co czyni je atrakcyjnymi kandydatami do dalszej optymalizacji. Badanie pokazuje, jak szeroko zakrojone przesiewanie komputerowe, prowadzone na podstawie znanych cech strukturalnych, może odkryć nowe inhibitory LDH, które osłabiają komórki nowotworowe poprzez odcięcie ich zmienionego źródła energii. Przy dalszych pracach nad ulepszeniem struktur, dokładniejszym potwierdzeniu bezpośredniego wiązania i badaniach in vivo, związki te mogą przyczynić się do powstania nowej klasy środków przeciwnowotworowych atakujących guzy przez ich unikatowe podatności metaboliczne.
Cytowanie: Huang, Y., Benni, S., Yadav, U.P. et al. Deploying the high-throughput virtual screening (HTVS) approach for the identification of new lactate dehydrogenase (LDH) inhibitors with anticancer assets. Sci Rep 16, 5921 (2026). https://doi.org/10.1038/s41598-026-36385-6
Słowa kluczowe: inhibitory dehydrogenazy mleczanowej, metabolizm nowotworów, przesiewanie wirtualne, rak prostaty, odkrywanie leków przeciwnowotworowych