Clear Sky Science · pl
Nadmierna ekspresja MGMT pośredniczy w oporności na temozolomid wynikającej z zależności od USP5
Dlaczego niektóre guzy mózgu przestają reagować na kluczowy lek
Dla osób z agresywnym rakiem mózgu — glejakiem wielopostaciowym — jednym z głównych leków stosowanych przez lekarzy jest temozolomid. Początkowo chemioterapia ta może spowolnić rozwój choroby, ale guzy często uczą się, jak się jej oprzeć. Badanie to stawia praktyczne pytanie o konsekwencjach życia i śmierci: co dokładnie pozwala komórkom nowotworowym wymknąć się działaniu leku i czy można znaleźć nowe słabe punkty, aby leczenie znów stało się skuteczne?
Lek, który pomaga na początku, potem traci skuteczność
Temozolomid działa przez uszkadzanie DNA szybko dzielących się komórek nowotworowych, zmuszając je do śmierci. Jednak wiele glejaków wytwarza białko naprawcze MGMT, które potrafi cofnąć te uszkodzenia. Pacjenci, których guzy włączają MGMT, zwykle mają gorsze rokowanie, ponieważ efekt leku jest niwelowany. Lekarze częściowo przewidują odpowiedź, sprawdzając, czy gen MGMT jest chemicznie wyłączony (metylowany) czy włączony (niemetylowany), ale to nie wyjaśnia w pełni, dlaczego rozwija się oporność ani jak poziomy MGMT pozostają wysokie w komórkach guza przez czas.
Ukryci pomocnicy, którzy chronią białko naprawcze
Autorzy przyjrzeli się innemu poziomowi kontroli: molekularnym „załogom sprzątającym”, które decydują, które białka są niszczone, a które oszczędzane. Komórki zwykle znakują zużyte białka do degradacji, podczas gdy grupa enzymów zwanych deubikwitynującymi (DUB) może uratować białka przed tym losem. Przez analizę dużych publicznych baz danych onkologicznych i badanie linii komórkowych glejaka opornych na lek hodowanych w laboratorium, zespół skupił się na dwóch takich enzymach, USP5 i USP8. W próbkach guzów od setek pacjentów wyższe poziomy USP5 zwykle współwystępowały z podwyższonym MGMT, a pacjenci, których guzy miały oba geny o wysokiej ekspresji, generalnie umierali wcześniej.
Budowanie oporności w laboratorium
Aby naśladować to, co dzieje się u pacjentów, badacze powoli eksponowali dwie powszechne linie komórkowe glejaka na rosnące dawki temozolomidu, aż komórki stały się oporne. W tych zahartowanych komórkach wzrosło kilka DUB, ale USP5, USP8, USP10 i białko naprawcze MGMT były szczególnie podwyższone. Gdy zespół użył małych cząsteczek RNA do wyciszenia USP5 lub USP8, oporne komórki nagle stały się wrażliwe: aktywowały programy autodestrukcji, w tym apoptozę i formę stresowo wywołanej autodegradacji zwanej autofagią. Jednocześnie poziomy MGMT gwałtownie spadły, a inne białko powiązane z opornością, USP10, również się obniżyło, co sugeruje, że te enzymy zajmują uprzywilejowaną pozycję w sieci przetrwania.
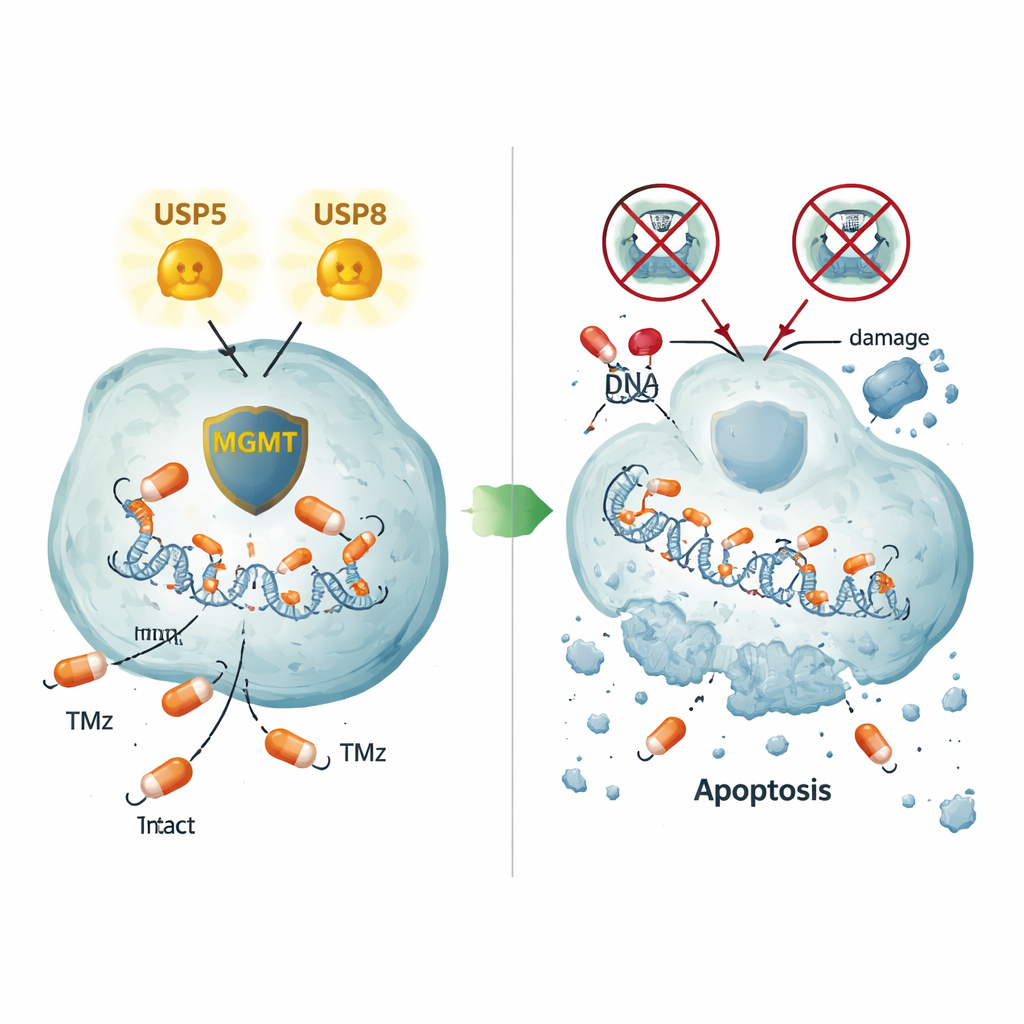
Dwa różne sposoby utrzymania MGMT przy życiu
Szczegółowe obrazowanie komórek guza i ludzkiej tkanki nowotworowej pokazało, że USP5 i MGMT często występują razem w tych samych rejonach komórki, szczególnie w cytoplazmie. Zablokowanie USP5 obniżało nie tylko poziom MGMT, lecz także powodowało jego rozkład przez maszynerię rozdrabniającą białka w komórce — proces, który dało się odwrócić za pomocą bortezomibu, leku blokującego proteasom. Nadprodukcja USP5 w komórkach, które normalnie nie wykazywały MGMT, wystarczyła, by podnieść poziomy białka MGMT, nawet w linii komórkowej niezwiązanej z mózgiem, potwierdzając bezpośredni efekt stabilizujący. USP8 okazał się działać inaczej: jego wyciszenie również obniżało MGMT, ale bez zmiany poziomu USP5, co ujawnia drugi, niezależny od USP5 mechanizm pomagający utrzymać MGMT. Nawet w linii opornej, która w ogóle nie produkowała MGMT, wyłączenie USP5 lub USP8 wywołało rozległą śmierć komórek, wskazując na dodatkowe ścieżki oporności kontrolowane przez te enzymy.
Powiązania z układem odpornościowym i nowe pomysły terapeutyczne
Poza opornością na lek, badanie łączy USP5 z interakcją glejaka z układem odpornościowym. Analiza danych genomowych sugerowała, że zmiany poziomów i kopii genu USP5 przesuwają równowagę różnych komórek odpornościowych wokół guza, w tym cytotoksycznych limfocytów T i komórek regulatorowych T. Wcześniejsze prace wykazały też, że USP5 może stabilizować PD‑L1, białko, którego guzy używają do wyłączania atakujących limfocytów T. Razem te ustalenia sugerują, że USP5 może pomagać guzom zarówno przetrwać chemioterapię, jak i unikać ataku odpornościowego, co czyni go szczególnie atrakcyjnym celem terapeutycznym.
Co to oznacza dla przyszłego leczenia nowotworów mózgu
Mówiąc prosto, praca ta identyfikuje USP5 i USP8 jako kluczowych ochroniarzy, którzy chronią białko naprawcze MGMT i pomagają komórkom glejaka opierać się temozolomidowi. Demontując tych ochroniarzy, autorzy byli w stanie zniszczyć komórki oporne na lek w laboratorium i obniżyć poziomy MGMT, nawet w przypadkach, gdy oporność oparta na MGMT nie była jedynym problemem. To daje nadzieję, że przyszłe leki ukierunkowane na USP5 lub USP8, być może w połączeniu z istniejącą chemioterapią i terapiami immunologicznymi, mogłyby przywrócić wrażliwość uporczywych guzów mózgu i dać pacjentom więcej czasu.
Cytowanie: Bhardwaj, S., Sanjay, Sharma, D. et al. MGMT upregulation mediates Temozolomide resistance conferred USP5 dependency. Sci Rep 16, 6118 (2026). https://doi.org/10.1038/s41598-026-36379-4
Słowa kluczowe: glejak, oporność na temozolomid, MGMT, USP5, enzymy deubikwitynujące