Clear Sky Science · pl
Wzajemna, kooperacyjna bramka łącząca SqueezeNet i ShuffleNetV2 do wykrywania raka piersi na obrazach histopatologicznych
Inteligentniejsze wsparcie diagnostyki raka piersi
Gdy w piersi wykryje się guz, lekarze często polegają na cienkich plastrach tkanki, wybarwionych i oglądanych pod mikroskopem, aby zdecydować, czy komórki są niegroźne, czy złośliwe. Ta uważna inspekcja jest złotym standardem diagnostyki, ale jest powolna, pracochłonna i może się różnić między specjalistami. Opisane badanie przedstawia narzędzie komputerowe analizujące takie obrazy mikroskopowe przy użyciu sztucznej inteligencji, mające na celu wspieranie patologów szybkimi, spójnymi i wysoce dokładnymi opiniami drugimi przy zachowaniu niskich kosztów obliczeniowych, odpowiednich do codziennego użycia w szpitalach.
Wyzwanie związane z odczytem obrazów tkankowych
Rak piersi jest jednym z najczęstszych nowotworów na świecie i odpowiada za setki tysięcy zgonów rocznie. Kluczem do lepszych wyników jest wczesne wykrycie i charakterystyka guzów, co nadal w dużej mierze opiera się na histopatologii: badaniu wybarwionych przekrojów tkanki pod mikroskopem. Jednak wiele wzorców tkankowych wygląda myląco podobnie. Próbki prawidłowe i łagodne (niegroźne) mogą mieć podobne struktury, podczas gdy wczesne zmiany przedinwazyjne i nowotwory inwazyjne mogą się wzajemnie zacierać. Dodatkowo różnice w barwieniu, oświetleniu i kontraście obrazów między laboratoriami mogą sprawiać, że ta sama choroba wygląda zupełnie inaczej. Tradycyjne programy komputerowe mają trudności z tymi subtelnościami, a wiele nowoczesnych systemów głębokiego uczenia, które radzą sobie lepiej, jest tak dużych i energochłonnych, że trudno je wdrożyć poza ośrodkami badawczymi najwyższego szczebla.
Dwie kompaktowe sieci pracujące zespołowo
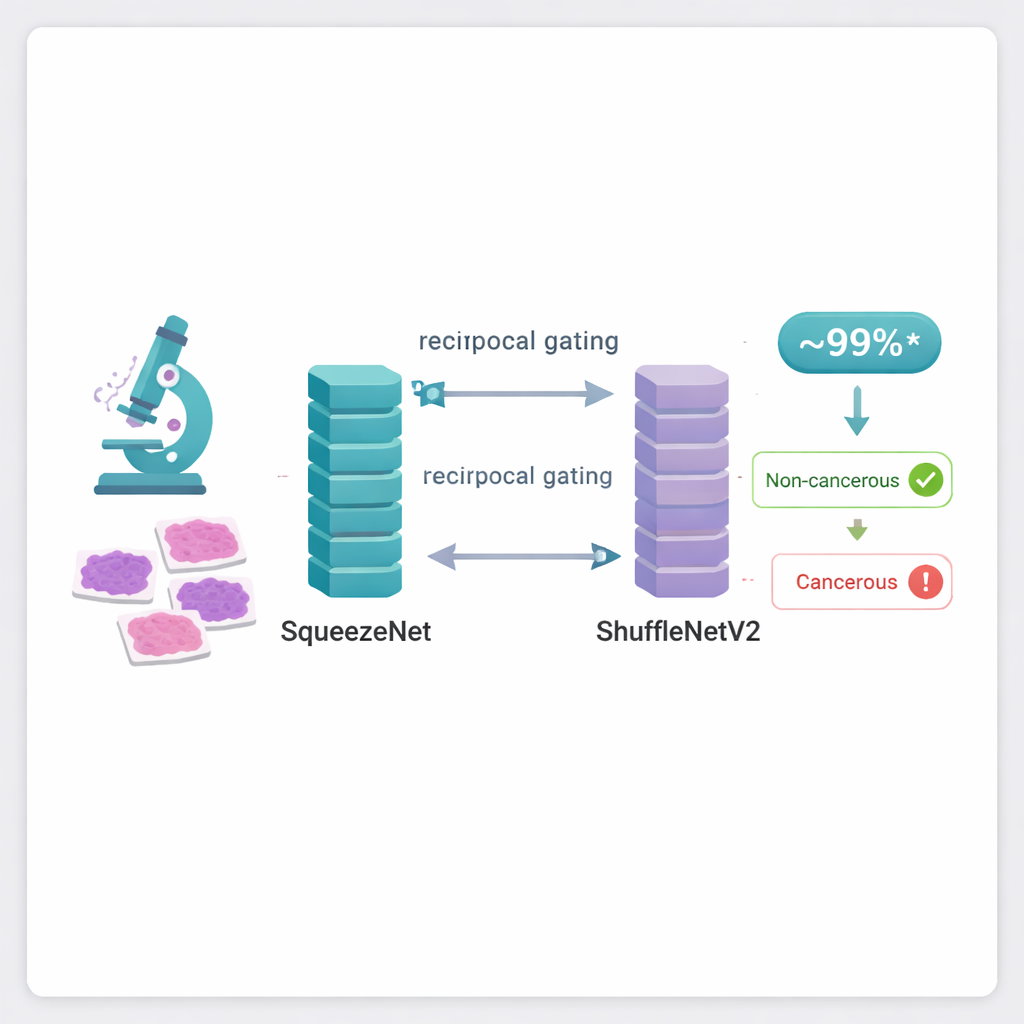
Aby sprostać temu problemowi, autorzy łączą dwie istniejące kompaktowe sieci neuronowe, znane jako SqueezeNet i ShuffleNetV2. Modele te zostały pierwotnie zaprojektowane do rozpoznawania codziennych obiektów na zdjęciach przy znacznie mniejszych wymaganiach obliczeniowych niż ciężkie systemy, takie jak Transformery czy bardzo głębokie sieci. W tej pracy przeuczono je do rozpoznawania wzorców na obrazach tkanki piersi. Każda sieć analizuje to samo zdjęcie mikroskopowe i uczy się wyłapywać różne wskazówki wizualne — subtelne różnice w kształcie komórek, teksturze tkanki i układzie kolorów. Samodzielnie każdy model radzi sobie dobrze, ale prawdziwą innowacją jest sposób, w jaki łączone są ich mocne strony.
Mechanizm bramkowy filtrujący szum
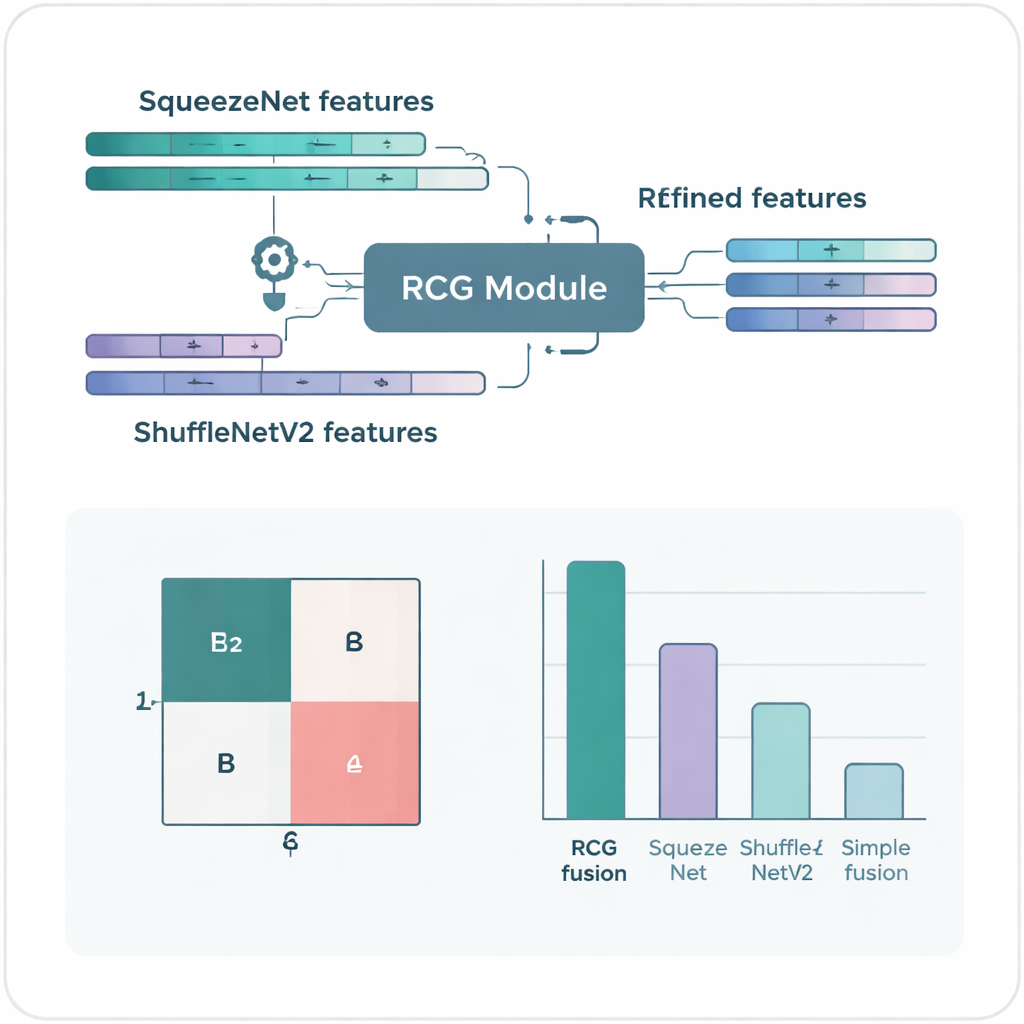
Główną ideą badania jest nowy moduł „wzajemnej, kooperacyjnej bramki”, który pozwala obu sieciom komunikować się i decydować, które fragmenty ich wewnętrznych sygnałów są naprawdę użyteczne. Zamiast prostego łączenia lub uśredniania wyjść, system bramek ocenia, ile informacji niesie każdy kanał i na ile jest on redundantny wobec tego, co już zobaczył partner. Kanały wnoszące nowe, pomocne szczegóły są wzmacniane, natomiast te powtarzające informacje lub dodające szum są tłumione. Ta dwukierunkowa korekta zachodzi w obu kierunkach, więc SqueezeNet wyostrza cechy ShuffleNetV2 i odwrotnie. W efekcie powstaje pojedyncza, zintegrowana reprezentacja obrazu, która jest bogatsza, czystsza i bardziej skupiona na drobnych różnicach rozróżniających diagnozy.
Wysoka dokładność przy niewielkich wymaganiach obliczeniowych
Testowany na dwóch powszechnie stosowanych zbiorach obrazów raka piersi, ICIAR‑2018 i BreakHis, system połączony wykazuje imponujące wyniki. W zadaniu czteroklasowym — rozróżnianiu tkanki prawidłowej, zmian łagodnych, raka przedinwazyjnego i raka inwazyjnego — poprawnie klasyfikuje 97 procent obrazów. Gdy zadanie uprości się do rozróżnienia tkanek nowotworowych od nienowotworowych, dokładność rośnie do 99 procent dla ICIAR‑2018 i około 99,7 procent dla BreakHis. Wyniki te przewyższają wiele bardziej złożonych metod opisanych w literaturze, mimo że nowy model używa relatywnie niewielu parametrów i skromnej mocy obliczeniowej, co przekłada się na szybsze predykcje i mniejsze wymagania sprzętowe.
Co to oznacza dla pacjentek i placówek
Mówiąc prosto, autorzy zbudowali smukłego, lecz potężnego asystenta, który potrafi przesiać obrazy mikroskopowe tkanki piersi i oznaczyć je z niemal ekspercką niezawodnością. Dzięki efektywnemu projektowi jest on lepiej dostosowany do rzeczywistych warunków, takich jak szpitale regionalne czy centra przesiewowe, które mogą nie dysponować wysokiej klasy serwerami. System nie zastępuje patologów, lecz może wskazywać podejrzane obszary, dostarczać spójnych drugich opinii i potencjalnie przyspieszać diagnostykę. Praca wskazuje także na szerszy trend: przez sprytne łączenie mniejszych modeli AI i uczenie ich współpracy zamiast rywalizacji, można osiągnąć najwyższą jakość wyników bez kosztów i złożoności, które często utrudniają praktyczne zastosowanie medycznej sztucznej inteligencji.
Cytowanie: Khati, B., Mukherjee, S., Sinitca, A. et al. Reciprocal cooperative gating fusion of SqueezeNet and ShuffleNetV2 for breast cancer detection in histopathology images. Sci Rep 16, 5904 (2026). https://doi.org/10.1038/s41598-026-36375-8
Słowa kluczowe: rak piersi, histopatologia, Sztuczna inteligencja w obrazowaniu medycznym, lekka sieć CNN, wspomaganie diagnostyki komputerowej