Clear Sky Science · pl
Rozwikłanie patogenezy POChP: podejście multi-omics w celu identyfikacji metabolitów i powiązań genetycznych
Dlaczego choroby płuc i biochemia organizmu są powiązane
Przewlekła obturacyjna choroba płuc (POChP) jest powszechnie postrzegana jako choroba płuc palaczy, ale to badanie pokazuje, że to, co dzieje się w naszej krwiochemii, może być równie ważne jak to, co wdychamy. Łącząc duże zbiory danych genetycznych, szczegółowe pomiary małych cząsteczek we krwi oraz eksperymenty laboratoryjne na ludzkich komórkach dróg oddechowych, badacze odkrywają, jak zaburzone przetwarzanie tłuszczów w organizmie może przyczyniać się do POChP — i w jaki sposób dobrze znany lek wziewny, salbutamol, może pomagać w zaskakujący sposób.
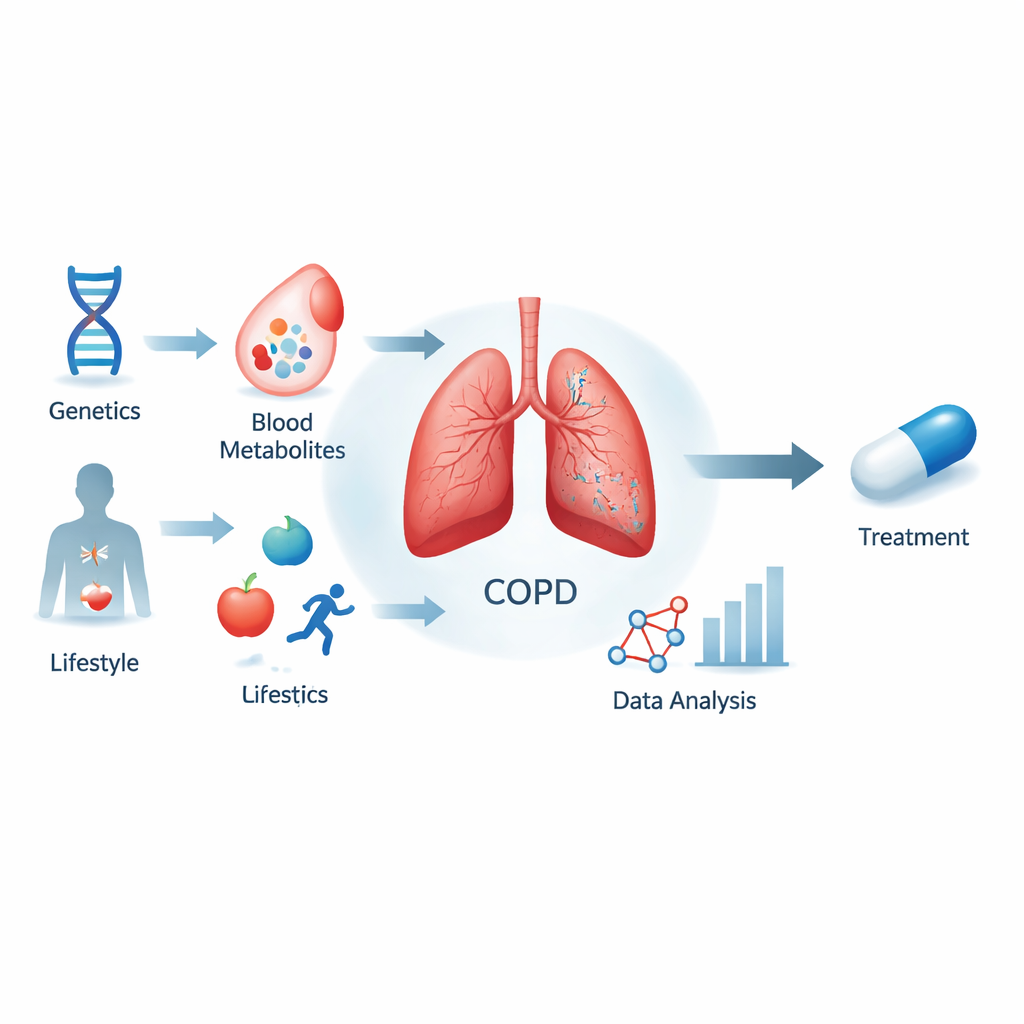
Patrząc na POChP poza paleniem
POChP dotyka setek milionów ludzi na całym świecie i prognozuje się, że stanie się trzecią najczęstszą przyczyną zgonów. Chociaż palenie i zanieczyszczenie powietrza są głównymi winowajcami, nie wyjaśniają w pełni, kto zachoruje na POChP ani jak szybko choroba postępuje. Zespół stojący za tym projektem zapytał, czy konkretne cząsteczki krwi, nazywane metabolitami, są nie tylko markerami uszkodzeń, ale aktywnymi uczestnikami choroby. Skupili się na ponad 1 400 metabolitach mierzonych w dużych europejskich badaniach i powiązali je z ryzykiem POChP, wykorzystując różnice genetyczne ludzi jako rodzaj naturalnego eksperymentu.
Wykorzystanie genów do testowania przyczynowości
Aby wyjść poza prostą korelację, badacze zastosowali technikę zwaną randomizacją Mendla. Mówiąc prosto, śledzili, czy osoby, które rodzą się z wariantami genów podwyższającymi lub obniżającymi poziomy określonych metabolitów, mają także wyższe lub niższe szanse rozwoju POChP. Podejście to pomaga oddzielić prawdziwe przyczyny od nawyków życiowych, które mogą zaciemniać obraz, jak picie kawy czy palenie. Spośród 1 400 metabolitów sześć początkowo wyróżniało się powiązaniem z ryzykiem POChP. Jednak drugi, bardziej rygorystyczny test genetyczny wykazał, że tylko dwa — karnityna C14 i 3-hydroksyoleoilo-karnityna — dzielą ten sam podstawowy sygnał genetyczny co POChP. Oba związane są z metabolizmem długołańcuchowych kwasów tłuszczowych, co sugeruje, że metabolizm tłuszczów, a nie tylko zapalenie i przepływ powietrza, leży u źródeł POChP.
Od cząsteczek do kluczowych przełączników
Gdy zidentyfikowano dwa wiarygodne metabolity, badacze prześledzili drogi metaboliczne, którymi one podążają. Drogi te skupiły się na metabolizmie kwasów tłuszczowych i uwypukliły zestaw enzymów działających jak sygnalizacja świetlna, kontrolujących, ile tłuszczu jest budowane lub rozkładane — w szczególności enzymy ACACA i ACACB. Przeszukując istniejące bazy danych leków i interakcji białek, zespół odkrył, że enzymy te leżą w tej samej sieci co ADRB2, białkowy cel salbutamolu, powszechnego leku rozszerzającego oskrzela stosowanego w POChP. Analizy tkanek płucnych od pacjentów wykazały zwiększoną ekspresję ACACA i ACACB, podczas gdy ADRB2 był obniżony, co jest zgodne ze stanem przeciążenia kwasami tłuszczowymi w chorobowo zmienionych płucach.
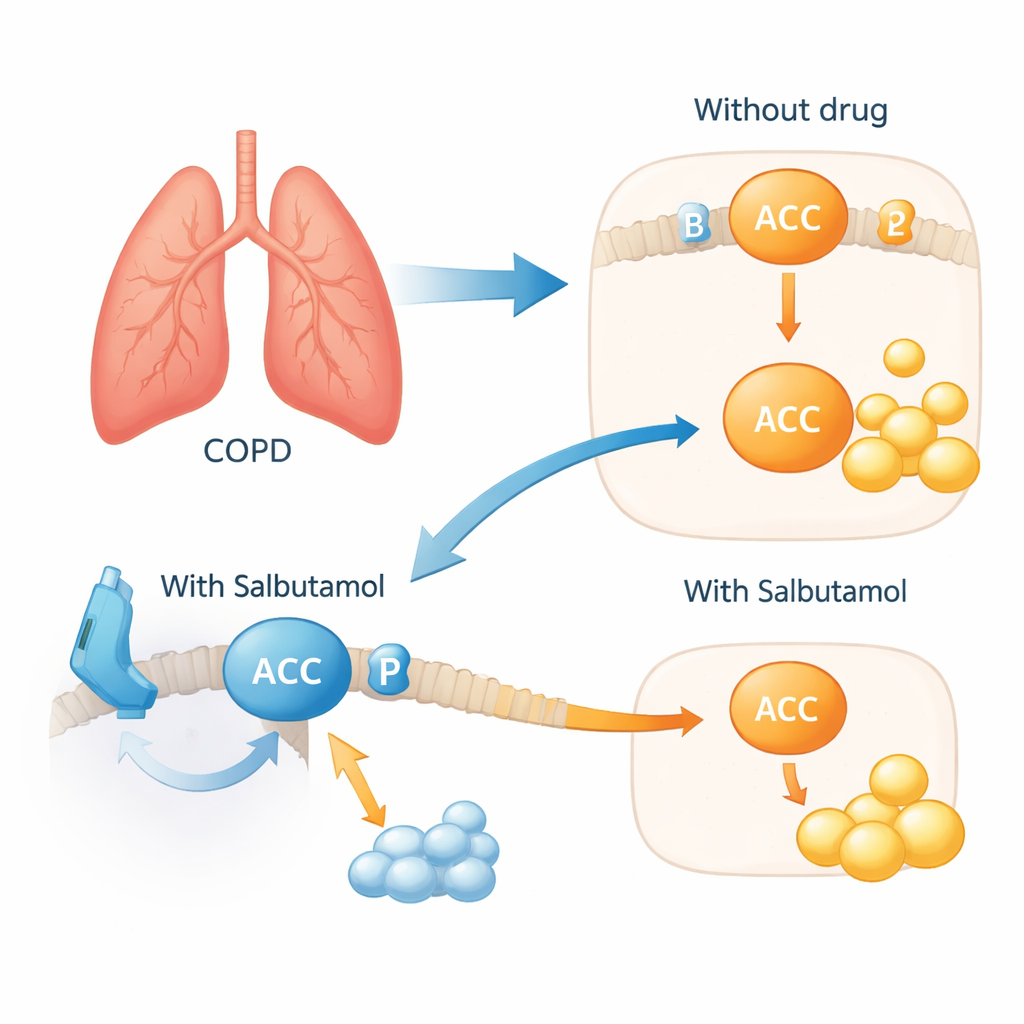
Wziewny lek, który także hamuje bezkrytyczną syntezę tłuszczów
Aby sprawdzić, czy ta sieć ma znaczenie w żywych komórkach, naukowcy wystawili ludzkie komórki oskrzelowe na ekstrakt z dymu papierosowego, by naśladować stres podobny do POChP. Komórki zareagowały zwiększeniem ekspresji ACACA i ACACB oraz zmniejszeniem ochronnej modyfikacji chemicznej na ACACA, która normalnie utrzymuje pod kontrolą produkcję tłuszczu. Po dodaniu salbutamolu ten szkodliwy wzorzec odwrócił się: ochronna modyfikacja ACACA została przywrócona, a oznaki nadmiernej syntezy tłuszczów zmalały. Mówiąc prościej, lek wydawał się włączać hamulec w maszynerii budującej tłuszcz wewnątrz komórek dróg oddechowych, działając przez przełącznik ADRB2 na powierzchni komórki. Analizy genetyczne związane ze stylami życia dodatkowo wspierały ideę, że dwa kluczowe metabolity są powiązane z podstawową biologią, a nie jedynie z nawykami, jak spożycie kawy, które wyjaśniało kilka innych kandydatów.
Co to znaczy dla pacjentów i przyszłych terapii
Dla osób niebędących specjalistami najważniejszy wniosek jest taki, że POChP może być częściowo napędzana przez metaboliczny korek w sposobie, w jaki komórki płuc przetwarzają tłuszcze, i że szeroko stosowany bronchodilatator może również cicho pomagać w usuwaniu tego zatoru. Karnityna C14 i 3-hydroksyoleoilo-karnityna wyłaniają się jako silne markery we krwi, które w przyszłości mogą pomóc wykrywać osoby o wyższym ryzyku lub śledzić postęp choroby. Enzymy ACACA i ACACB, znajdujące się w kluczowych punktach metabolizmu tłuszczów i powiązane z celem salbutamolu ADRB2, oferują nowe punkty uchwytu dla deweloperów leków. Choć potrzebne są dalsze badania w zróżnicowanych populacjach i dogłębne analizy metaboliczne, podejście multi-omics otwiera drogę do terapii POChP, które robią więcej niż tylko rozszerzają drogi oddechowe — mogą również przywracać zdrowsze wykorzystanie paliwa w płucach.
Cytowanie: Zeng, M., Liu, J., Cao, X. et al. Unraveling COPD pathogenesis: a multi-omics approach to identify metabolites and genetic links. Sci Rep 16, 6013 (2026). https://doi.org/10.1038/s41598-026-36368-7
Słowa kluczowe: POChP, metabolizm kwasów tłuszczowych, Salbutamol, biomarkery karnitynowe, multi-omics