Clear Sky Science · pl
Rola modyfikacji histonów mediowanych przez MNX1 i rodziny genów PBX w leukemogenezie indukowanej przez MNX1
Dlaczego drobna wada genetyczna ma znaczenie dla chorych dzieci
Większość białaczek dziecięcych da się dziś leczyć, ale rzadki typ zwany ostrą białaczką szpikową (AML) u niemowląt pozostaje wyjątkowo śmiertelny. U wielu tych niemowląt pojawia się ten sam wypadek genetyczny: dwa chromosomy zamieniają się fragmentami, co przemienia cichy gen rozwojowy MNX1 w nadaktywnego sprawcę. W badaniu zadano proste, lecz kluczowe pytanie: gdy MNX1 zostaje włączony, co dokładnie robi wewnątrz młodych komórek krwi, by popchnąć je w kierunku nowotworu — i czy ten proces da się przerwać?
Od normalnych komórek krwi niemowlęcia do niekontrolowanego wzrostu
Białaczka powstaje, gdy niedojrzałe komórki krwi przestają się różnicować i zaczynają mnożyć w niekontrolowany sposób. U niemowląt z translokacją t(7;12) MNX1 staje się nadmiernie aktywny w bardzo wczesnych komórkach tworzących krew, występujących w wątrobie płodowej i szpiku. Naukowcy stworzyli model myszy odzwierciedlający tę sytuację: włączyli ludzki MNX1 w płodowych komórkach macierzystych krwi, przeszczepili je do myszy i obserwowali, jak zwierzęta przechodzą od stanu przedbiałaczkowego do pełnoobjawowej białaczki. Porównując komórki z tych etapów z komórkami zdrowymi, mogli prześledzić, jak MNX1 z czasem przepisuje wewnętrzne systemy kontroli komórkowej.
Jak MNX1 przepisuje instrukcję komórki
MNX1 to czynnik transkrypcyjny — białko, które przyłącza się do DNA i kontroluje, które geny są włączane lub wyłączane. Zespół zastosował kilka zaawansowanych metod — spektrometrię mas, sekwencjonowanie RNA i profilowanie chromatyny — aby sprawdzić, z jakimi partnerami współpracuje MNX1 i jakie geny zmienia. Odkryli, że MNX1 łączy się z enzymami, które dodają chemiczne znaczniki do białek histonowych, tworzacych „szpule”, wokół których owinięte jest DNA. W szczególności MNX1 zwiększa obecność markera „WŁĄCZONE” H3K4me3 i zmniejsza marker „WYŁĄCZONE” H3K27me3 w określonych miejscach genomu. Te zmiany rozluźniają lokalną strukturę DNA i ułatwiają włączanie kluczowych genów związanych z wzrostem.
Krótkie, lecz decydujące działanie na krytyczny gen kontrolny
Wśród wielu dotkniętych genów wyróżnił się jeden: Pbx1, należący do rodziny białek wiążących DNA PBX, od dawna powiązanych z białaczką. Badanie pokazuje, że MNX1 wiąże się bezpośrednio z obszarem kontrolnym genu Pbx1, zwiększając marker WŁĄCZENIA i usuwając marker WYŁĄCZENIA w tym miejscu. To przyspiesza ekspresję Pbx1 bardzo wcześnie, gdy komórki są wciąż tylko przedbiałaczkowe. Co zaskakujące, później — gdy białaczka jest już utrwalona — MNX1 nie jest już silnie związany z tym miejscem, a mimo to gen Pbx1 pozostaje aktywny, a jego markery histonowe utrzymują pro‑wzrostową konfigurację. Sugeruje to mechanizm „uderz i odejdź”: MNX1 krótko odwiedza kluczowe regiony chromatyny, pozostawia trwałe zmiany epigenetyczne, a następnie może odejść, podczas gdy zmieniony stan nadal napędza chorobę.
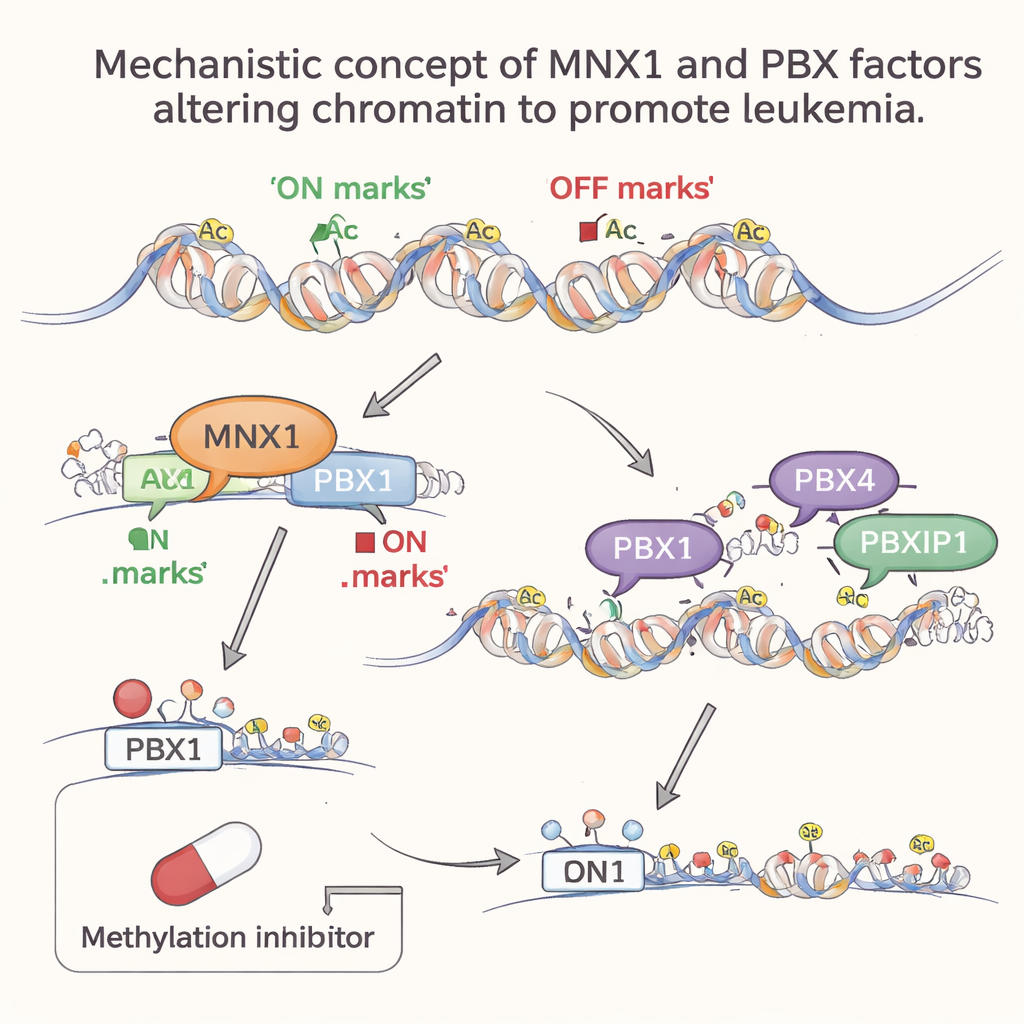
Późniejsi wspomagacze dołączają, by utrwalić stan nowotworowy
W miarę postępu białaczki inne członkinie rodziny PBX, PBX4 i PBXIP1, stają się bardziej aktywne, ale dopiero na tym późniejszym etapie. Analizy obejmujące cały genom wykazały, że ich preferowane motywy DNA są silnie wzbogacone w regionach otwartej, aktywnej chromatyny, które zostały przeformowane w następstwie aktywności MNX1. Innymi słowy, MNX1 najpierw przekształca krajobraz chromatyny i uruchamia Pbx1; potem PBX4 i PBXIP1 wchodzą w te nowo dostępne regiony, aby wzmocnić nieprawidłowe programy genowe sprzyjające podziałom komórek, blokujące normalne tworzenie krwi i upośledzające naprawę DNA. Ta stopniowa współpraca sugeruje podział ról: PBX1 działa jako wczesny wyłącznik zależny od MNX1, podczas gdy PBX4 i PBXIP1 pomagają utrzymać program białaczkowy.
Blokowanie chemicznych znaków napędzających białaczkę
Ponieważ MNX1 działa przez enzymy dodające grupy metylowe do histonów, zespół sprawdził, czy szeroki inhibitor metylotransferaz, Sinefungin, może przerwać ten łańcuch zdarzeń. W przedbiałaczkowych płodowych komórkach krwi wyrażających MNX1, Sinefungin silnie obniżył poziomy Pbx1, co jest zgodne z blokowaniem metylacji na promotorze, na której polega działanie MNX1. Natomiast poziomy PBX4 i PBXIP1 zmieniły się nieznacznie, co pasuje do ich późniejszej, pośredniej aktywacji w przebiegu choroby. Razem te wyniki przekonująco wskazują, że AML niemowląt z t(7;12) napędzana jest nie tylko przez uszkodzony gen, lecz przez kaskadę trwałych zmian epigenetycznych, które inicjuje MNX1.
Co to oznacza dla przyszłych terapii
Dla osób niespecjalistycznych najważniejszy wniosek jest taki: badanie mapuje reakcję łańcuchową — nadaktywne MNX1 przebudowuje chemiczne markery na białkach pakujących DNA, wcześnie włącza PBX1 i toruje drogę, by PBX4 i PBXIP1 pomogły zablokować komórki w stanie białaczkowym. Ponieważ te etapy zależą od określonych wzorców metylacji histonów, stanowią one jasne, testowalne cele dla leków ingerujących w te markery. W dłuższej perspektywie terapie ukierunkowane na oś MNX1–PBX lub na enzymy umieszczające te epigenetyczne znaczniki mogłyby wyłączyć błędne instrukcje napędzające tę agresywną białaczkę u niemowląt i zwiększyć szanse na trwałe wyleczenia.
Cytowanie: Malmhäll-Bah, E., Östlund, A., Nilsson, T. et al. Role of MNX1-mediated histone modifications and PBX gene family in MNX1-induced leukemogenesis. Sci Rep 16, 2593 (2026). https://doi.org/10.1038/s41598-026-36367-8
Słowa kluczowe: ostra białaczka szpikowa u niemowląt, MNX1, PBX1 PBX4 PBXIP1, epigenetyczne metylacje histonów, translokacja chromosomalna t(7;12)