Clear Sky Science · pl
Translacyjne ocenianie BUB1B jako biomarkera medycyny precyzyjnej dla raka wątrobowokomórkowego
Dlaczego gen kontrolujący podział komórek ma znaczenie w raku wątroby
Większość osób myśli o raku w kontekście guzów widocznych w badaniach obrazowych, ale głęboko w tych zmianach działają mikroskopijne systemy sterujące, które decydują, jak i kiedy komórki się dzielą. W badaniu skupiono się na jednym takim przełączniku — genie o nazwie BUB1B — i pokazano, w jaki sposób może on pomóc lekarzom przewidywać, u których pacjentów z rakiem wątroby przebieg będzie gorszy, kto może odpowiadać na konkretne leki oraz dlaczego niektóre guzy potrafią przechytrzyć układ odpornościowy. Przekształcając podstawowy regulator cyklu komórkowego w „panel kontrolny” zachowania raka wątroby, praca wskazuje drogę do bardziej precyzyjnego i zindywidualizowanego leczenia.
Powszechny rak wątroby potrzebuje lepszych drogowskazów
Rak wątrobowokomórkowy, najczęstsza postać pierwotnego raka wątroby, często jest wykrywany późno, gdy pojawiają się objawy, a możliwości terapeutyczne są ograniczone. Dotychczasowe testy krwi i markery tkankowe, takie jak alfa-fetoproteina czy Ki-67, są niedoskonałe: nie wychwytują niezawodnie wczesnej choroby ani nie wskazują jednoznacznie terapii spersonalizowanych. Autorzy poszukiwali więc innego rodzaju markera — takiego, który odzwierciedla wewnętrzne okablowanie komórek nowotworowych, a nie tylko ich obecność. Skoncentrowali się na BUB1B, białku pomagającym zapewnić prawidłowy rozdział chromosomów podczas podziału komórki. Gdy ten system zawodzi, kumulują się błędy genetyczne, które mogą napędzać agresywne guzy.
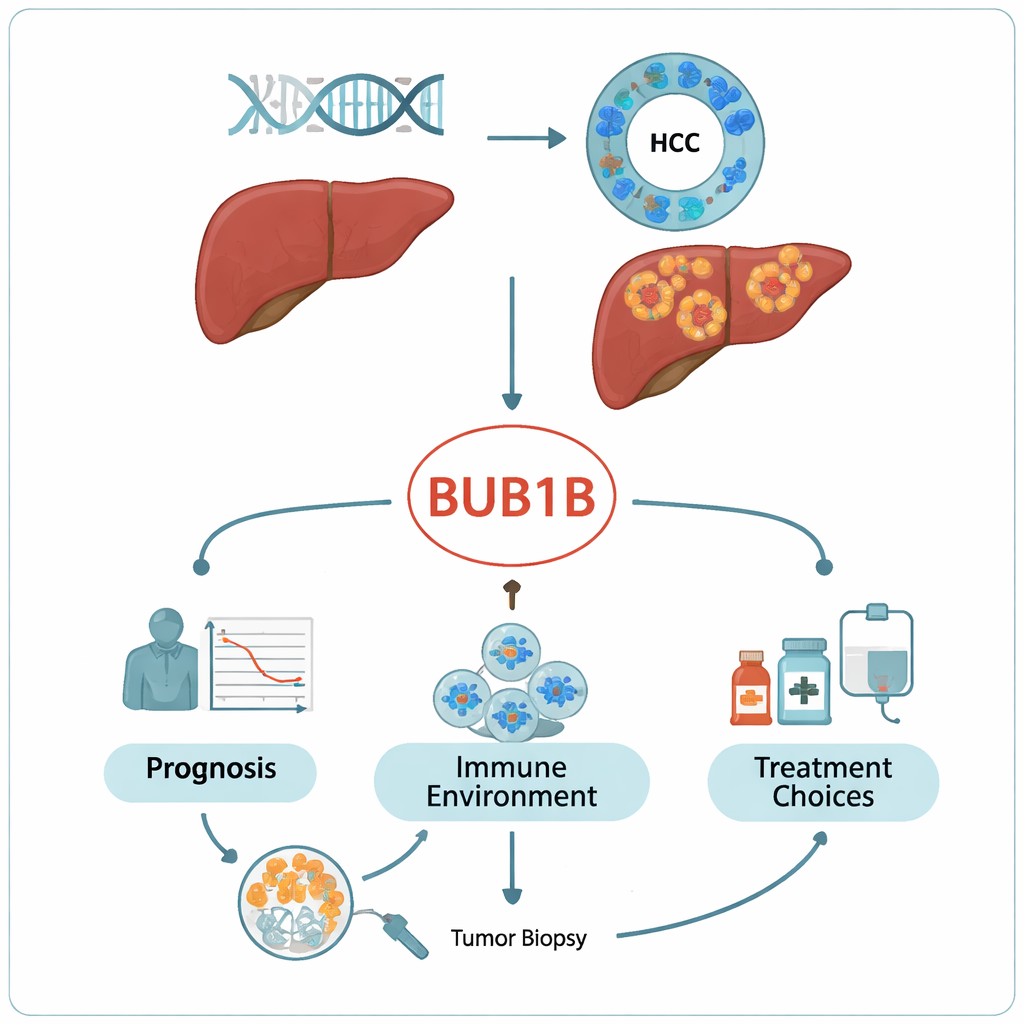
Śledzenie BUB1B w różnych nowotworach i u rzeczywistych pacjentów
Korzystając z dużych publicznych baz danych onkologicznych, w tym The Cancer Genome Atlas, badacze najpierw przeanalizowali aktywność BUB1B w wielu typach guzów. Stwierdzili, że jest on podwyższony w 19 różnych nowotworach, z wyjątkowo silną nadaktywnością w guzach wątroby w porównaniu z przylegającą zdrową tkanką. Pacjenci, u których raki wątroby wykazywały wyższe poziomy BUB1B, mieli tendencję do krótszego przeżycia, nawet po uwzględnieniu zaawansowania choroby, co czyni BUB1B niezależnym wskaźnikiem ostrzegawczym. Dogłębna analiza 50 pacjentów z rakiem wątroby leczonych w ich własnym szpitalu potwierdziła ten wzorzec: guzy wykazywały intensywne barwienie BUB1B pod mikroskopem, szczególnie w cytoplazmie komórek, a wysokie poziomy korelowały z większymi guzami, wyższym stadium choroby i gorszym przeżyciem.
Chaos genetyczny, odpowiedź na leki i zdezorientowany układ odpornościowy
Wysoki poziom BUB1B nie tylko sygnalizował, że guz jest groźny; wiązał się z głębszą niestabilnością DNA w nowotworze. Guzy z podwyższonym BUB1B wykazywały więcej oznak zaburzeń naprawy DNA i subtelnych form niestabilności mikrosatelitarnej — cech chaosu genomowego, które mogą zarówno napędzać szybką ewolucję, jak i kształtować odpowiedź na leczenie. Modele komputerowe łączące wzorce genowe z wynikami testów lekowych sugerowały, że raki wątroby z wysokim BUB1B mogą być w rzeczywistości bardziej podatne na niektóre leki, w tym lek celowany sorafenib oraz klasyczne chemioterapeutyki, takie jak paklitaksel i doksorubicyna, przy jednoczesnej względnej oporności na leki ukierunkowane na szlak EGFR. Równocześnie te guzy zawierały wiele komórek układu odpornościowego, zwłaszcza limfocytów T, ale mimo to osiągały wysokie wyniki w miarach dysfunkcji i wykluczenia immunologicznego — co oznacza, że układ odpornościowy był obecny, lecz skutecznie unieszkodliwiony i mniej skłonny do odpowiedzi na powszechne immunoterapie blokujące PD-1 lub PD-L1.
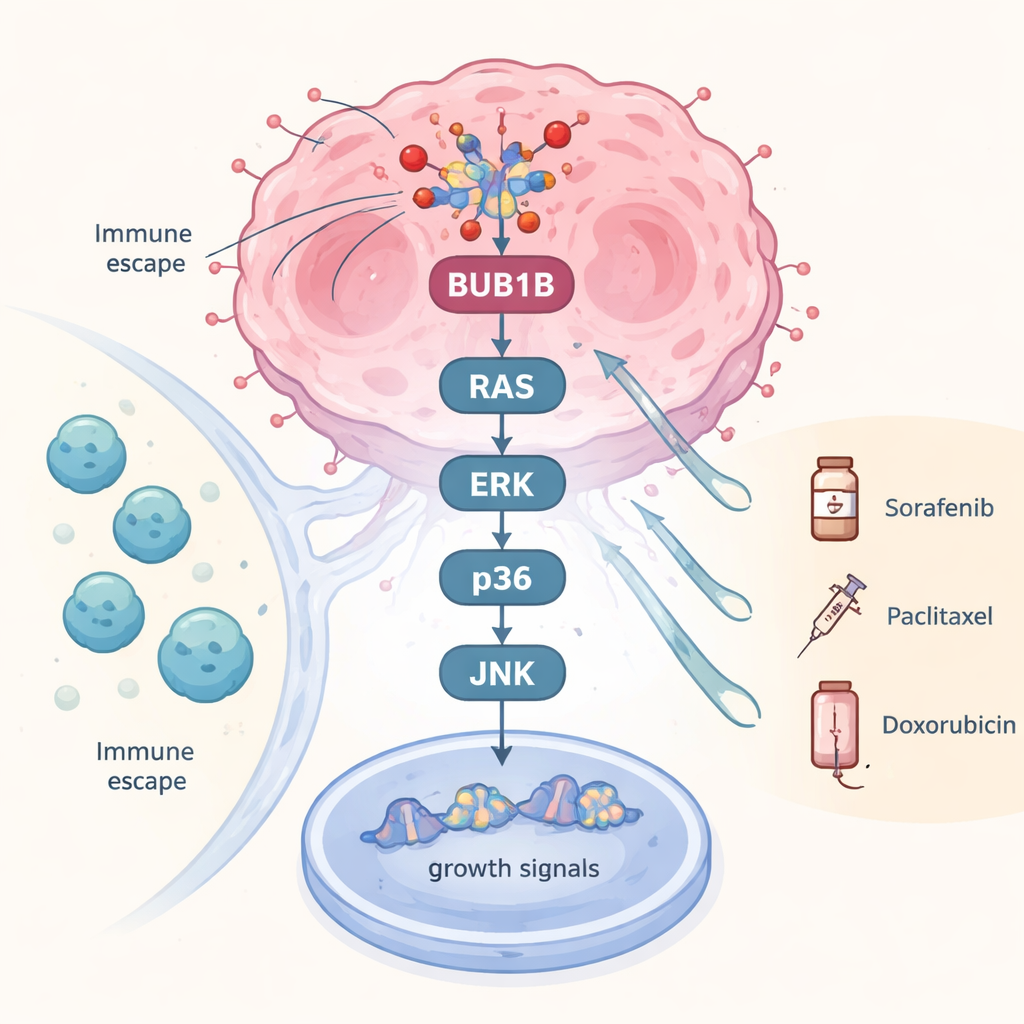
W jaki sposób BUB1B napędza sygnały wzrostu w komórkach nowotworowych
Aby wyjść poza powiązania statystyczne, zespół przetestował, co się dzieje, gdy BUB1B jest chemicznie hamowany w hodowanych w laboratorium komórkach raka wątroby. Zablokowanie tego genu osłabiło cały łańcuch sygnałów wzrostu zwykle składających się na szlaki MAPK. Kluczowe elementy na kilku poziomach — w tym RAS, niektóre białka rodziny RAF, ERK oraz liczne kinazy p38 i inne powiązane kinazy — zostały wyraźnie zredukowane. Ponieważ te szlaki działają jak przekaźnik nakazujący komórkom nowotworowym dalszy podział i oporność na stres, ich osłabienie sugeruje, że BUB1B nie jest tylko przypadkowym markerem, lecz aktywnym czynnikiem pomagającym utrzymać wewnętrzne okablowanie nowotworu. Niektóre składniki wykazały niespodziewane odbicia, sugerujące wbudowane pętle sprzężenia zwrotnego, lecz ogólny efekt polegał na szerokim osłabieniu sygnalizacji pro-wzrostowej.
Co to oznacza dla pacjentów i przyszłej opieki
Dla osób niebędących specjalistami wniosek jest taki, że pojedynczy gen kontroli podziału komórek, BUB1B, wydaje się leżeć na skrzyżowaniu trzech kluczowych cech raka wątroby: niestabilności DNA guza, jego dialogu z układem odpornościowym oraz odpowiedzi na kilka istotnych leków. Pomiar BUB1B w próbkach guza mógłby pomóc lekarzom przydzielać pacjentów do grup ryzyka, dokładniej oszacować przeżycie i wybierać terapie wykorzystujące słabości nowotworu — przy jednoczesnym rozpoznaniu, kiedy standardowa immunoterapia prawdopodobnie nie zadziała. Ponieważ guzy wątroby polegają na BUB1B, by utrzymywać sygnały wzrostu i odpowiedzi na stres, leki ukierunkowane na to białko, samodzielnie lub w połączeniu z istniejącymi terapiami, mogą otworzyć nowe drogi do bardziej precyzyjnego i skutecznego leczenia raka wątrobowokomórkowego.
Cytowanie: Sun, Cy., Yu, X., Deng, Lq. et al. Translational evaluation of BUB1B as a precision medicine biomarker for hepatocellular carcinoma. Sci Rep 16, 5301 (2026). https://doi.org/10.1038/s41598-026-36364-x
Słowa kluczowe: rak wątrobowokomórkowy, BUB1B, biomarker, szlak sygnalizacyjny MAPK, onkologia precyzyjna