Clear Sky Science · pl
Obniżenie ekspresji CDC25C hamuje wzrost HCC poprzez stres mitochondrialny wywołujący autofagię i apoptozę
Dlaczego to badanie nad rakiem wątroby ma znaczenie
Rak wątroby jest jednym z najgroźniejszych nowotworów na świecie, a wielu pacjentów jest diagnozowanych zbyt późno, by operacja lub standardowe terapie były skuteczne. Badanie to analizuje pojedynczy komórkowy „przełącznik”, białko nazwane CDC25C, które wydaje się napędzać wzrost raka wątroby, jednocześnie będąc mniej istotnym dla zdrowych komórek wątroby. Przy jego stłumieniu badacze zaobserwowali, że można wywołać stres i ostateczne zniszczenie komórek nowotworowych poprzez ich własne mechanizmy samoczyszczenia i samozniszczenia, co wskazuje na obiecującą i bardziej selektywną strategię leczenia.
Przełącznik wzrostu wewnątrz guzów wątroby
Każda komórka musi decydować, kiedy się dzielić, a kiedy zatrzymać. CDC25C jest jednym z kluczowych białek, które popycha komórki przez cykl podziału. W raku wątroby ten przełącznik często jest zablokowany w pozycji „włączonej”, co pomaga guzom rosnąć i się rozsiewać. Zespół użył mysich komórek raka wątroby i normalnych mysich komórek wątroby oraz myszy z guzami, aby sztucznie obniżyć poziom CDC25C. Potwierdzili za pomocą standardowych testów genetycznych i białkowych, że CDC25C został wyraźnie zredukowany w grupie eksperymentalnej w porównaniu z kontrolami, ustanawiając solidny model do badania, co się dzieje, gdy ten przełącznik wzrostu jest przykręcony.
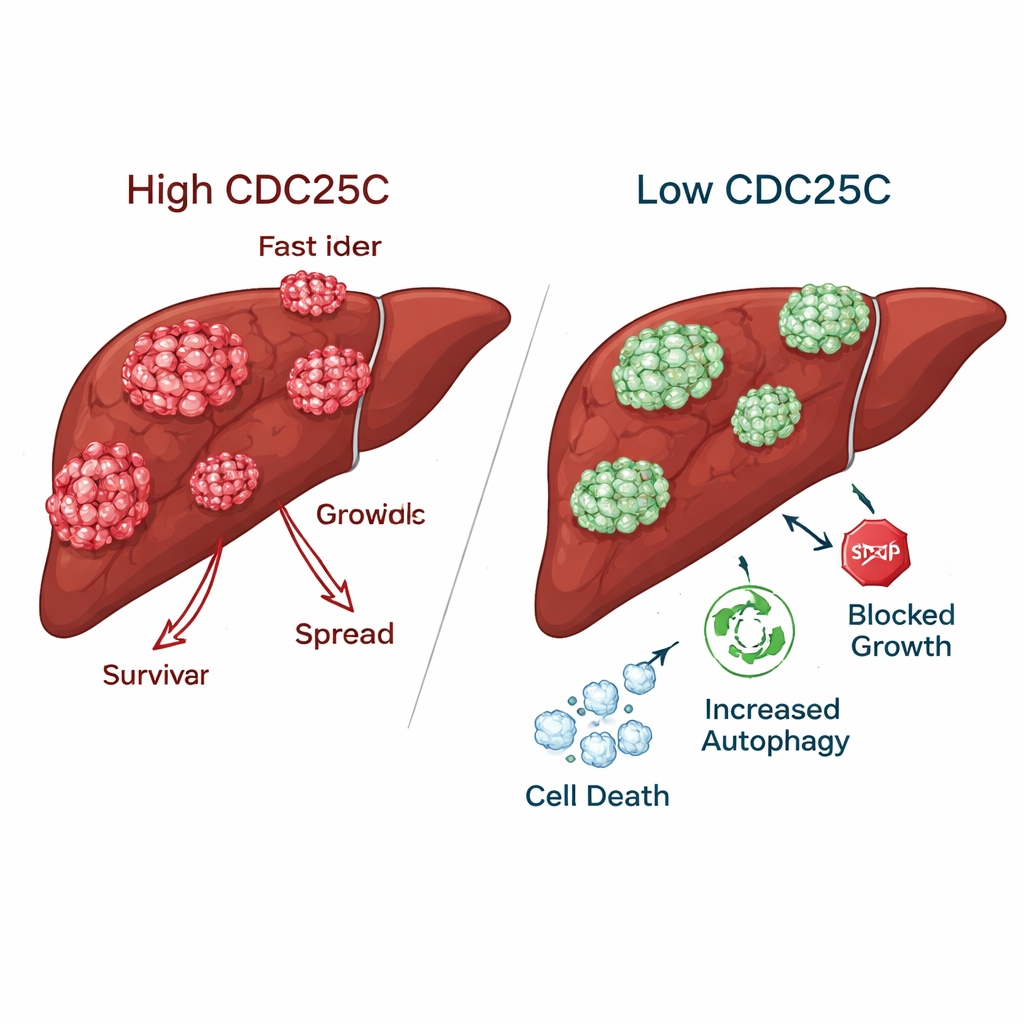
Spowalnianie raka przy jednoczesnym oszczędzaniu zdrowej wątroby
Gdy CDC25C został zmniejszony w komórkach raka wątroby, guzy utraciły wiele ze swoich agresywnych cech. Komórki nowotworowe tworzyły znacznie mniej kolonii, poruszały się wolniej przy sztucznych „urazach” i mniej skutecznie przechodziły przez bariery w testach inwazyjności. W przeciwieństwie do tego, normalne komórki wątroby wykazywały wręcz lepszy wzrost i ruch po obniżeniu CDC25C, co sugeruje, że zdrowa tkanka może tolerować lub nawet odnieść korzyść z hamowania CDC25C. U myszy, guzy zaprojektowane z obniżonym CDC25C wykazywały niższe poziomy tego białka zarówno w pomiarach genowych, jak i białkowych, co potwierdza, że ten sam efekt występował in vivo.
Stres energetyczny i system sprzątający komórki
Patrząc do wnętrza komórek za pomocą mikroskopii elektronowej, badacze zauważyli, że komórki nowotworowe z niskim CDC25C zawierały spuchnięte, uszkodzone mitochondria — małe elektrownie komórkowe — oraz struktury przypominające pęcherzyki zwane autofagosomami, które sygnalizują aktywację wewnętrznego systemu recyklingu komórkowego, autofagii. Następnie zmierzyli kluczowe wskaźniki stresu mitochondrialnego: poziomy wapnia i reaktywnych form tlenu (ROS), oba zwiększyły się w komórkach nowotworowych po obniżeniu CDC25C. Markery odpowiedzi na stres mitochondrialny, w tym białka pomocnicze takie jak HSP60 i dwie mitochondrialne enzymy „kontroli jakości”, również wzrosły, podobnie jak CHOP — czynnik związany ze stresem łączący problemy mitochondrialne z szerzej zakrojoną reakcją komórkową. Co istotne, te sygnały stresowe zmieniały się w przeciwnym kierunku w normalnych komórkach wątroby, wzmacniając ideę, że komórki nowotworowe i zdrowe reagują bardzo odmiennie na utratę CDC25C.
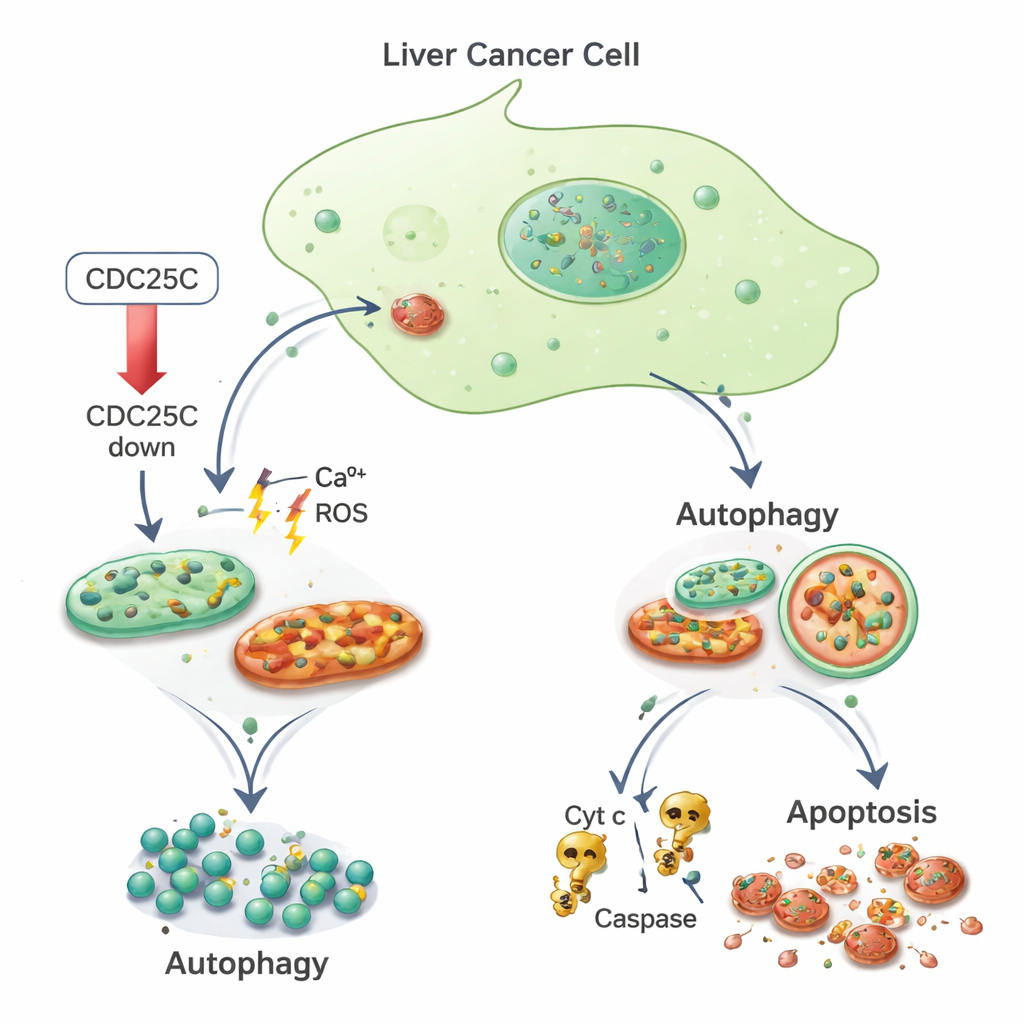
Od stresu do samostrawienia i śmierci komórki
Zespół zapytał następnie, jak te zestresowane komórki nowotworowe sobie radzą. Stwierdzili, że markery autofagii były podwyższone zarówno w komórkach nowotworowych, jak i w normalnych komórkach wątroby po obniżeniu CDC25C. Białka takie jak LC3 i p62, które odzwierciedlają tworzenie i aktywność autofagosomów, zwiększyły się, co wskazuje, że komórki intensyfikują swoją maszynerię sprzątającą. Jednocześnie, tylko w komórkach nowotworowych, uszkodzenie mitochondriów wydaje się popychać komórki poza punkt naprawy i w kierunku programowanej śmierci. Przy użyciu barwień fluorescencyjnych i cytometrii przepływowej badacze zaobserwowali więcej komórek nowotworowych z pofragmentowanymi, intensywnie barwiącymi się jądrami — cechą charakterystyczną apoptozy — oraz obniżony potencjał błony mitochondrialnej. Stwierdzili także podwyższone poziomy cytochromu c oraz enzymów Kaspazy-3 i Kaspazy-9, klasycznych komponentów mitochondriozależnej ścieżki śmierci. Normalne komórki wątroby, w przeciwieństwie do tego, wykazywały mniejszą apoptozę przy tych samych warunkach obniżenia CDC25C.
Co to może znaczyć dla przyszłych terapii
Dla czytelnika spoza specjalności kluczowy wniosek jest taki, że przykręcenie CDC25C wydaje się uderzać w komórki raka wątroby tam, gdzie są najsłabsze: przeciąża ich „elektrownie”, pobudza systemy recyklingu do nadmiernej pracy i ostatecznie wywołuje czyste samozniszczenie — przy jednoczesnym względnym oszczędzeniu zdrowych komórek wątroby. Autorzy wnioskują, że CDC25C to coś więcej niż prosty przełącznik wzrostu; kształtuje także sposób, w jaki komórki radzą sobie ze stresem, sprzątaniem i śmiercią. Ponieważ komórki nowotworowe silnie polegają na CDC25C i reagują na jego utratę śmiertelnym stresem mitochondrialnym i apoptozą, leki celujące w to białko lub jego pośrednie ścieżki stresowe mogłyby w przyszłości zaoferować bardziej selektywną metodę leczenia raka wątroby z mniejszą szkodą dla zdrowej tkanki wątroby.
Cytowanie: Miao, X., Zheng, F., Mo, X. et al. CDC25C downregulation suppresses HCC growth via mitochondrial stress-induced autophagy and apoptosis. Sci Rep 16, 5631 (2026). https://doi.org/10.1038/s41598-026-36351-2
Słowa kluczowe: rak wątrobowokomórkowy, CDC25C, stres mitochondrialny, autofagia, apoptoza