Clear Sky Science · pl
TET1 hamuje rozwój raka wątrobowokomórkowego poprzez modulację szlaków sygnałowych PI3K/Akt
Dlaczego enzym wątrobowy ma znaczenie dla raka
Pierwotny rak wątroby, a w szczególności rak wątrobowokomórkowy, jest jednym z najgroźniejszych nowotworów na świecie. Wielu pacjentów jest diagnozowanych zbyt późno, by można było zastosować leczenie chirurgiczne z zamiarem wyleczenia, a dostępne leki pomagają tylko niewielkiej części chorych. W tym badaniu zbadano cząsteczkę nazwaną TET1, enzym, który modyfikuje chemiczne znaczniki na DNA, aby postawić proste, lecz istotne pytanie: czy TET1 pomaga guzom wątroby rosnąć i czy może stać się nowym celem terapeutycznym?
Ukryty edytor w naszym DNA
Nasze geny są kontrolowane nie tylko przez sam kod DNA, lecz także przez chemiczne znaki, które włączają lub wyłączają geny. Jednym z powszechnych znaczników jest metylacja DNA, działająca jak ściemniacz aktywności genowej. TET1 należy do rodziny enzymów, które usuwają lub przekształcają te znaczniki, pomagając komórkom reagować na środowisko i utrzymywać normalną funkcję. Gdy ten system zawodzi, komórki mogą przejść w stany chorobowe, w tym nowotworowe. Wcześniejsze badania wykazały, że TET1 może hamować lub przyspieszać wzrost guza w zależności od tkanki, ale jego dokładna rola w ludzkim raku wątroby pozostawała niejasna i budziła szerokie kontrowersje.
Poziomy TET1 rosną w guzach wątroby
Aby ustalić, co TET1 robi w raku wątroby, badacze najpierw sięgnęli do dużych publicznych baz danych genowych, a potem przeanalizowali próbki od pacjentów. W wielu typach nowotworów poziomy TET1 były nietypowo wysokie w kilku guzach, w tym w raku wątroby. Skupiając się na guzach wątroby, porównali tkankę guza z pobliską, niezmienioną tkanką wątrobową od tych samych pacjentów. W ośmiu sparowanych próbkach białko TET1 było konsekwentnie wyższe w guzie. Publicznie dostępne zestawy danych z setek pacjentów pokazały podobny obraz na poziomie RNA: raki wątroby miały więcej TET1 niż zdrowe wątroby lub wątroby z samym włóknieniem. Pacjenci, których guzy wykazywały wyższe poziomy TET1, mieli skłonność do bardziej zaawansowanej choroby oraz krótszego całkowitego i chorobowo‑wolnego przeżycia, co sugeruje związek TET1 z agresywnością guza i gorszym rokowaniem.
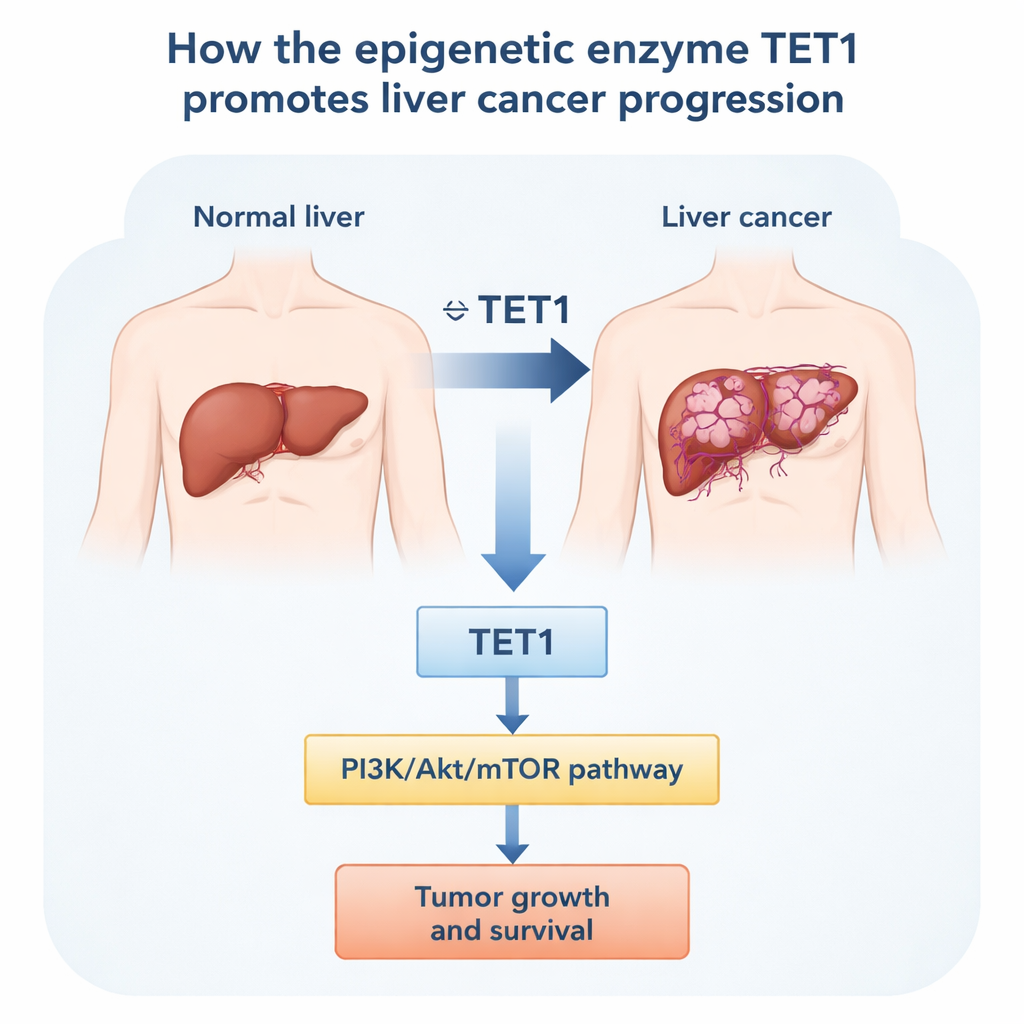
Wyłączenie TET1 hamuje komórki nowotworowe
Następnie zespół sprawdził, co się dzieje, gdy obniżyć poziom TET1 w komórkach raka wątroby hodowanych w laboratorium. Używając małych fragmentów RNA do wyciszenia genu TET1, znacznie zredukowali jego poziom w kilku ludzkich liniach komórkowych raka wątroby, w tym w liniach związanych z zakażeniem wirusem zapalenia wątroby typu B. Po stłumieniu TET1 komórki dzieliły się wolniej, tworzyły mniej kolonii i wykazywały wyraźne objawy stresu. Analizy cytometrii przepływowej ujawniły, że więcej komórek zatrzymało się we wczesnej fazie G1 cyklu komórkowego, zamiast przechodzić do podziału. Równocześnie wzrosła frakcja komórek przechodzących apoptozę, czyli zaprogramowaną śmierć komórki. Efekty te obserwowano zarówno w typowych komórkach raka wątroby, jak i w linii pozytywnej na HBV, co wskazuje, że TET1 pomaga podtrzymywać przeżywalność i ciągły wzrost w różnych kontekstach raka wątroby.
Szlak wzrostu pod kontrolą TET1
Aby odkryć, w jaki sposób TET1 wywiera ten wpływ, badacze przeanalizowali, które geny różnią się między normalnymi komórkami wątroby a komórkami nowotworowymi. Tysiące genów wykazywało różnice, a wiele z nich skupiało się w znanych obwodach regulujących wzrost i przeżycie. Jednym z wyróżniających się szlaków był PI3K/Akt/mTOR — centralny łańcuch sygnałowy, którego wiele nowotworów używa do zwiększania metabolizmu, oporności na śmierć komórki i unikania terapii. Analizy baz danych wykazały, że poziomy TET1 rosły wraz z kluczowymi składnikami tego szlaku, a spadały w odwrotnej korelacji do PTEN, naturalnego hamulca aktywności PI3K/Akt. Gdy TET1 został wyciszony w komórkach raka wątroby, zmniejszyły się aktywowane, „fosforylowane” formy PI3K, Akt i szczególnie mTOR. Leczenie komórek inhibitorem chemicznym blokującym aktywność enzymów z rodziny TET również zmniejszyło fosforylację Akt i mTOR. Wyniki te sugerują, że aktywność enzymatyczna TET1 — jego zdolność do przekształcania znaczników DNA — wpływa na kaskadę PI3K/Akt/mTOR, przesuwając równowagę w stronę wzrostu i przeżycia zamiast hamowania.
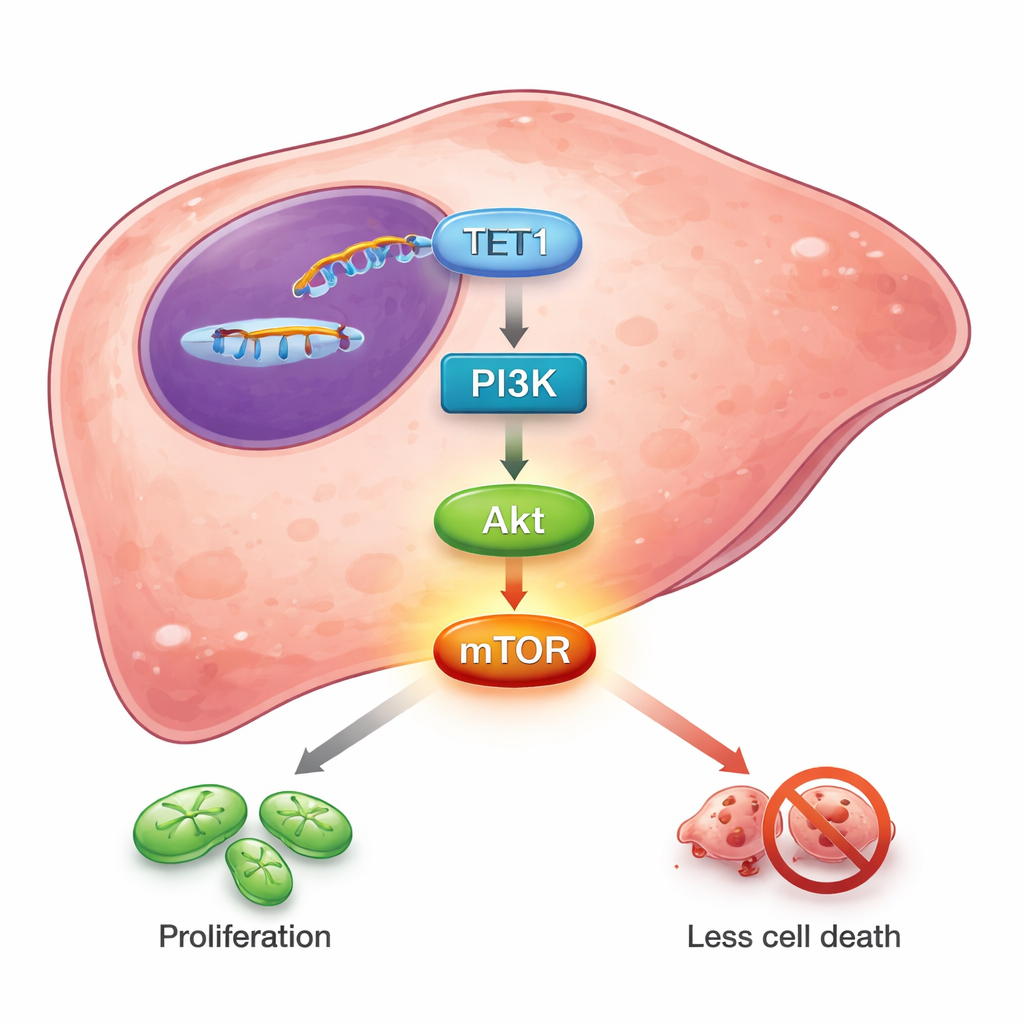
Od wglądu molekularnego do możliwych terapii
Podsumowując, praca ta ukazuje TET1 jako kluczowego sprzymierzeńca guzów wątroby, a nie jako ich obrońcę. Wysoki poziom TET1 pomaga komórkom raka wątroby proliferować i unikać śmierci, częściowo poprzez utrzymywanie włączonego szlaku PI3K/Akt/mTOR. U pacjentów większa ilość TET1 w guzach wiąże się z bardziej zaawansowaną chorobą i gorszymi wynikami. Dla czytelnika niebędącego specjalistą przesłanie jest takie: enzym cicho edytujący chemiczne znaczniki na DNA może w istotny sposób decydować o tym, czy komórki raka wątroby przeżyją czy zginą. Projektując leki hamujące TET1 lub łącząc takie związki z istniejącymi terapiami ukierunkowanymi na PI3K/Akt, przyszłe terapie mogą odciąć istotne wsparcie dla guzów wątroby i poprawić przeżywalność osób z tą trudną chorobą.
Cytowanie: Qi, S., Chen, M., Ding, Z. et al. TET1 suppresses hepatocellular carcinoma progression by modulating the PI3K/Akt signaling pathways. Sci Rep 16, 5791 (2026). https://doi.org/10.1038/s41598-026-36334-3
Słowa kluczowe: rak wątroby, TET1, epigenetyka, PI3K Akt mTOR, rak wątrobowokomórkowy