Clear Sky Science · pl
Przezwyciężanie oporności biofilmu Candida albicans na leki dzięki synergii azoli i soforolipidów
Dlaczego uporczywe infekcje grzybicze mają znaczenie
Każdy, kto miał przewlekłą infekcję drożdżakową, cewnik centralny w szpitalu lub implant medyczny, może być narażony na Candida albicans — powszechny grzyb, który staje się niebezpieczny, gdy tworzy trudne do leczenia społeczności zwane biofilmami. Te śluzowate warstwy chronią drobnoustroje przed wieloma najskuteczniejszymi lekami przeciwgrzybiczymi, pozwalając infekcjom utrzymywać się i czasami stawać się zagrażającymi życiu. Opisywane tu badanie szuka nowego sposobu na przełamanie tych barier poprzez łączenie istniejących leków z naturalną, mydlaną cząsteczką produkowaną przez drożdże.
Ukryta tarcza na powierzchniach medycznych
Candida albicans może przylegać do tkanek i urządzeń medycznych, a następnie rozwijać się w ustrukturyzowane biofilmy — gęste warstwy komórek spajane przez samodzielnie wytwarzaną matrycę z cukrów, białek i DNA. W tej twierdzy grzyb zwalnia metabolizm i wypompowuje leki na zewnątrz, więc środki, które łatwo zabijają wolno pływające komórki, ledwo działają na komórki żyjące w biofilmie. Leki azolowe, takie jak flukonazol i itrakonazol, są filarem terapii przeciwgrzybiczej, ale wobec dojrzałych biofilmów często wymagają znacznie wyższych dawek, co może powodować skutki uboczne i nadal nie usuwać infekcji w całości. Klinicyści coraz częściej stają przed infekcjami opartymi na biofilmach i jednocześnie opornymi, co podkreśla potrzebę cząsteczek pomocniczych mogących osłabić sam biofilm.
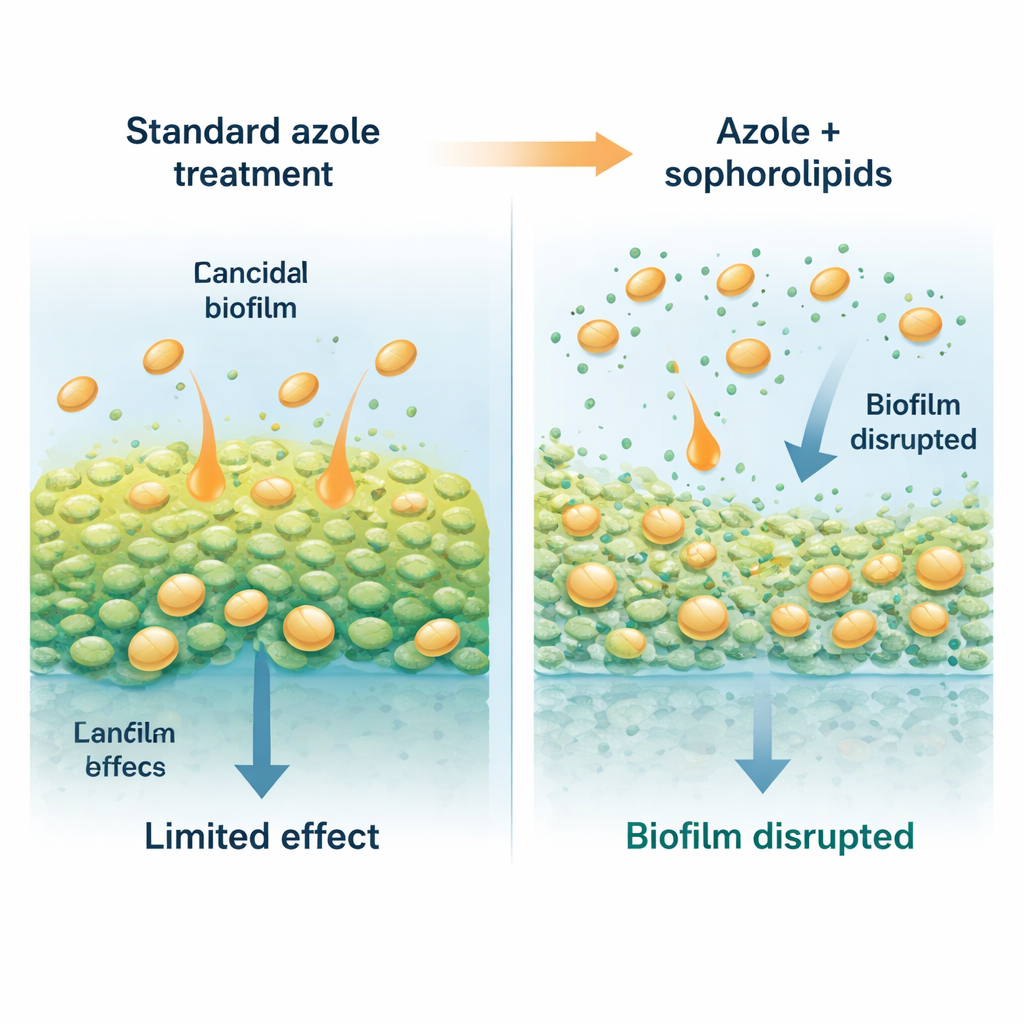
Mydlane pomocniki od przyjaznego drożdża
Naukowcy zwrócili się ku soforolipom, naturalnym, biodegradowalnym surfaktantom — cząsteczkom zachowującym się nieco jak bardzo łagodne detergenty — produkowanym przez niektóre niepatogenne drożdże. Te molekuły mają hydrofilową głowę cukrową i oleisty ogon, co pozwala im osiadać na powierzchniach i granicach faz. W badaniu użyto drożdża Starmerella riodocensis do wytworzenia mieszaniny soforolipidów, która następnie została oczyszczona i przeanalizowana. Same soforolipidy nie zabijały wolno pływających komórek Candida nawet w wysokich dawkach, ale silnie zakłócały zdolność grzyba do tworzenia i utrzymywania biofilmów. Młode, dopiero formujące się biofilmy były szczególnie wrażliwe, a nawet uformowane przez 24 godziny biofilmy można było przerzedzić i osłabić po ekspozycji na oczyszczone soforolipidy.
Współpraca z istniejącymi lekami przeciwgrzybiczymi
Głównym pytaniem było, czy soforolipidy mogą poprawić działanie standardowych azoli. Zespół testował kombinacje soforolipidów z trzema szeroko stosowanymi azolami: flukonazolem, itrakonazolem i ketokonazolem. Gdy eksponowali biofilmy na te mieszanki, odkryli, że niektóre pary dawały efekt większy niż suma ich indywidualnych działań — działały synergistycznie, co oznacza, że kombinacja była silniejsza niż można by oczekiwać po każdym składniku osobno. Najbardziej wyróżniała się para itrakonazol plus soforolipidy. W przypadku opornych, uprzednio uformowanych biofilmów ilość itrakonazolu potrzebna do zmniejszenia biofilmu o połowę spadła nawet do szesnastokrotnie, podczas gdy wymagana dawka soforolipidów także zmalała wielokrotnie w porównaniu z użyciem samych soforolipidów. Kombinacje z flukonazolem i ketokonazolem przyniosły bardziej umiarkowane korzyści, co sugeruje, że chemiczna natura poszczególnych leków wpływa na to, jak bardzo zyskują one dzięki „wsparciu” surfaktantu.
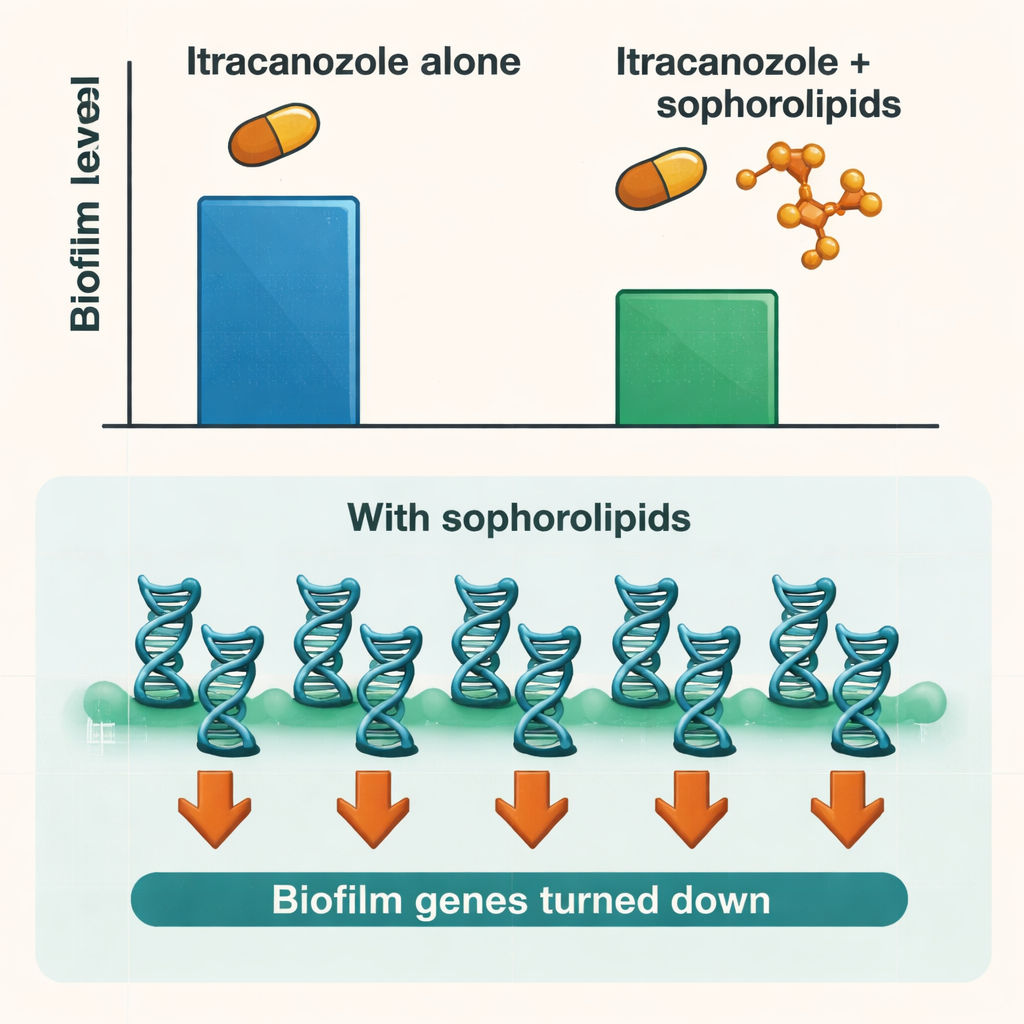
Wyciszanie programu biofilmowego grzyba
Aby zrozumieć, co działo się wewnątrz komórek grzyba, badacze zbadali aktywność kluczowych genów Candida zaangażowanych w przyleganie do powierzchni, wzrost w postaci strzępek i budowę matrycy biofilmu. Leczenie samymi soforolipidami obniżało aktywność wielu z tych genów, zwłaszcza tych kontrolujących najwcześniejsze etapy adhezji i przejście z formy drożdżopodobnej do nitkowatej. Gdy komórki zsynchronizowano w specyficznym etapie cyklu komórkowego sprzyjającym tworzeniu biofilmu, efekty wyciszania genów były jeszcze silniejsze. To sugeruje, że soforolipidy nie tylko mechanicznie zmywają biofilm; zakłócają także własny program biologiczny grzyba odpowiedzialny za budowę i utrzymanie tej ochronnej społeczności.
Obietnica łagodniejszych, skuteczniejszych terapii
Badanie kończy się wnioskiem, że soforolipidy z Starmerella riodocensis mogą działać jako bezpieczni, ukierunkowani na biofilm partnerzy dla leków azolowych, a kombinacja itrakonazol–soforolipidy jest szczególnie skuteczna. Ponieważ soforolipidy wykazują niską toksyczność w komórkach ssaczych i głównie osłabiają strukturę biofilmu oraz sieci genów, zamiast bezpośrednio zatruwać grzyba, mogą pozwolić lekarzom na stosowanie niższych dawek konwencjonalnych leków przy jednoczesnym usuwaniu uporczywych infekcji na urządzeniach i tkankach. Dla pacjentów taka inteligentna terapia skojarzona mogłaby w przyszłości przełożyć się na leczenie bardziej skuteczne wobec opornych biofilmów Candida i łagodniejsze dla reszty organizmu.
Cytowanie: Jayasekara, L.C.B., Watchaputi, K., Butkinaree, C. et al. Overcoming Candida albicans biofilm drug resistance via azole-sophorolipid synergy. Sci Rep 16, 5963 (2026). https://doi.org/10.1038/s41598-026-36278-8
Słowa kluczowe: biofilm Candida, antygrzybicze azole, soforolipidy, synergia leków, oporność na środki przeciwdrobnoustrojowe