Clear Sky Science · pl
Słabo nadzorowana segmentacja gruczołów jelita grubego poprzez uczenie samonadzorowane i etykietowanie pseudoz użyciem uwagi
Dlaczego ma to znaczenie dla diagnozy raka
Kiedy patolog ogląda pod mikroskopem wycinek jelita grubego, jednym z najważniejszych wskazówek dotyczących zaawansowania nowotworu jest kształt i organizacja drobnych rurkowatych struktur zwanych gruczołami. Ręczne obrysowywanie każdego gruczołu jest czasochłonne, kosztowne i trudne do ustandaryzowania pomiędzy ośrodkami. W badaniu pokazano, jak sztuczna inteligencja może nauczyć się odtwarzać te obrysy niemal tak dobrze jak eksperci, przy jednoczesnym wykorzystaniu znacznie mniej szczegółowego oznakowania przez ludzi, co potencjalnie przyspiesza i usprawnia diagnozowanie raka jelita grubego.
Problem z rysowaniem każdego maleńkiego obrysu
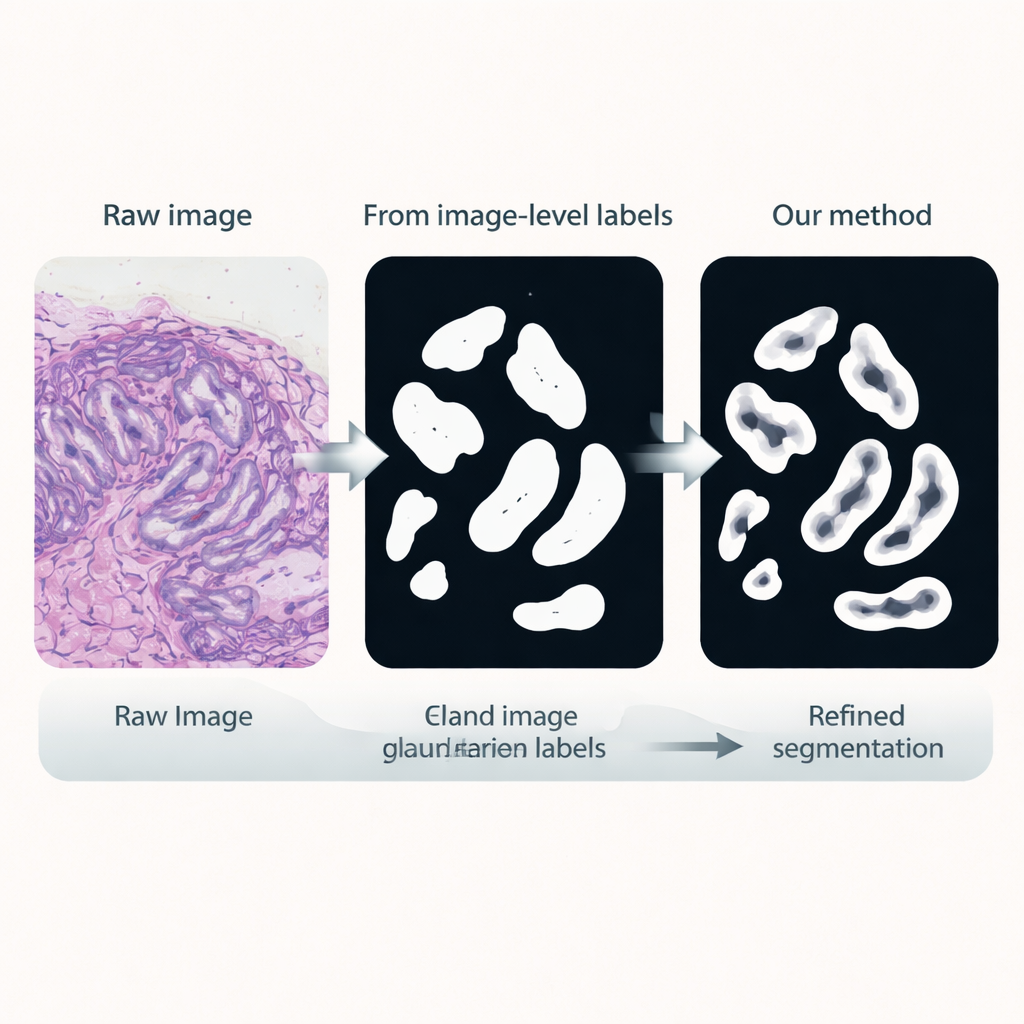
Rak jelita grubego jest jednym z najczęściej występujących i najgroźniejszych nowotworów na świecie, a gradacja jego zaawansowania w dużej mierze zależy od wyglądu gruczołów. W tkance zdrowej lub we wczesnym stadium gruczoły przypominają uporządkowane, okrągłe rurki; w agresywnych guzach stają się poszarpane, zlane lub ledwie rozpoznawalne. Komputery można wyszkolić do segmentacji, czyli „pokolorowania” każdego gruczołu, aby umożliwić automatyczne pomiary, ale tradycyjne systemy głębokiego uczenia wymagają pracochłonnych obrysów piksel po pikselu wykonanych przez ekspertów. W praktyce klinicznej znacznie łatwiej uzyskać proste etykiety na poziomie obrazu, na przykład czy fragment tkanki zawiera gruczoły, albo czy jest łagodny czy złośliwy.
Nauka SI na nieoznakowanych i słabo oznakowanych preparatach
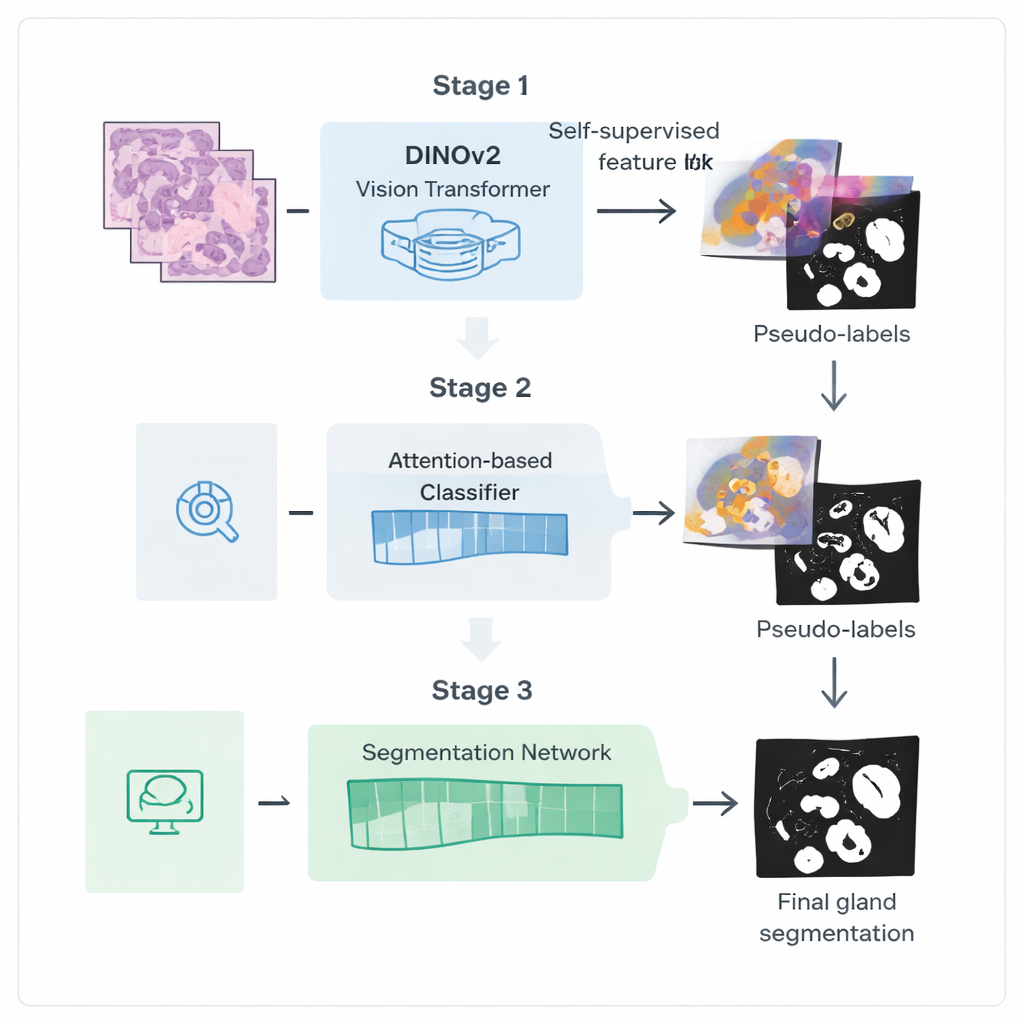
Autorzy proponują trzyetapowy proces treningowy zaprojektowany tak, aby wydobyć więcej informacji z tych słabszych etykiet. Najpierw rozpoczynają od potężnego modelu widzenia o nazwie DINOv2, pierwotnie trenowanego na zdjęciach naturalnych, i eksponują go na tysiącach nieoznakowanych obrazów wycinków jelita grubego. Poprzez zadanie modelowi dopasowywania różnych widoków tej samej łatki tkanki do siebie, uczy się on cech wizualnych dostrojonych do kolorów i tekstur preparatów histologicznych bez potrzeby adnotacji. Ten etap tworzy wyspecjalizowany „enkoder”, który przekształca surowe obrazy w bogate wewnętrzne reprezentacje wychwytujące struktury przypominające gruczoły.
Pozwolenie SI, by pokazała, na co patrzy
W drugim etapie ten enkoder jest podłączany do sieci klasyfikacyjnej, która potrzebuje jedynie etykiet na poziomie obrazu, na przykład informacji, czy gruczoły są obecne. Mechanizm uwagi wewnątrz sieci uczy się przypisywać większe wagi tym obszarom obrazu, które mają największe znaczenie dla decyzji. Mapy uwagi skutecznie podświetlają miejsca, w których sieć „uważa”, że znajdują się gruczoły. Badacze przekształcają te miękkie mapy cieplne w przybliżone maski binarne za pomocą mieszania i progowania, a następnie oczyszczają je dalej techniką wygładzania probabilistycznego zwaną warunkowym polem losowym (Conditional Random Field). Wynikiem jest zestaw dopracowanych pseudoadnotacji: generowanych komputerowo obrysów gruczołów, które nie są idealne, ale wystarczająco dobre, by poprowadzić bardziej wyspecjalizowany model segmentacyjny.
Wyostrzanie granic gruczołów
W trzecim etapie wyspecjalizowana sieć segmentacyjna jest trenowana przy użyciu tych pseudoadnotacji jako zastępników ręcznych oznaczeń. Wykorzystuje ona dostrojony enkoder, dodając lekki dekoder, który przekształca cechy z powrotem w szczegółową maskę gruczołu. Kluczowe znaczenie ma funkcja straty używana podczas treningu, która kładzie dodatkowy nacisk na granice: błędy zniekształcające brzegi gruczołów są karane mocniej niż drobne pomyłki wewnątrz obszaru. Takie podejście uwzględniające granice sprzyja otrzymywaniu ostrych, anatomicznie realistycznych obrysów, niezbędnych do dokładnego pomiaru kształtu i separacji gruczołów.
Jak dobrze to działa w praktyce?
Zespół przetestował swoją metodę na dwóch standardowych zestawach danych dotyczących tkanek jelita grubego. W zbiorze GlaS ich podejście słabo nadzorowane nie tylko przewyższyło inne metody używające ograniczonych etykiet, ale w kilku miarach zbliżyło się do klasycznych systemów w pełni nadzorowanych, opartych na pełnych adnotacjach pikselowych, a nawet je przewyższyło. W trudniejszym zbiorze CRAG, zawierającym wysoce nieregularne, złośliwe gruczoły, wydajność spadła dla wszystkich metod, jednak nowa rama nadal przewyższała innych konkurentów korzystających z słabych etykiet i zmniejszała różnicę względem modeli w pełni nadzorowanych. Badania ablacjne wykazały, że każdy element—samonadzorowane dostrajanie, etykietowanie pseudoz oparte na uwadze z postprocessingiem oraz strata uwzględniająca granice—wnosił istotny wkład w osiągane rezultaty.
Co to oznacza dla przyszłych narzędzi patologicznych
Dla czytelnika niebędącego specjalistą kluczowy wniosek jest taki, że praca ta wskazuje kierunek rozwoju systemów SI, które mogą dostarczać wysokiej jakości, precyzyjne względem granic mapy mikroskopowych struktur gruczołowych, opierając się głównie na prostych etykietach na poziomie preparatu, już powszechnych w archiwach szpitalnych. Ograniczając zależność od żmudnego ręcznego obrysowywania, podejście może uczynić zaawansowaną gradację obrazową i analizę ilościową bardziej wykonalnymi w wielu ośrodkach, pomagając patologom diagnozować raka jelita grubego bardziej spójnie i efektywnie, a potencjalnie rozciągając zastosowania na inne typy tkanek i struktur w przyszłości.
Cytowanie: Wen, H., Wu, Y., Huang, D. et al. Weakly supervised colorectal gland segmentation through self-supervised learning and attention-based pseudo-labeling. Sci Rep 16, 5771 (2026). https://doi.org/10.1038/s41598-026-36256-0
Słowa kluczowe: rak jelita grubego, cyfrowa patologia, segmentacja gruczołów, słabo nadzorowane uczenie, widzenie samonadzorowane