Clear Sky Science · pl
Przeznaczenie dapagliflozyny w nanogelu polimerowym do terapii raka jelita grubego
Dlaczego lek na cukrzycę może pomóc w walce z rakiem jelita
Rak jelita grubego jest jedną z głównych przyczyn zgonów związanych z rakiem na świecie, a wielu pacjentów nadal doświadcza nawrotów mimo operacji i chemioterapii. Badanie to bada nieoczekiwanego sprzymierzeńca w walce z tą chorobą: dapagliflozynę, powszechnie stosowaną tabletkę na cukrzycę typu 2. Pakuąc ten lek w maleńkie miękkie cząsteczki, które w żołądku przechodzą w delikatny żel, badacze dążą do dostarczenia większej ilości substancji do jelita grubego — miejsca rozwoju guzów — przy jednoczesnym zachowaniu podobnej dawki doustnej jak w obecnych tabletkach.
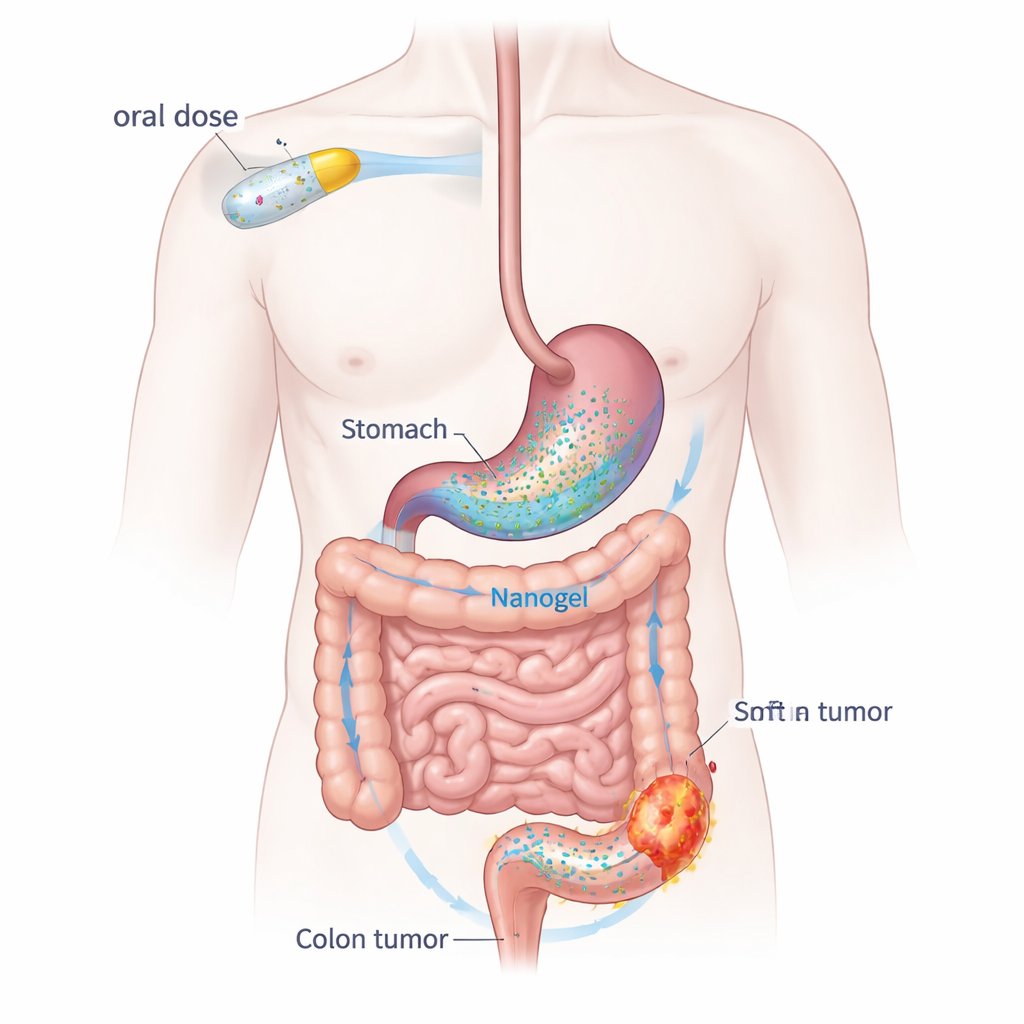
Przekształcenie codziennej tabletki w ładunek celowany w raka
Dapagliflozyna zwykle działa w nerkach, obniżając poziom cukru we krwi, ale ma też działanie przeciwzapalne i hamujące wzrost komórek — dwa procesy, od których zależą nowotwory. Sama w sobie substancja słabo rozpuszcza się w wodzie i jest szybko usuwana z organizmu. Aby temu zaradzić, zespół opracował system dostarczania „nanogelu” z użyciem dwóch polimerów przypominających składniki spożywcze: alginianu sodu, pozyskanego z alg, oraz poliwinylowego alkoholu, powszechnie stosowanego, biokompatybilnego zagęszczacza. Lek jest uwięziony we wnętrzu nanocząstek o wielkości około jednej dziesięciotysięcznej milimetra. Gdy te cząsteczki napotkają kwas żołądkowy, osiadają i spajają się w miękką masę hydrożelową, która utrzymuje się, a następnie stopniowo uwalnia lek w miarę przemieszczania się w stronę okrężnicy.
Zwiększenie rozpuszczalności leku i opóźnienie jego wypłukiwania
Naukowcy najpierw zoptymalizowali proces wytwarzania cząstek, dopracowując proporcje dwóch polimerów, tak aby nanocząstki pozostawały małe, równomierne i stabilne w cieczy. Potwierdzili, że lek dobrze osiadł w sieci polimerowej i częściowo przekształcił się z postaci krystalicznej w bardziej amorficzną, która zwykle lepiej się rozpuszcza. W cieczach testowych naśladujących soki żołądkowe i jelitowe, formulacja nanogelu zwiększyła pozorną rozpuszczalność dapagliflozyny o około 1,7–1,8 razy w porównaniu z surowym lekiem. Monitorując tempo wymywania leku, nanogel wykazał łagodny profil „powolnego uwalniania” przez kilka godzin, zamiast gwałtownego wyrzutu obserwowanego przy czystym leku. Jedna z receptur, oznaczona jako F2, utworzyła zwartą, trwałą galaretę, która utrzymywała się co najmniej przez dwie godziny w warunkach kwaśnych, jednocześnie stopniowo uwalniając substancję czynną.
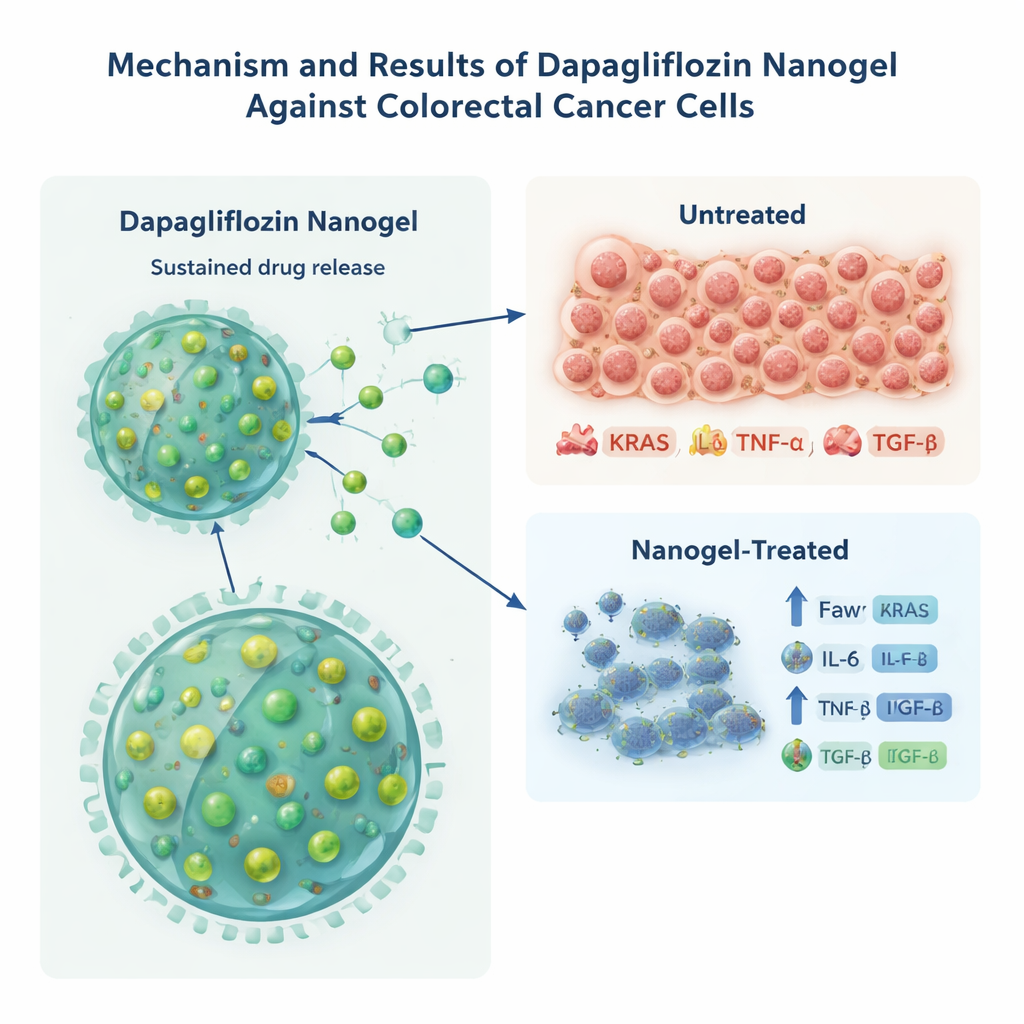
Wywoływanie stresu w komórkach nowotworowych w laboratorium
Aby sprawdzić, czy ta nowa forma dapagliflozyny może faktycznie szkodzić komórkom nowotworowym, zespół przetestował ją na komórkach raka jelita grubego HCT-116 hodowanych w naczyniach laboratoryjnych. W porównaniu z taką samą ilością wolnego leku, wersja w nanogelu zabijała komórki nowotworowe przy niższych stężeniach, zmniejszając dawkę potrzebną do zahamowania wzrostu komórek o połowę o około jedną trzecią. Badacze przeanalizowali również molekuły związane z agresywnym zachowaniem guza i przewlekłym stanem zapalnym, w tym KRAS (kluczowy białkowy czynnik napędzający raka) oraz białka sygnałowe IL-6, TNF-α i TGF-β. Komórki traktowane nanogelem z lekiem wykazały znacznie niższe poziomy wszystkich tych markerów niż komórki traktowane wolnym lekiem lub pustymi cząstkami, co sugeruje, że utrzymane narażenie przez nanocząstki skuteczniej wygasza sygnały związane z rakiem i zapaleniem. Ponieważ linia komórkowa już nosi stałą mutację KRAS, autorzy zastrzegają, że spadek białka KRAS może odzwierciedlać reakcje stresowe, a nie bezpośrednią korektę genetyczną, ale i tak świadczy o silnym wpływie biologicznym.
Zmienianie sposobu, w jaki organizm przetwarza lek
Zespół przeszedł następnie do badań na zwierzętach, podając szczuróm albo prostą zawiesinę proszku dapagliflozyny, albo zoptymalizowany nanogel, oba doustnie w tej samej dawce. W grupie otrzymującej nanogel maksymalne stężenia leku we krwi pojawiały się później i były niższe, ale lek utrzymywał się w krążeniu dłużej. Całkowita ekspozycja (mierzona jako pole pod krzywą) wzrosła umiarkowanie o około 7%, a pozorna okres półtrwania mniej więcej się podwoiła. Te zmiany oznaczają, że organizm doznaje łagodniejszej, przedłużonej dawki w czasie, zamiast ostrego skoku i szybkiego spadku. Takie zachowanie odpowiada projektowi żelu: zatrzymać lek w przewodzie pokarmowym, uwalniać go powoli i potencjalnie utrzymywać wyższe stężenia kąpiące dolne jelito i okrężnicę, gdzie powstają guzy.
Co to może znaczyć dla przyszłej opieki onkologicznej
Mówiąc prostymi słowami, badanie to doposaża dobrze znany lek przeciwcukrzycowy w nowy „kostium dostawczy”, aby mógł lepiej docierać i utrzymywać się przy guzach okrężnicy. Nanogel ułatwia rozpuszczanie leku, spowalnia jego ucieczkę z jelit i wydaje się zwiększać jego toksyczność wobec komórek raka jelita grubego przy jednoczesnym osłabieniu kluczowych sygnałów zapalnych i wzrostu. U szczurów przedłuża łagodnie obecność leku we krwi bez dramatycznego zwiększenia całkowitej dawki. Prace te są wciąż na wczesnym etapie — ograniczone do jednej linii komórkowej i krótkoterminowych badań na zwierzętach — i nie wykazały jeszcze bezpośredniego zmniejszenia guzów u żywych zwierząt czy ludzi. Mimo to stanowią szczegółową podstawę do ponownego zastosowania dapagliflozyny jako elementu przyszłych terapii raka jelita grubego, wykorzystując inteligentne doustne nanogele, by przekształcić znaną tabletkę w bardziej ukierunkowane narzędzie przeciwnowotworowe.
Cytowanie: Abdullah, S., Thiab, S., Altamimi, A.A. et al. A repurposing Dapagliflozin via polymeric nanogels for colorectal cancer therapy. Sci Rep 16, 5625 (2026). https://doi.org/10.1038/s41598-026-36232-8
Słowa kluczowe: rak jelita grubego, ponowne zastosowanie leku, nanocząsteczki, doustne podawanie leku, dapagliflozyna