Clear Sky Science · pl
Krajowy monitoring genomowy izolatów Klebsiella pneumoniae opornych na karbapenemy i kolistynę z krwiobiegu w Tajlandii (2020–2024)
Wzrastają śmiertelne zakażenia krwi
Szpitale na całym świecie mierzą się z niepokojącym trendem: zwykłe bakterie, które kiedyś ustępowały najsilniejszym antybiotykom, stają się niemal niemożliwe do wyleczenia. Badanie koncentruje się na Klebsiella pneumoniae, mikrobie mogącym dostać się do krwiobiegu i powodować zagrażające życiu zakażenia, i śledzi, jak ewoluowała w całej Tajlandii, zdobywając odporność nawet na leki ostatniej linii. Zrozumienie, gdzie te superbakterie się rozprzestrzeniają i jak unikają leków, jest kluczowe dla ochrony pacjentów, wspierania decyzji klinicznych i kształtowania polityki zdrowia publicznego.
Śledzenie szpitalnego superbakterium w całym kraju
Naukowcy przeanalizowali 227 próbek Klebsiella pneumoniae pobranych z krwi pacjentów w szpitalach w całej Tajlandii w latach 2020–2024. Próbki pochodziły z krajowej sieci nadzoru, która rutynowo zbiera dane o zakażeniach opornych na leki. Badania laboratoryjne wykazały, że ponad 93% tych izolatów z krwi było opornych na karbapenemy — potężną klasę antybiotyków stosowaną często, gdy inne leki zawodzą. Niepokojąco, prawie jedna trzecia szczepów opornych na karbapenemy była także oporna na kolistynę, jedno z ostatnich dostępnych lekarstw. Łącząc standardowe testy wrażliwości z sekwencjonowaniem całych genomów, zespół mógł ustalić nie tylko, które leki zawiodły, lecz także jakie genetyczne sztuczki bakterie stosują, by przetrwać.
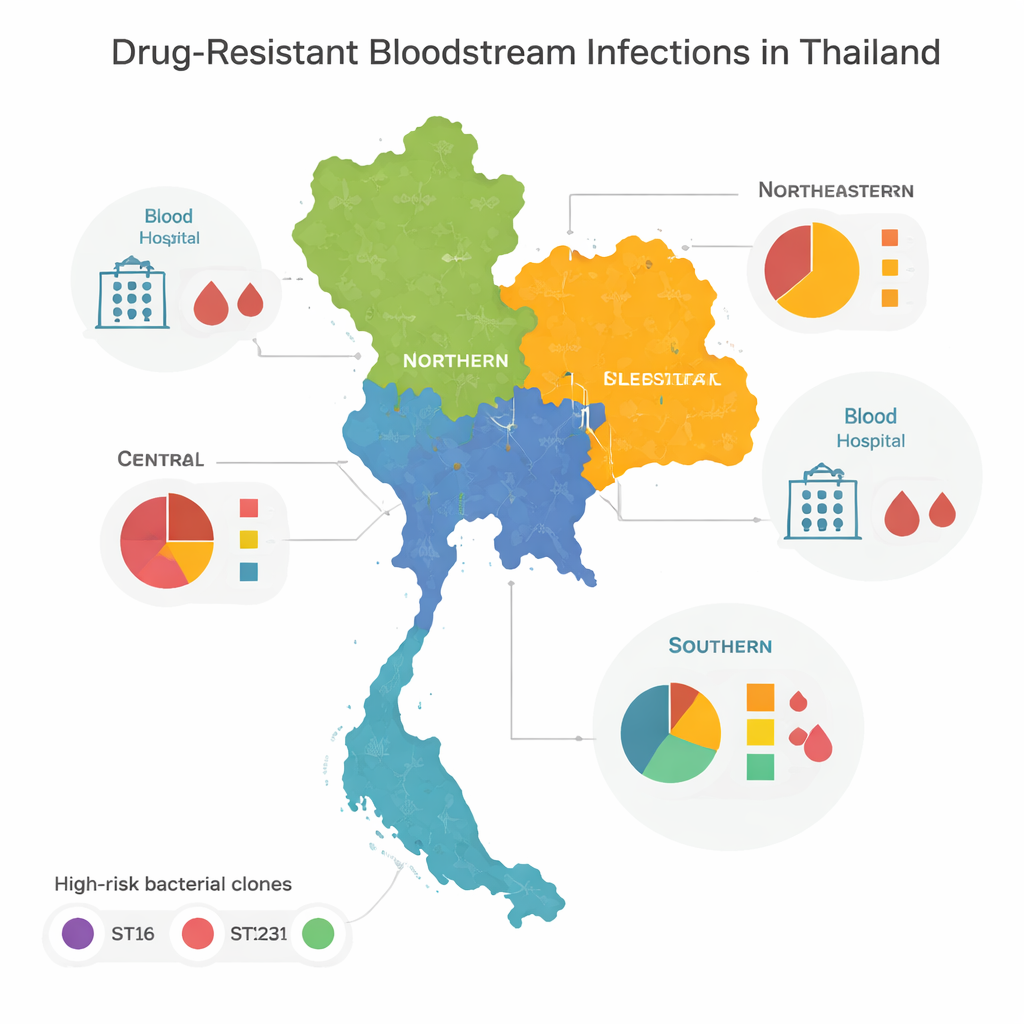
Wysokiego ryzyka klony i wzory regionalne
Porównanie genomów wykazało, że większość opornych bakterii należała do kilku „wysokiego ryzyka” rodzin lub klonów, znanych na całym świecie z wywoływania ognisk szpitalnych. Trzy z nich — określane jako ST16, ST147 i ST231 — dominowały w regionie centralnym, północnym i północno‑wschodnim Tajlandii. Klony te szeroko się rozprzestrzeniły między regionami, co sugeruje częste przemieszczanie pacjentów, personelu lub samych bakterii między placówkami. Południowa część kraju wyglądała inaczej: zamiast dominacji kilku typów występowało duże zróżnicowanie linii bakterii, z wieloma obserwowanymi tylko raz. Ta różnorodność wskazuje na bardziej złożoną mieszankę lokalnych ognisk, źródeł środowiskowych i ruchu przez granice, zamiast jednego czy dwóch dominujących klonów.
Jak bakterie przechytrzają antybiotyki
Badanie ujawniło, jak te bakterie kumulują wiele mechanizmów oporności. Wiele szczepów ST16 i ST231 niosło geny znane jako blaNDM i blaOXA, które kodują enzymy rozkładające karbapenemy zanim leki zdążą zadziałać. Niektóre miały też zmiany w błonie zewnętrznej ograniczające wnikanie leku, co w połączeniu dawało bardzo wysoki poziom oporności. Szczepy ST231 często niosły dodatkowo gen rmtF1, który blokuje istotną grupę leków — aminoglikozydy — jeszcze bardziej zawężając opcje terapeutyczne. ST147 wyróżniał się genetyczną elastycznością: mieszał i dopasowywał różne geny oporności i plazmidy — małe, mobilne pierścienie DNA — co czyniło go potencjalnym hubem szerzenia cech oporności na inne bakterie.
Załamanie leków ostatniej linii i ukryte zagrożenia
Najbardziej alarmujące odkrycie dotyczyło oporności na kolistynę, lek zarezerwowany na sytuacje desperackie. Niektóre rzadkie rodziny bakterii niosły geny mcr, które mogą przeskakiwać między gatunkami na plazmidach i bezpośrednio powodować oporność na kolistynę. Inne, zwłaszcza w klonie ST16, były oporne na kolistynę mimo braku znanych genów oporności lub mutacji. To sugeruje, że naukowcy nie odkryli jeszcze wszystkich sposobów, jakimi bakterie mogą neutralizować ten lek ostatniej linii. Zespół zidentyfikował też hiperwirusyjne szczepy — bakterie szczególnie zdolne do wywoływania ciężkich chorób — w tym jedną linię, która łączyła wysoką wirulencję z opornością na wszystkie badane karbapenemy, co stanowi szczególnie niebezpieczne połączenie.
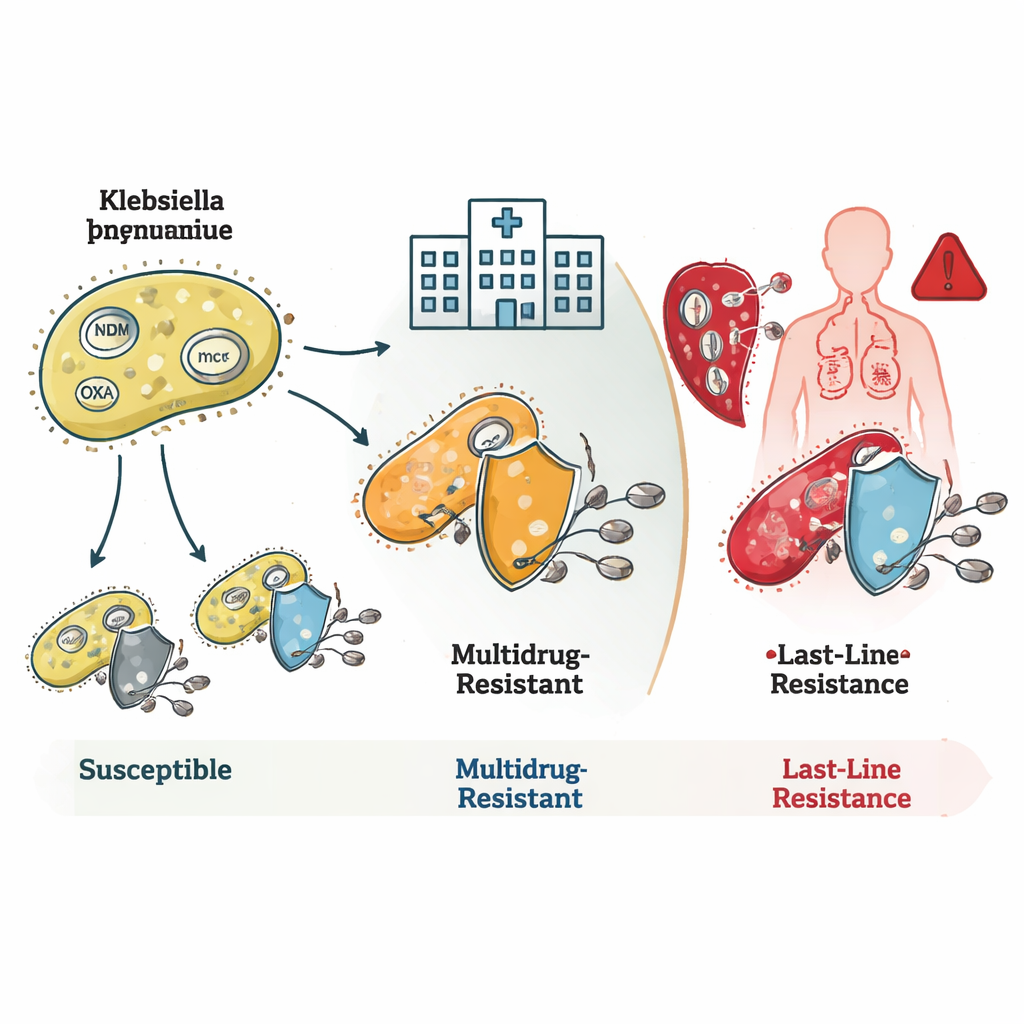
Dlaczego monitoring genomowy ma znaczenie
Aby zrozumieć, jak zmiany genetyczne przekładają się na rzeczywiste porażki leczenia, badacze zastosowali modele statystyczne łączące konkretne geny oporności z wynikami badań laboratoryjnych. Geny takie jak blaNDM-1 i ich bliscy krewni wykazały bardzo silne powiązania z opornością na karbapenemy, potwierdzając ich kluczową rolę w zawodzeniu terapii. Jednak w przypadku kolistyny większość opornych bakterii nie miała rozpoznanych markerów oporności, co wskazuje na ukryte mechanizmy, które nadal trzeba odkryć. Autorzy argumentują, że rutynowe stosowanie sekwencjonowania całych genomów w nadzorze szpitalnym może działać jak radar wczesnego ostrzegania: wykrywać pojawiające się klony wysokiego ryzyka, śledzić ich przemieszczanie między regionami i granicami oraz kierować szybkie działania kontroli zakażeń.
Co to oznacza dla pacjentów i polityki
Dla osoby niebędącej specjalistą przesłanie jest ostre, ale jasne: niektóre zakażenia krwi w Tajlandii wywoływane są teraz przez bakterie odporne na niemal wszystkie leki, jakie dysponują lekarze, a kilka groźnych rodzin tych drobnoustrojów szerzy się na dużą skalę. Jednocześnie badanie pokazuje, że przy odpowiednich narzędziach — krajowym pobieraniu próbek, analizie genetycznej i szybkim udostępnianiu danych — systemy opieki zdrowotnej mogą przewidywać te zagrożenia i się do nich dostosować. Rozszerzenie monitoringu genomowego, opracowanie szybkich testów molekularnych oraz zaostrzenie kontroli zakażeń może pomóc spowolnić postęp tych superbakterii i zyskać czas na rozwój nowych terapii i szczepionek.
Cytowanie: Krobanan, K., Kamjumphol, W., Leethongdee, P. et al. Nationwide genomic surveillance of carbapenem- and colistin-resistant Klebsiella pneumoniae bloodstream isolates in Thailand (2020–2024). Sci Rep 16, 5853 (2026). https://doi.org/10.1038/s41598-026-36228-4
Słowa kluczowe: oporność na środki przeciwdrobnoustrojowe, Klebsiella pneumoniae, zakażenie krwi, monitoring genomowy, opieka zdrowotna w Tajlandii