Clear Sky Science · pl
Nieprawidłowo eksprymowane długie RNA niekodujące w różnicowaniu mezenchymalnych komórek macierzystych pochodzących z tkanki tłuszczowej do komórek podobnych do jądra miażdżystego
Dlaczego ból pleców i ukryte RNA mają znaczenie
Ból dolnej części pleców jest jedną z głównych przyczyn nieobecności w pracy lub wizyt u lekarza, a jednym z jego głównych sprawców jest stopniowy rozkład miękkich poduszek między kręgami, zwanych krążkami międzykręgowymi. W każdym krążku znajduje się żelopodobne jądro miażdżyste, które zależy od zdrowej populacji wyspecjalizowanych komórek, aby zachować elastyczność i odpowiednie nawodnienie. Wraz z utratą lub starzeniem się tych komórek krążek wysycha, zapada się i może wywołać przewlekły ból. Naukowcy badają, czy komórki macierzyste — uniwersalne komórki zdolne przekształcić się w różne tkanki — można poprowadzić tak, by zastąpiły zużyte komórki krążka. W tym badaniu zadano zaskakująco podstawowe pytanie: które „ciche” sygnały genetyczne włączają się, gdy komórki macierzyste są kierowane na drogę tworzenia komórek krążka, i jak można by je wykorzystać do ulepszenia przyszłych terapii?
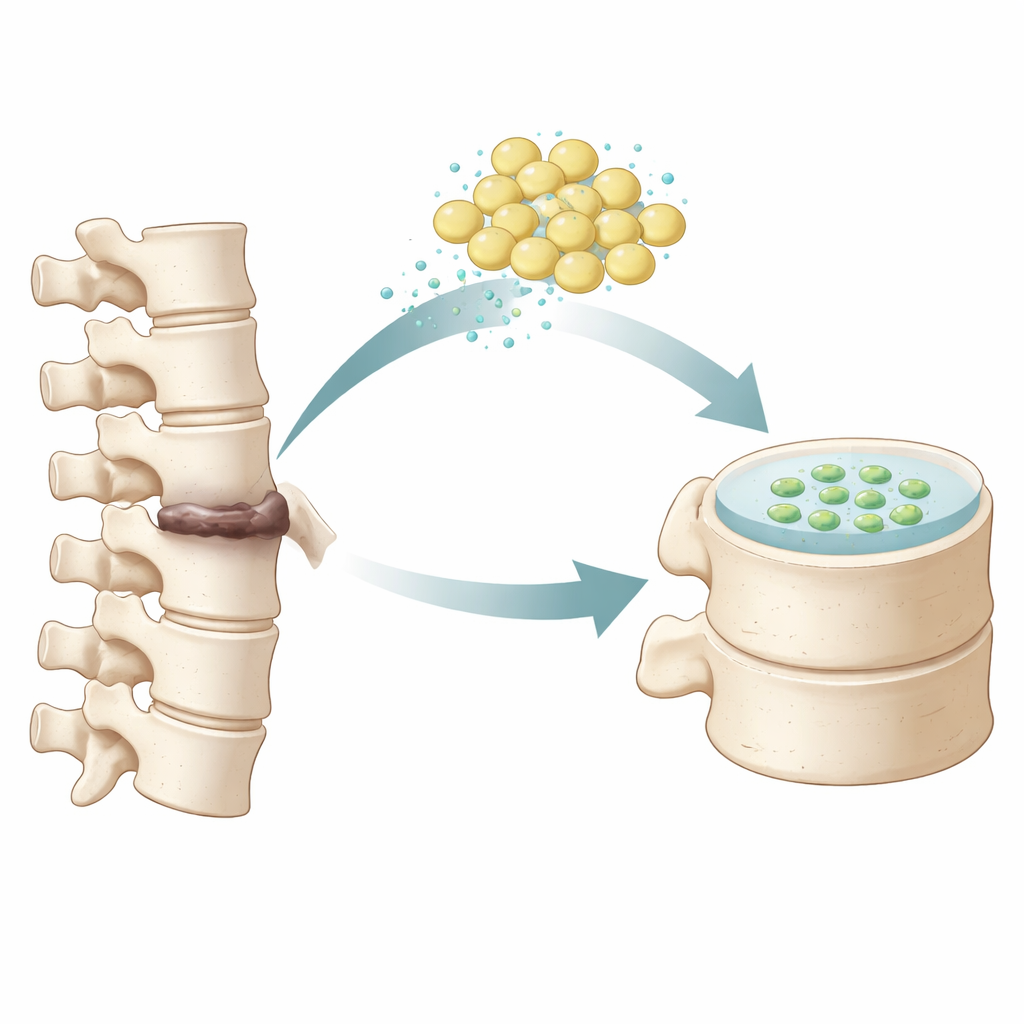
Z tkanki tłuszczowej do naprawy krążka
Naukowcy skupili się na ludzkich mezenchymalnych komórkach macierzystych pochodzących z tkanki tłuszczowej, które pobiera się z tłuszczu i które są stosunkowo łatwe do pozyskania. W laboratorium hodowali te komórki w małych trójwymiarowych pelletach i eksponowali je na starannie dobraną mieszaninę czynników wzrostu, które wcześniejsze prace wykazały jako zdolne skierować komórki ku tożsamości podobnej do jądra miażdżystego. Przez kilka tygodni zespół monitorował pellety za pomocą standardowych barwień mikroskopowych i znakowania fluorescencyjnego. Leczone komórki zaczęły przypominać i zachowywać się bardziej jak komórki żelowego jądra zdrowego krążka, wytwarzając charakterystyczne składniki tkanki krążka, takie jak kolagen i aggrekan, oraz uruchamiając kluczowe geny związane z tożsamością jądra miażdżystego.
Podsłuchiwanie „tła rozmów” w komórce
Ponad znanymi genami kodującymi białka, komórki produkują także długie RNA niekodujące — odcinki RNA, które nie tworzą białek, ale mogą subtelnie kierować tym, które geny są włączane lub wyłączane. Molekuły te wyłaniają się jako ważni dyrygenci w orkiestrze różnicowania komórek. Wykorzystując wysokoprzepustowe sekwencjonowanie RNA, zespół zmierzył zarówno tradycyjne mRNA, jak i długie RNA niekodujące w komórkach macierzystych przechodzących różnicowanie w kierunku komórek podobnych do jądra miażdżystego, i porównał je z nierozróżnionymi komórkami kontrolnymi. Odkryto rozległe przeorganizowanie krajobrazu genetycznego: aktywność 500 długich RNA niekodujących i 601 mRNA uległa zmianie — niektóre stały się bardziej obfite, inne zostały przyciszone, gdy komórki przemieszczały się w stronę stanu podobnego do jądra miażdżystego.
Kluczowe szlaki i główne regulatory
Aby nadać sens tej obszernej liście zmieniających się molekuł, naukowcy użyli narzędzi bioinformatycznych grupujących geny według ich ról w komórce. Wiele zmienionych genów związanych było z budową i organizacją macierzy zewnątrzkomórkowej — sieci kolagenu, cukrów i innych cząsteczek, które nadają tkance krążka właściwości amortyzujące. Analiza szlaków wskazała na szlak sygnałowy PI3K–Akt oraz systemy kontrolujące wewnętrzny szkielet komórkowy jako szczególnie aktywne podczas różnicowania, sugerując, że te obwody pomagają napędzać przemianę komórek macierzystych pochodzących z tłuszczu w komórki przypominające jądro miażdżyste. Poprzez budowę sieci interakcji zespół zidentyfikował zestaw długich RNA niekodujących, w tym MALAT1, MEG3, GAS5, ZNF331 oraz RNA powiązane z JARID2, które wydają się zajmować centralne miejsce w komunikacji między regulatorowymi RNA, mRNA i mikroRNA. Te węzły mogą działać jako główne przełączniki kontrolujące, jak skutecznie komórki macierzyste angażują się w los podobny do komórek krążka.
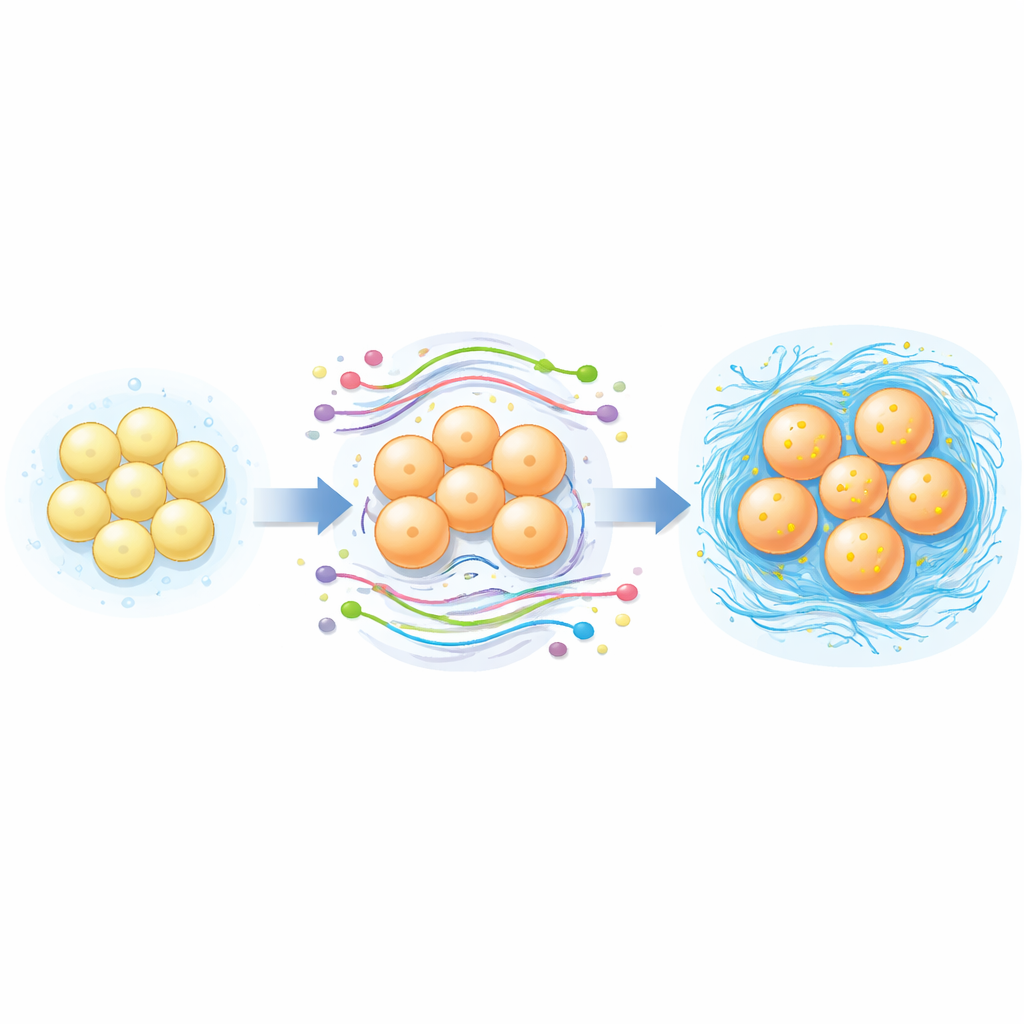
Wskazówki dla lepszych terapii komórkami macierzystymi
Degradacja krążków międzykręgowych stwarza szczególnie surowe środowisko — kwaśne, ubogie w tlen i bogate w cząsteczki zapalne — które może uniemożliwić przeżycie przeszczepionych komórek macierzystych. Mapując, które RNA i szlaki ulegają zmianie podczas pomyślnej konwersji komórek tłuszczowych w laboratorium w komórki podobne do jądra miażdżystego, to badanie dostarcza katalogu molekularnych celów, które można by modulować, aby zwiększyć przeżywalność i wydajność komórek terapeutycznych u pacjentów. Choć prace przeprowadzono in vitro i na ograniczonej liczbie próbek, stanowią one fundament pod przyszłe eksperymenty, które mogłyby np. modyfikować konkretne długie RNA niekodujące lub szlaki sygnałowe w celu wzmocnienia regeneracji krążka.
Co to oznacza dla osób z bólem pleców
Dla osób żyjących z przewlekłym bólem dolnej części pleców te odkrycia nie zmienią leczenia jutro, ale pomagają wypełnić istotną brakującą część: jak komórki macierzyste uczą się stawać dokładnie tym typem komórek krążka potrzebnym do naprawy. Badanie pokazuje, że ta przemiana jest kierowana nie tylko przez dobrze znane geny, ale także przez złożoną sieć długich RNA niekodujących i szlaków sygnałowych kształtujących zachowanie komórek. Dekodując tę ukrytą warstwę kontroli, naukowcy zbliżają się do projektowania mądrzejszych terapii komórkami macierzystymi, które lepiej wytrzymają wrogie środowisko uszkodzonego krążka i bardziej niezawodnie odbudują jego amortyzujące jądro, potencjalnie oferując długotrwałą ulgę w przyszłości.
Cytowanie: Zhu, J., Jin, L., Jin, K. et al. Aberrantly expressed long noncoding RNAs in adipose-derived mesenchymal stem cells differentiation to nucleus pulposus-like cells. Sci Rep 16, 8029 (2026). https://doi.org/10.1038/s41598-026-36219-5
Słowa kluczowe: degradacja krążków międzykręgowych, terapia komórkami macierzystymi, komórki jądra miażdżystego, długie RNA niekodujące, sekwencjonowanie RNA