Clear Sky Science · pl
Kubosomalne nanocząstki likopenu jako nowa platforma zwiększająca właściwości antyoksydacyjne i przeciwnowotworowe z badaniem dokowania molekularnego
Moc pomidora w maleńkim opakowaniu
Wielu ludzi słyszało, że jedzenie pomidorów może pomagać w ochronie przed rakiem dzięki czerwonemu pigmentowi zwanemu likopenem. Jednak sam likopen trudno przyswaja się w organizmie i trafia do guzów mało efektywnie. W tym badaniu zbadano sprytne rozwiązanie: zapakowanie likopenu w ultramaleńkie cząstki lipidowe zwane kubosomami, aby sprawdzić, czy to „skompresowane działanie pomidora” lepiej zwalcza komórki raka jelita grubego w warunkach laboratoryjnych.
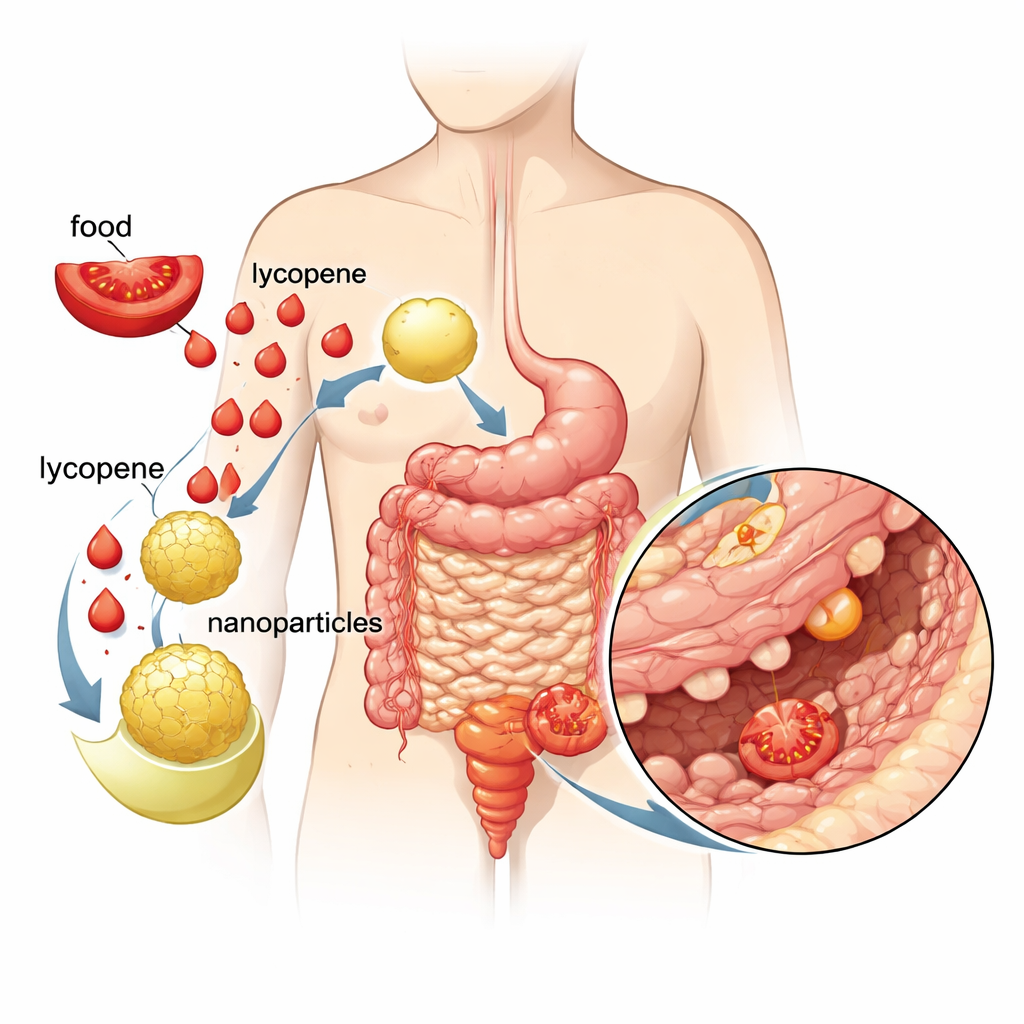
Dlaczego zwykły likopen nie wystarcza
Likopen jest silnym naturalnym antyoksydantem występującym w pomidorach, arbuzach i innych czerwonych owocach. Neutralizuje szkodliwe cząsteczki znane jako wolne rodniki, które uszkadzają DNA, białka i tłuszcze w komórkach i przyczyniają się do chorób przewlekłych, takich jak rak czy choroby serca. Jednak likopen jest wyjątkowo lipofilowy i słabo rozpuszcza się w płynach na bazie wody, takich jak te w układzie trawiennym. W rezultacie jedynie niewielka część tego, co spożywamy, trafia do krwiobiegu i na docelowe tkanki. Słaba rozpuszczalność i niestabilność ograniczają praktyczne zastosowania likopenu jako terapii, mimo dobrze udokumentowanego potencjału ochronnego.
Budowanie lepszego nośnika
Aby pokonać te przeszkody, badacze stworzyli kubosomalne nanocząstki — maleńkie, miękkie cząstki z biokompatybilnych lipidów i stabilizatorów, które układają się w gąbczastą, plastry miodu przypominającą strukturę wewnętrzną. Te struktury mogą zamykać lipofilne molekuły, takie jak likopen, chronić je przed degradacją i uwalniać stopniowo. W tej pracy zespół skutecznie załadował likopen do kubosomów o wielkości około 150 nanometrów, przy czym większość likopenu była efektywnie uwięziona wewnątrz. Testy wykazały, że ponad trzy czwarte likopenu uwolniło się do roztworu w ciągu 15 minut, co stanowi dramatyczną poprawę w porównaniu z samym likopenem, który niemal się nie rozpuszcza w wodzie.
Badanie siły antyoksydacyjnej i przeciwnowotworowej
Naukowcy porównali następnie zwykły likopen i likopen w kubosomach na dwa sposoby. Po pierwsze zmierzyli, jak dobrze każdy z nich neutralizuje wolne rodniki za pomocą standardowych testów antyoksydacyjnych. W obu testach nano‑opakowany likopen wymagał znacznie mniejszych dawek, aby osiągnąć ten sam efekt antyoksydacyjny, co wskazuje na znacznie silniejsze działanie. Po drugie poddali ludzkie komórki raka jelita grubego (HT‑29) działaniu obu form. W standardowym teście żywotności stwierdzono, że likopen w kubosomach zabijał komórki nowotworowe skuteczniej niż wolny likopen, co oznacza, że do zahamowania wzrostu komórek potrzebne były niższe dawki. Eksperymenty z użyciem cytometrii przepływowej wykazały, że forma nanopartykułowa przesuwała znacznie więcej komórek w fazę spoczynku, w której przestają się dzielić, oraz wywoływała wyraźny wzrost zaprogramowanej śmierci komórek (apoptozy) w porównaniu z komórkami nieleczonymi.
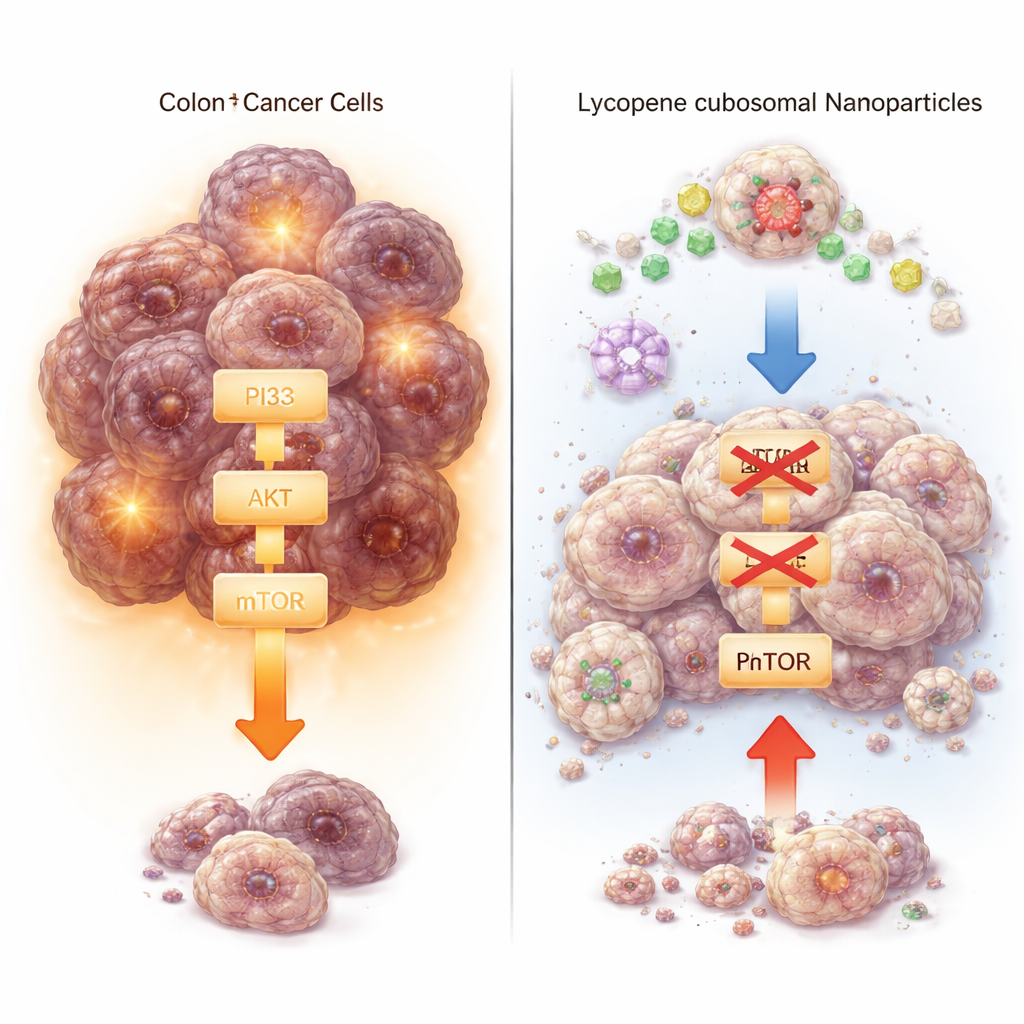
Zajrzeć do obwodów sterujących komórką
Poza prostym zliczaniem przeżywających komórek zespół zbadał kluczowe molekularne przełączniki sterujące wzrostem i śmiercią. Skoncentrowano się na szlaku PI3K–AKT–mTOR, łańcuchu sygnałów, którego komórki nowotworowe często używają, by przeżyć i się namnażać, oraz na białkach, które promują lub blokują samobójstwo komórkowe. Za pomocą testów ekspresji genów i pomiarów białek stwierdzono, że zarówno zwykły likopen, jak i likopen w kubosomach obniżały poziomy PI3K, AKT, mTOR oraz białka przeżycia Bcl‑2, jednocześnie zwiększając poziom enzymu wykonującego śmierć — kaspazy‑3. Zmiany te były konsekwentnie silniejsze w przypadku formy kubosomalnej. Symulacje dokowania komputerowego wspierały hipotezę, że likopen może dopasować się do aktywnej kieszeni PI3K, sugerując bezpośredni sposób, w jaki mógłby zakłócać ten szlak wzrostu.
Co to może oznaczać dla przyszłych terapii
Mówiąc prościej, opakowanie likopenu w kubosomalne nanocząstki ułatwiło jego rozpuszczanie, zwiększyło stabilność i znacząco wzmocniło działanie w testach laboratoryjnych. Forma nano nie tylko skuteczniej neutralizowała szkodliwe cząsteczki, ale też wyłączała sygnały wzrostu w komórkach nowotworowych i zachęcała te komórki do samobójczej zagłady. Chociaż wyniki pochodzą z hodowli komórkowych i modeli komputerowych — a nie od pacjentów — wskazują na obiecującą strategię: wykorzystanie inteligentnych, lipidowych nanonośników, by przekształcić znany z diety związek w ukierunkowanego pomocnika przeciw rakowi jelita grubego. Jeśli przyszłe badania na zwierzętach i badania kliniczne potwierdzą te korzyści i bezpieczeństwo, kubosomalne likopeny mogłyby uzupełniać istniejące terapie, oferując łagodniejszy, bardziej naturalny sposób wsparcia obrony antyoksydacyjnej i osłabiania komórek nowotworowych.
Cytowanie: Alsunbul, M., El-Masry, T.A., El-Bouseary, M.M. et al. Cubosomal nanoparticles of lycopene as a novel platform for enhancement in antioxidant and anticancer properties with a molecular docking study. Sci Rep 16, 5941 (2026). https://doi.org/10.1038/s41598-026-36217-7
Słowa kluczowe: likopen, nanocząstki, rak jelita grubego, antyoksydanty, nośniki leków