Clear Sky Science · pl
Barwniki distyrylowe BODIPY podstawione grupą pirydyniową i bromem do fotodynamicznej terapii ukierunkowanej na mitochondria
Rozświetlając komórki nowotworowe od środka
Terapia fotodynamiczna to leczenie nowotworów wykorzystujące specjalne leki aktywowane światłem, które zabijają komórki guza, przy jednoczesnym ograniczeniu uszkodzeń tkanek zdrowych. W pracy tej badana jest nowa rodzina barwników fluorescencyjnych zaprojektowanych tak, by trafiać do „elektrowni” komórki — mitochondriów — i pod wpływem światła dalekoczerwonego generować toksyczne formy tlenu zdolne zniszczyć komórki nowotworowe. Badanie pokazuje zarówno potencjał, jak i ograniczenia inżynierii takich barwników na poziomie molekularnym.
Dlaczego celować w „stacje energetyczne” komórki?
Mitochondria są kluczowe dla wytwarzania energii i odgrywają rolę w decydowaniu o przeżyciu lub śmierci komórki. Komórki nowotworowe mają zwykle bardziej spolaryzowaną błonę mitochondrialną niż komórki zdrowe, co sprawia, że przyciągają dodatnio naładowane cząsteczki znacznie silniej. Badacze wykorzystali to, dołączając dodatnio naładowaną grupę pirydyniową do dobrze znanego szkieletu barwnika BODIPY. Takie rozwiązanie pomaga kierować barwniki do mitochondriów, gdzie wyzwolone światłem reakcje chemiczne mogą wyrządzić maksymalne szkody komórkom nowotworowym przy ograniczonym wpływie na inne struktury.
Projektowanie bardziej inteligentnych barwników aktywowanych światłem
Zespół opracował trzy blisko spokrewnione barwniki, nazwane PyBHI, PyBMI i PyBBrI, które różnią się głównie liczbą atomów bromu (brak, jeden lub dwa). Wszystkie mają długą, rozciągniętą strukturę przesuwającą absorpcję i emisję światła w kierunku bliskiej podczerwieni — korzystne pasmo, w którym światło przenika głębiej w tkanki. W teorii barwniki te mogą korzystać z dwóch wewnętrznych ścieżek prowadzących do stanu wzbudzonego „trypletowego”, który wytwarza reaktywny tlen singletowy: jednej wspomaganej przez ciężkie atomy bromu i drugiej wynikającej z przejściowego przesunięcia ładunku wewnątrz cząsteczki. 
Gdy teoria spotyka eksperyment
Mimo eleganckiego projektu szczegółowe testy wykazały, że barwniki nie generują tlenu singletowego tak wydajnie, jak oczekiwano. Przy użyciu sond chemicznych tracących barwę po reakcji z tlenem singletowym badacze zmierzyli bardzo niskie wydajności generowania tlenu dla wszystkich trzech barwników, z jedynie umiarkowaną poprawą przy wzroście liczby atomów bromu. Ultraszybkie eksperymenty laserowe wyjaśniły przyczynę: po absorpcji światła barwniki szybko wchodzą w stany ze przesunięciem ładunku, które głównie relaksują się bezzwrotnie jako ciepło zamiast przechodzić do pożądanego stanu trypletowego. W bromowanych wersjach ciężkie atomy otwierają co prawda drogę do trypletu, ale ta ścieżka jest znacznie wolniejsza niż konkurencyjne straty energii, co ogranicza ogólną wydajność.
Celowanie w mitochondria guzów w żywych komórkach
Sytuacja zmienia się w środowisku biologicznym. W hodowlach ludzkich komórek raka piersi (MCF-7) i szyjki macicy (HeLa) wszystkie trzy barwniki wykazały, za pomocą mikroskopii konfokalnej, silne gromadzenie się w mitochondriach, współlokalizując się ze standardowym barwnikiem mitochondrialnym. Testy toksyczności w ciemności wskazały, że bez światła barwniki są w dużej mierze nieszkodliwe. Pod naświetlaniem czerwonym światłem z kolei di-bromowany barwnik PyBBrI wywołał znaczną śmierć komórek nowotworowych, przy czym niskie stężenia w nanomolach zmniejszały żywotność komórek o połowę. Pozostałe dwa barwniki były znacznie mniej efektywne. 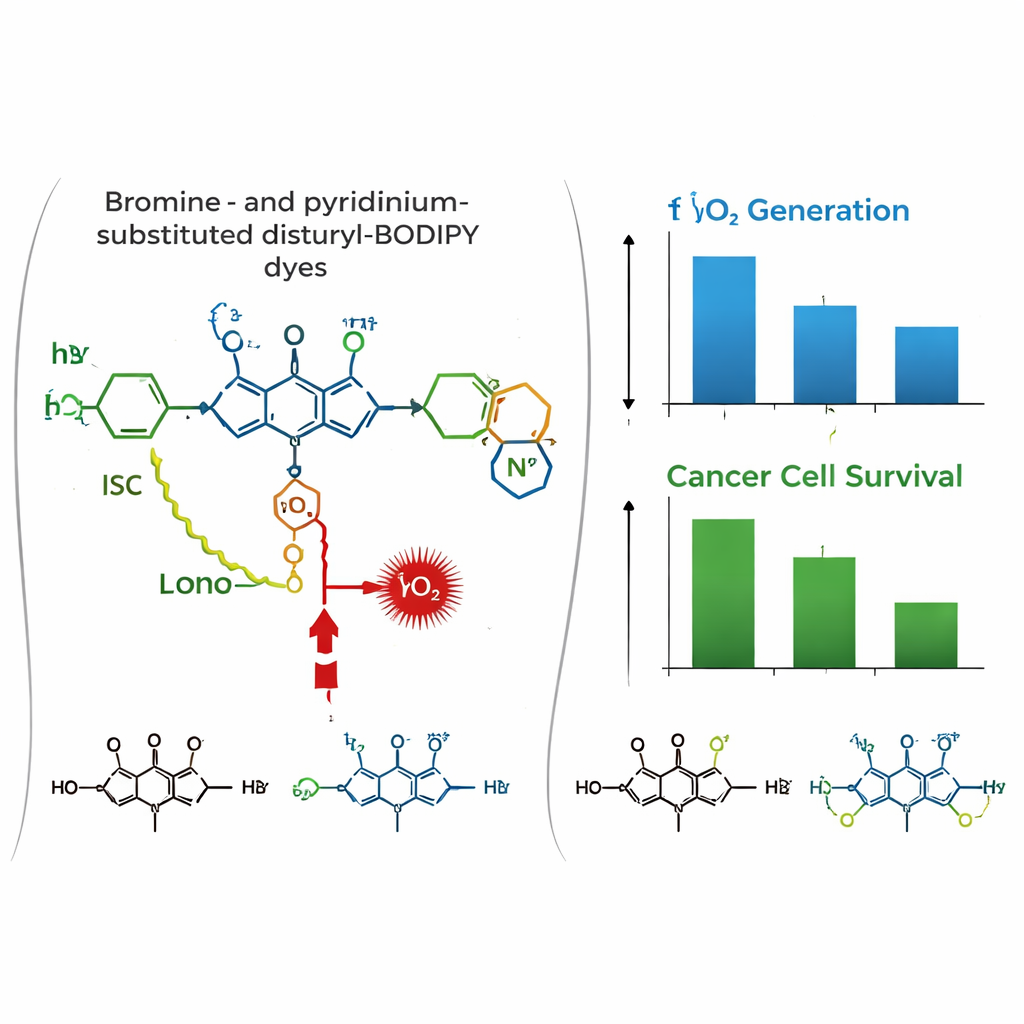
Co to oznacza dla przyszłych terapii nowotworowych
Dla laika kluczowa wiadomość jest taka, że drobne modyfikacje chemiczne mogą drastycznie zmieniać zachowanie leków aktywowanych światłem, a ich wydajność w rzeczywistych komórkach może być lepsza — lub gorsza — niż przewidywana na podstawie podstawowych pomiarów. W tym przypadku najsilniej zmodyfikowany barwnik, PyBBrI, wykazywał jedynie umiarkowaną produkcję reaktywnego tlenu w probówce, lecz okazał się wysoce skuteczny przeciwko komórkom nowotworowym po dotarciu do ich mitochondriów. Praca podkreśla zarówno znaczenie kierowania leków do wrażliwych struktur wewnątrz komórek nowotworowych, jak i złożoność przewidywania efektywności fotodynamicznej. Wskazuje drogę do następnej generacji terapii ukierunkowanych na mitochondria, które wykorzystują światło w bliskiej podczerwieni do selektywnego „włączania” chemii niszczącej komórki dokładnie tam, gdzie jest to potrzebne.
Cytowanie: Kim, C., Badon, I.W., Jo, J. et al. Pyridinium- and bromine-substituted distyryl-BODIPY dyes for mitochondria-targeted photodynamic therapy. Sci Rep 16, 6789 (2026). https://doi.org/10.1038/s41598-026-36213-x
Słowa kluczowe: terapia fotodynamiczna, barwniki ukierunkowane na mitochondria, BODIPY, tlen singletowy, komórki nowotworowe