Clear Sky Science · pl
Rozwój dorosłych osobników Dirofilaria immitis u myszy NSG, wykrywanie mikroRNA pochodzącego od pasożyta i analiza porównawcza izolatów laboratoryjnych
Dlaczego heartwormy mają znaczenie poza gabinetem weterynaryjnym
Choroba wywoływana przez heartwormy jest najbardziej znana jako zagrożenie dla psów, ale pasożyt wywołujący ją, Dirofilaria immitis, może też zakażać koty, a nawet ludzi. W miarę jak pasożyty rozszerzają zasięg w wyniku zmian klimatu i narastającej odporności na leki, trudniej i drożej będzie chronić zwierzęta domowe. W badaniu opisano nową, wydajną metodę badania heartwormów w warunkach laboratoryjnych przy użyciu specjalnej linii myszy, oraz pokazano, jak drobne sygnały genetyczne we krwi mogą pewnego dnia pomóc w wcześniejszym wykrywaniu zakażeń i wskazywaniu lepszych terapii. 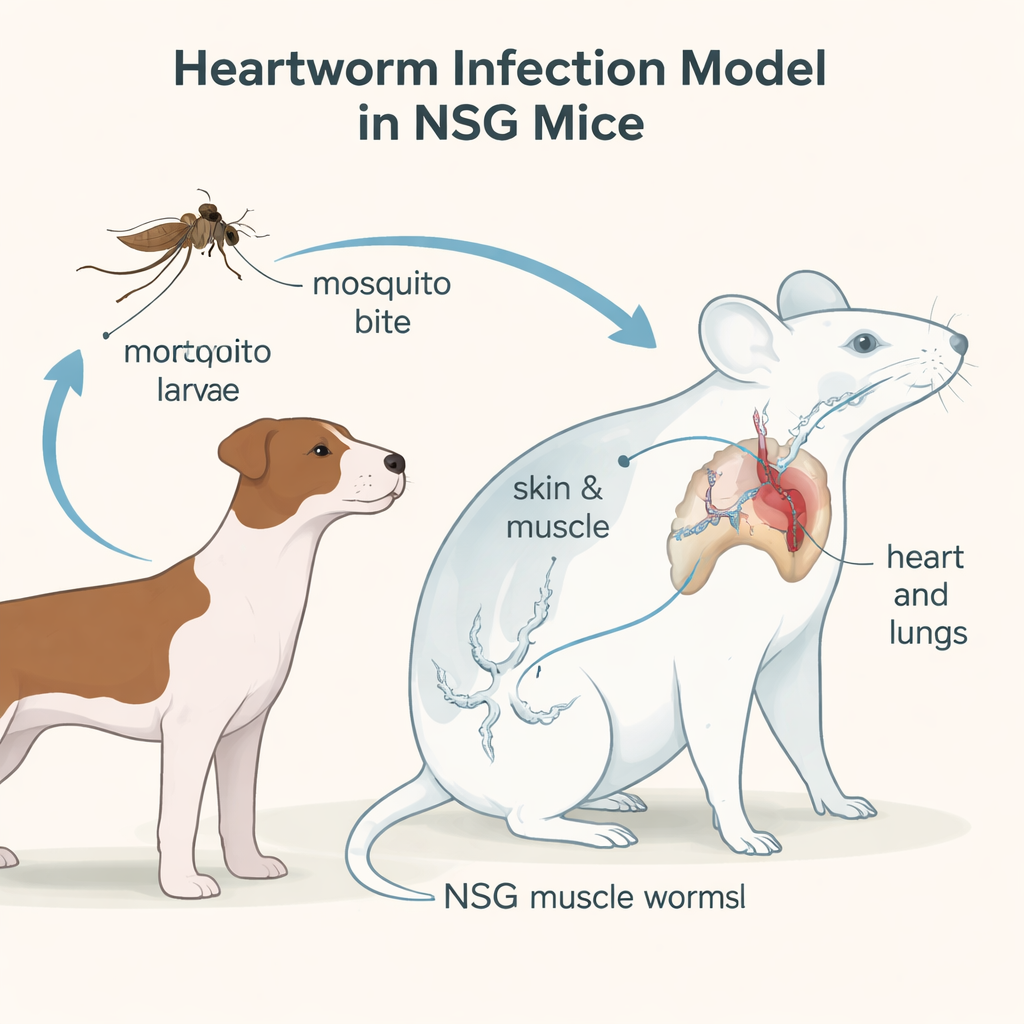
Maleńki robak o długiej wędrówce
Heartwormy mają zaskakująco złożony cykl życia. Zaczynają jako mikroskopijne larwy przenoszone przez komary, dostają się do nowego gospodarza przez ugryzienie, potem migrują pod skórą i przez mięśnie, aż w końcu osiedlają się w naczyniach krwionośnych serca i płuc. Do tej pory tylko psy w sposób niezawodny wspierały pełny rozwój tych robaków, co oznaczało, że testowanie nowych leków czy diagnostyki wymagało dużych, długotrwałych i kosztownych badań na psach. Naukowcy postanowili sprawdzić, czy myszy immunodeficyentne NSG — zwierzęta, których układ odpornościowy jest w dużej mierze wyłączony — mogą być gospodarzem heartwormów od wczesnych stadiów larwalnych aż do postaci dorosłej w sposób przypominający to, co dzieje się u psów.
Śledzenie robaków w sercu i płucach
Infekując myszy NSG laboratoryjnym szczepem heartwormów o nazwie JYD-34 i badając je przez niemal sześć miesięcy, zespół śledził, gdzie znajdowały się robaki i jak zmieniały się w czasie. Na początku larwy znajdowano w skórze i mięśniach, podobnie jak u psów. Później pojawiały się w jamach ciała i, po około 80 dniach, w sercu i płucach. Dokładne badania mikroskopowe wykazały, że zarówno samce, jak i samice przeszły główne etapy rozwojowe, osiągając rozmiary podobne do obserwowanych u psów i rozwijając w pełni ukształtowane organy rozrodcze. Jedna zasadnicza różnica polegała na tym, że nawet po prawie sześciu miesiącach samice u myszy nie uwolniły jeszcze następnego pokolenia mikroskopijnych potomków do krwiobiegu, co sugeruje, że może być potrzebny jakiś końcowy bodziec lub więcej czasu.
Co ujawniły organy i krew myszy
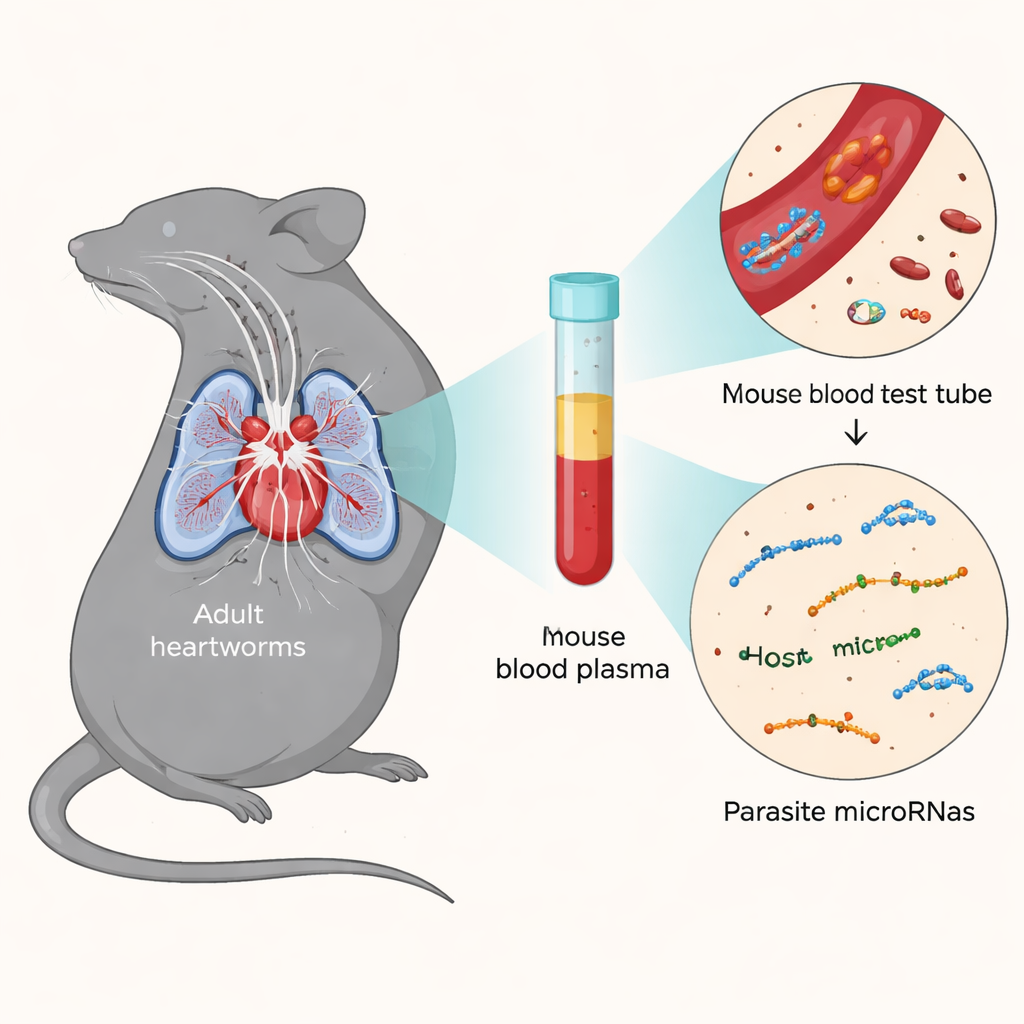
Mimo obecności dorosłych robaków w sercach i płucach, myszy NSG wykazywały jedynie łagodne zmiany tkankowe, z niewielkim stanem zapalnym i ograniczonymi oznakami uszkodzeń w płucach, nerkach i naczyniach krwionośnych. Kontrastuje to z ciężko zakażonymi psami, które mogą rozwijać kaszel, problemy z oddychaniem oraz poważne choroby serca i płuc. Ponieważ myszy NSG pozbawione są wielu mechanizmów odpornościowych, nie rozwijają pełnego obrazu choroby znanego ze zwierząt domowych, ale jednocześnie stanowią kontrolowany system do testowania działania leków na robaki bez komplikacji związanych z silną reakcją immunologiczną. Naukowcy zbadają również krew myszy pod kątem mikroRNA — krótkich fragmentów materiału genetycznego uwalnianych zarówno przez gospodarza, jak i pasożyta — i wykryli 31 odrębnych mikroRNA pochodzących od heartwormów oraz dziewięć mysich mikroRNA, które zmieniały się konsekwentnie w przebiegu zakażenia.
Sygnały wczesnego ostrzegania i różnice między szczepami
Odkrycie pasożytniczych mikroRNA we krwi myszy ma znaczenie, ponieważ robaki w tym czasie znajdowały się w stosunkowo wczesnych stadiach, które są trudne do wykrycia za pomocą dzisiejszych testów komercyjnych. Wiele z tych samych mikroRNA było również zgłaszanych u zakażonych psów, co sugeruje, że te drobne cząsteczki mogą służyć jako wiarygodne wczesne sygnały zakażenia. Zespół porównał także pięć różnych izolatów heartwormów, niektóre oporne, inne podatne na powszechnie stosowane leki zapobiegawcze. Wszystkie rozwijały się u myszy, ale nie zachowywały się identycznie: niektóre szczepy szybciej docierały do serca i płuc, podczas gdy jeden nie osiągnął tych miejsc w okresie trwania badania. Różnice te odzwierciedlają zmiany genetyczne i fenotypowe obserwowane w populacjach heartwormów w rzeczywistym świecie i podkreślają, dlaczego oporność na leki i niepowodzenia terapii mogą być tak złożone.
Co to oznacza dla zwierząt i ludzi
Pokazując, że myszy NSG mogą być gospodarzem heartwormów od zakaźnego stadium larwalnego aż po dojrzałe płciowo osobniki, oraz łącząc to z subtelnymi zmianami w narządach i charakterystycznymi sygnałami mikroRNA we krwi, badanie dostarcza wszechstronnego nowego modelu do badań nad heartwormami. Dla czytelników niebędących specjalistami kluczowy wniosek jest taki, że naukowcy mają teraz szybszy, bardziej etyczny sposób badania, jak heartwormy rosną, jak uszkadzają organizm, dlaczego niektóre szczepy są oporne na leki i jak wykrywać zakażenia wcześniej, korzystając z molekularnych odcisków palców we krwi. Z czasem ten model myszy i wykryte markery mikroRNA mogą przyczynić się do opracowania lepszych środków zapobiegawczych, bezpieczniejszych terapii i bardziej czułych testów chroniących zarówno zwierzęta, jak i opiekujących się nimi ludzi.
Cytowanie: Nakhale, M., Hess, J.A., Oliver, E. et al. Development of Dirofilaria immitis adult worms in NSG mice, detection of parasite-derived microRNA and comparative analysis of laboratory isolates. Sci Rep 16, 6764 (2026). https://doi.org/10.1038/s41598-026-36209-7
Słowa kluczowe: heartworm, Dirofilaria immitis, model myszy NSG, biomarkery mikroRNA, pasożyty oporne na leki