Clear Sky Science · pl
Promieniowanie γ wywołuje regionowo specyficzne zmiany podkomórkowe markerów stwardnienia zanikowego bocznego i otępienia czołowo‑skroniowego w mózgu świni
Dlaczego małe dawki promieniowania i mózgi świń mają znaczenie
Większość z nas postrzega promieniowanie jako wyłącznie szkodliwe, zwłaszcza dla mózgu. Jednak nasz świat wypełniony jest niskimi poziomami promieniowania pochodzącymi z badań medycznych, lotów samolotem i środowiska. Równocześnie naukowcy wciąż próbują rozwikłać przyczyny stwardnienia zanikowego bocznego (ALS), śmiertelnej choroby, która sparaliżowała gwiazdę baseballu Lou Gehriga, oraz jej bliskiego krewnego — otępienia czołowo‑skroniowego (FTD), które atakuje zachowanie i osobowość. W tym badaniu postawiono zaskakująco nadziejne pytanie: czy pojedyncza, umiarkowana dawka promieniowania gamma może subtelnie przekształcić chemię mózgu w sposób, który nie jest wyłącznie destrukcyjny, a być może nawet ochronny wobec molekularnych zmian związanych z ALS i FTD?
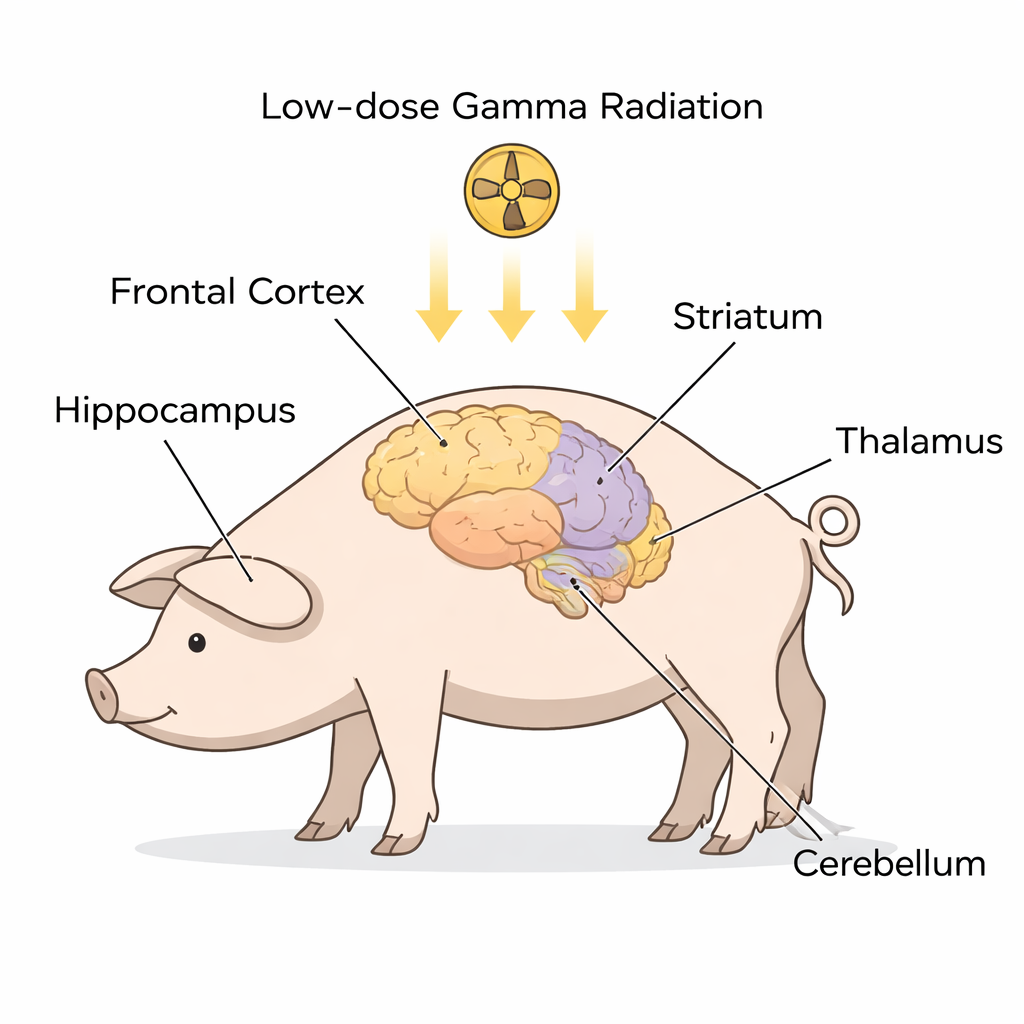
Bliższe spojrzenie na wczesne sygnały ALS w mózgu
Zamiast badać pacjentów już chorych na ALS, badacze pracowali na zdrowych świńcach rasy Göttingen, których mózgi są anatomicznie podobne do ludzkich. Dziewięć zwierząt otrzymało jednorazową, całego ciała ekspozycję na niską dawkę promieniowania gamma, podczas gdy sześć zostało znieczulonych, ale nie napromienionych i służyło jako grupa kontrolna. Około miesiąca później naukowcy rozdzielili pięć kluczowych regionów mózgu często angażowanych w ALS i FTD — korę czołową, hipokamp, prążkowie, wzgórze/podwzgórze oraz móżdżek. W każdym regionie oddzielili zawartość komórek na dwie główne frakcje: cytoplazmę (płynne wnętrze komórki) oraz jądro komórkowe (przestrzeń zawierająca DNA). Przy użyciu techniki Western blot zmierzyli poziomy kilku białek ściśle powiązanych z ALS i ALS‑FTD, w tym SOD1, FUS, C9orf72, STMN2, ubikwityny, TDP‑43 oraz zmodyfikowanej formy — fosforylowanego TDP‑43.
Promieniowanie zostawia niektóre markery bez zmian — inne ulegają przesunięciom
Jednym z uspokajających ustaleń było to, że całkowite poziomy SOD1, białka, którego mutacje powodują pewne dziedziczne postacie ALS, nie zmieniły się w żadnym regionie po napromienieniu. Podobnie główne formy TDP‑43 — białka najczęściej występującego w skupiskach związanych z ALS — pozostały stabilne zarówno w jądrze, jak i w cytoplazmie we wszystkich regionach. Jednak nie wszystko było statyczne. Zespół zaobserwował zmiany zależne od regionu i frakcji komórkowej w kilku innych białkach. Na przykład FUS, białko zwykle lokalizowane w jądrze, które w ALS może źle funkcjonować i tworzyć agregaty, zmniejszyło się w cytoplazmie wzgórza/podwzgórza po napromienieniu, podczas gdy jego poziomy jądrowe wzrosły w korze czołowej, a spadły w hipokampie. Białko związane z ALS, C9orf72, nie zmieniło się w frakcji cytoplazmatycznej, ale wykazało spadek we wnętrzu jąder hipokampa. STMN2, białko ważne dla utrzymania włókien nerwowych, także zmalało w jądrach hipokampa, sugerując skoordynowaną odpowiedź między tymi dwiema cząsteczkami w regionie związanym z pamięcią.
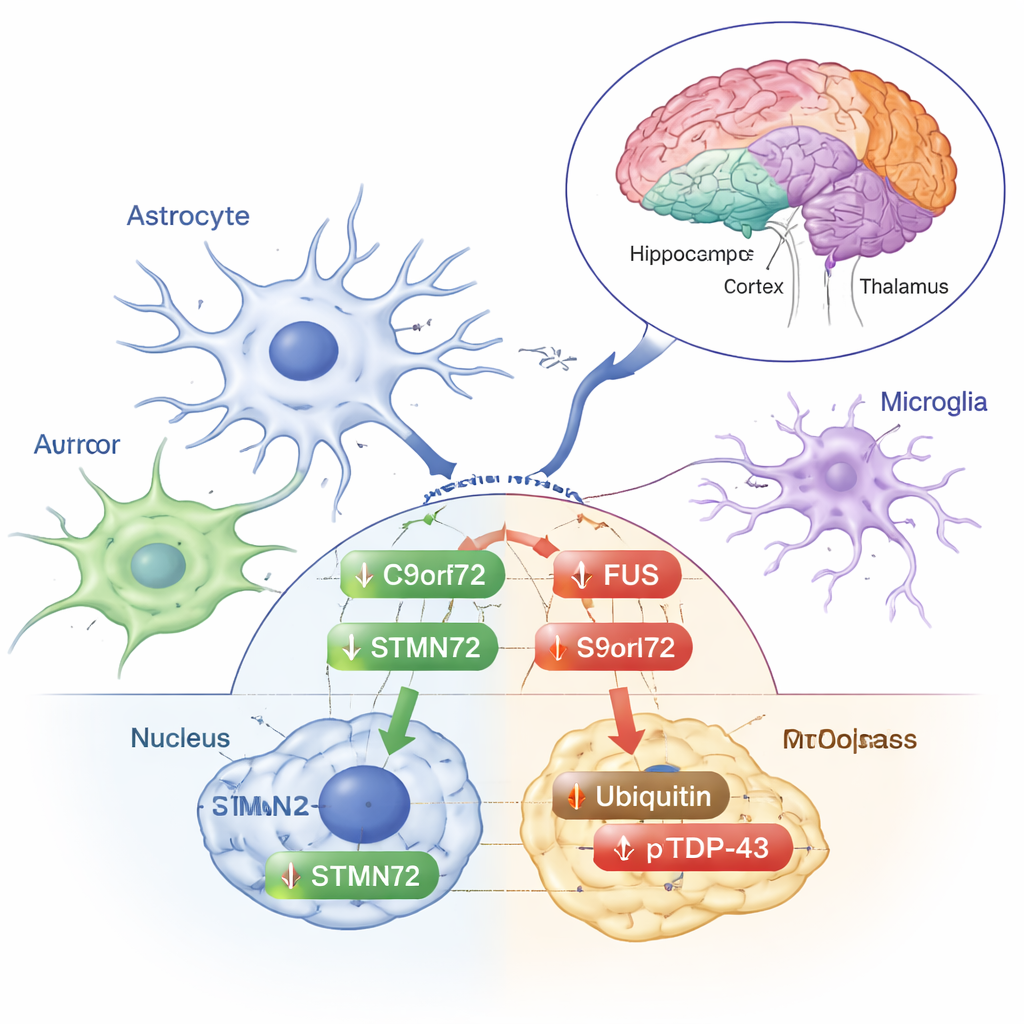
Sygnały stresowe czy wczesna ochrona?
Inne zmiany wyglądały bardziej jak klasyczne odpowiedzi na stres. Ubikwityna — mała etykieta, której komórka używa do oznaczania uszkodzonych białek do usunięcia — zwiększyła się w frakcji cytoplazmatycznej kory czołowej. Fosforylowana forma TDP‑43, która często gromadzi się w nieprawidłowych depozytach występujących w ALS i FTD, wzrosła w cytoplazmie kory czołowej, prążkowia i wzgórza/podwzgórza, mimo że całkowite poziomy TDP‑43 pozostały bez zmian. Te przesunięcia sugerują, że niskodawkowe promieniowanie delikatnie stymuluje mechanizmy zarządzania białkami w mózgu, nie wywołując jednak pełnych wzorców niewłaściwego fałdowania i agregacji charakterystycznych dla choroby. Autorzy podkreślają, że odpowiedzi te różnią się między regionami mózgu i zależą od lokalizacji białka — czy znajduje się w jądrze, czy poza nim — co pokazuje, jak precyzyjnie dostrojona potrafi być reakcja mózgu na stres.
Co to może oznaczać dla ryzyka ALS — i możliwych korzyści
Czy to znaczy, że niskodawkowe promieniowanie powoduje ALS? Dane przemawiają przeciwko tak prostemu wnioskowi. Badacze nie zaobserwowali charakterystycznej utraty prawidłowej lokalizacji ani nagromadzenia głównych białek związanych z ALS, a wiele zmian wskazywało raczej na zmienioną regulację niż na bezpośrednie uszkodzenie. Interesujące jest to, że wyniki te współgrają z wcześniejszymi pracami tej samej grupy i innych zespołów sugerującymi, że niewielkie dawki promieniowania mogą czasem wywołać „hormezę” — zjawisko, w którym łagodny stres aktywuje szlaki naprawcze i redukuje szkodliwe białka, np. związane z chorobą Alzheimera czy Parkinsona w modelach zwierzęcych. Obecne badanie sugeruje, że przynajmniej w krótkim okresie pojedyncza niska dawka promieniowania gamma modyfikuje markery związane z ALS w sposób, który może być adaptacyjny, a nie destrukcyjny.
Wielkie pytania i ostrożna nadzieja
Dla czytelników niebędących specjalistami kluczowy wniosek jest taki, że relacja między promieniowaniem a zdrowiem mózgu jest bardziej zniuansowana niż „wszystkie dawki są złe”. W tym modelu dużego zwierzęcia niskodawkowa ekspozycja na promieniowanie gamma wywołała subtelne, regionowo specyficzne zmiany w białkach związanych z ALS i FTD, nie odtwarzając jednocześnie destrukcyjnych wzorców widocznych w mózgach pacjentów. Zmiany te mogą odzwierciedlać próbę mózgu poradzenia sobie ze stresem i uruchomienia procesów naprawczych, a w niektórych przypadkach mogą okazać się wręcz korzystne. Należy jednak pamiętać, że badanie obejmowało jedynie obserwację miesiąc po pojedynczym napromienieniu i dotyczyło tylko mózgu (nie rdzenia kręgowego, który jest głównym miejscem działania ALS). Potrzebne są badania długoterminowe oraz z powtarzanymi dawkami, zanim będzie można rozważać translację tych wyników na ludzi. Mimo to praca ta otwiera nowe okno na to, jak promieniowanie na poziomie codziennym oddziałuje z molekułami leżącymi u podstaw wyniszczających chorób neurodegeneracyjnych — i sugeruje możliwość, że w ściśle kontrolowanych warunkach niewielkie dawki mogłyby w przyszłości być wykorzystane do stymulowania własnych mechanizmów obronnych mózgu.
Cytowanie: Iacono, D., Murphy, E.K., Perl, D.P. et al. γ-Radiation induces region-specific subcellular alterations of amyotrophic lateral sclerosis and frontotemporal dementia markers in swine brain. Sci Rep 16, 5627 (2026). https://doi.org/10.1038/s41598-026-36208-8
Słowa kluczowe: stwardnienie zanikowe boczne, otępienie czołowo‑skroniowe, niskodawkowe promieniowanie, białka mózgu, model świni miniaturowej