Clear Sky Science · pl
Kasetyl lizy dżumbofaga PhiKZ
Jak olbrzymie wirusy rozrywają bakterie
Wirusy atakujące bakterie — nazywane bakteriofagami lub po prostu fagami — są badane jako precyzyjna broń przeciw niebezpiecznym zakażeniom, takim jak te wywoływane przez Pseudomonas aeruginosa, szpitalnego superbakterium. Jeden szczególnie duży fag, phiKZ, zafascynował naukowców, ponieważ buduje wewnątrz gospodarza ochronne „jądrowe” przegrody białkowe. Do tej pory nie wiadomo było jednak, w jaki sposób ten olbrzymi fag faktycznie rozrywa komórkę gospodarza, by się z niej uwolnić. Badanie to ujawnia zestaw genów i narzędzi molekularnych, których phiKZ używa, aby wyznaczyć czas i przeprowadzić końcowy, gwałtowny etap infekcji.
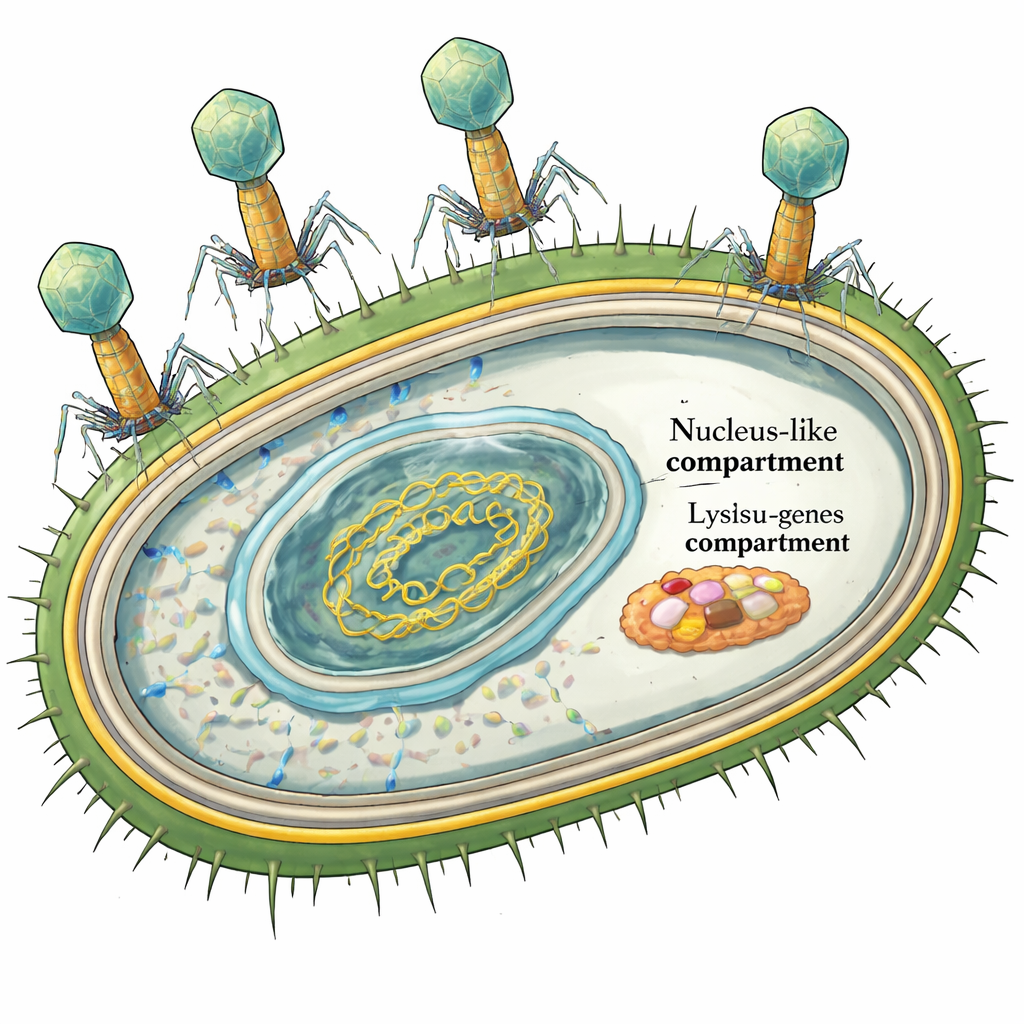
Gigantyczny fag i jego plan ucieczki
PhiKZ to dżumbofag, o genomie dłuższym niż 200 000 par zasad DNA. Wcześniejsze badania szczegółowo wykazały, jak ukrywa on swój materiał genetyczny w białkowej osłonie, by unikać bakterijnych mechanizmów obronnych. Ostatni akt infekcji — kontrolowane zniszczenie komórki bakteryjnej — pozostawał jednak zagadką. Większość fagów atakujących bakterie o dwóch błonach, takich jak Pseudomonas, korzysta z czteroczęściowego systemu lizy: jeden białkowy element tworzy otwory w błonie wewnętrznej, inny tnie ścianę komórkową, a kompleks dwu-składnikowy powoduje zapadnięcie się błony zewnętrznej. Ponieważ w genomie phiKZ wydawało się brakować rozpoznawalnego genu tworzącego otwory, niektórzy badacze sugerowali, że może on używać zupełnie innej strategii, aby umieścić enzym rozcinający ścianę na właściwym miejscu.
Odnalezienie ukrytego zestawu lizy
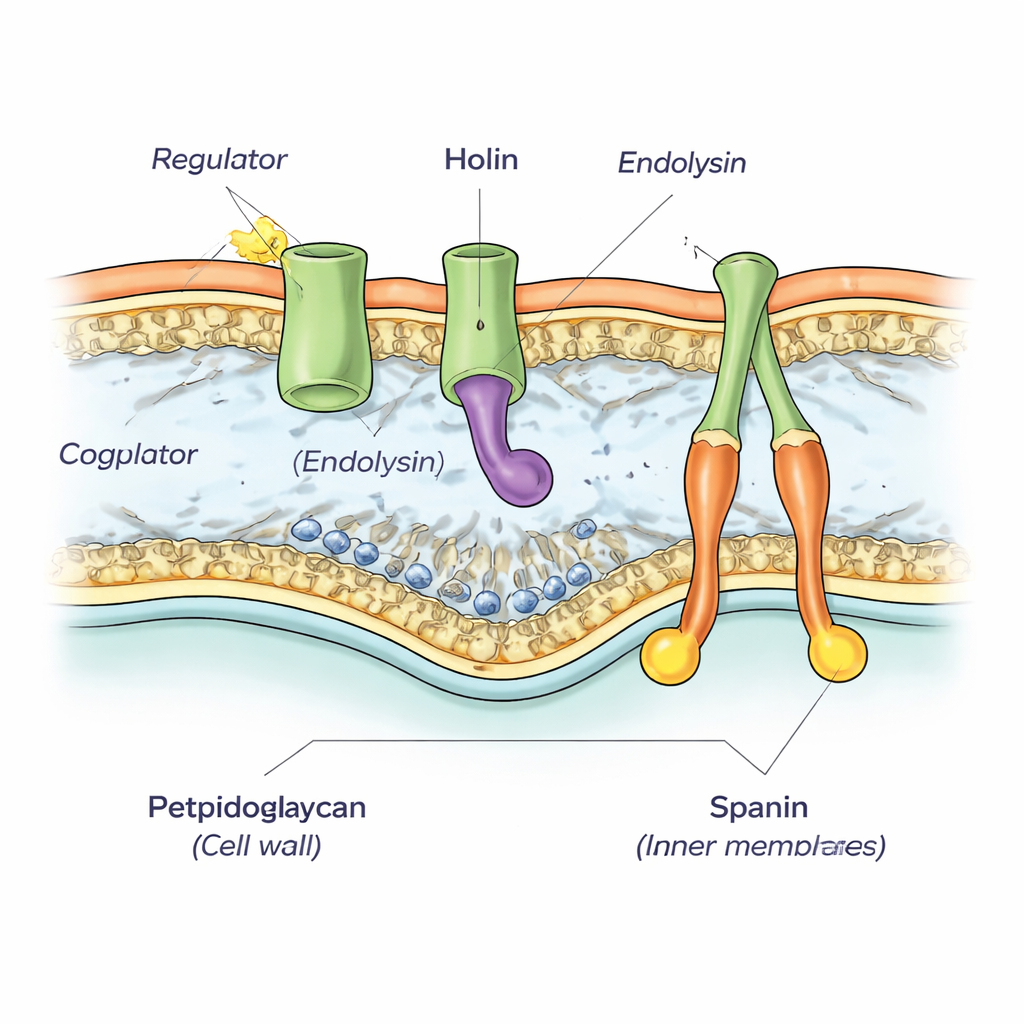
Reanalizując rejon genomu phiKZ otaczający znaną endolizynę (enzym rozkładający ścianę komórkową), autorzy odkryli ciasno upakowany klaster pięciu genów. Analizy sekwencji i przewidywania komputerowe wykazały, że dwa z tych genów kodują spaniny — parę białek łączących błonę wewnętrzną i zewnętrzną, które później pomagają im się zlać. Kolejny gen koduje samą endolizynę. Czwarty gen okazał się brakującym holinem — białkiem, które stopniowo odkłada się w błonie wewnętrznej, zanim nagle utworzy duże otwory. Badacze potwierdzili te funkcje eksperymentalnie, przenosząc geny phiKZ do dobrze poznanych systemów fagów lambda i Escherichia coli i pokazując, że wersje phiKZ mogą zastąpić brakujące elementy.
Przełącznik czasowy dla destrukcji komórki
Piąty gen w klastrze koduje małe białko, które pozostaje w cytoplazmie bakteryjnej, zamiast osadzać się w błonie. Gdy autorzy ekspresowali to białko razem z holinem w E. coli, komórki umierały wyraźnie wcześniej niż przy działaniu samego holinu, mimo że reszta aparatu lizy była nieobecna. Sugeruje to, że dodatkowe białko działa jako regulator, przesuwając holin ku wcześniejszemu lub silniejszemu formowaniu porów. Kiedy zespół skracał fragmenty długiego, skierowanego do wnętrza ogona holinu, regulator nie mógł już przyspieszać procesu, a w niektórych przypadkach nawet blokował lizę. Modele strukturalne wygenerowane programem AlphaFold wspierały obraz fizycznego partnerstwa między wewnętrznym ogonem holinu a regulatorem, tworzącego stabilny kompleks dwu-białkowy.
Sugestie mechanizmu opóźniającego przy dużych dawkach wirusa
Gdy badacze infekowali kultury bakteryjne różnymi liczbami cząstek phiKZ, zauważyli intrygujący wzorzec. Przy niskich dawkach wirusa kultura lizała się stosunkowo szybko i gwałtownie. Przy wysokich dawkach liza była jednak opóźniona i rozciągnięta na ponad dwie godziny. To pozornie sprzeczne spowolnienie przypomina klasyczne zjawisko zwane inhibicją lizy, znane z innego faga, T4, w którym dodatkowe infekcje sygnalizują wirusowi odłożenie pęknięcia komórki, by powstało więcej cząstek wirusa. Ponieważ phiKZ posiada parę holin–regulator zdolną zarówno do przyspieszania, jak i, w pewnych warunkach, blokowania lizy, autorzy sugerują, że podobny system opóźniający może istnieć także u tego dżumbofaga.
Znaczenie dla terapii fagowej
Pokazując, że phiKZ niesie konwencjonalny, ale wysublimowany kaset lizy — z holinem, endolizyną, spaninami i regulatorem czasu — praca ta dowodzi, że nawet egzotyczne dżumbofagi opierają się na znanych narzędziach, aby wydostać się ze swoich gospodarzy. Dla osób niebędących specjalistami kluczowy wniosek jest taki, że „czas wybuchu” leczniczych fagów można modulować małymi białkami regulatorowymi, które komunikują się z poretworzącymi holinami. Zrozumienie i ostatecznie zaprojektowanie tych przełączników czasowych może pomóc w tworzeniu terapii fagowych, które albo zabijają bakterie jak najszybciej, albo — gdy to korzystne — odwlekają lizę, aby zmaksymalizować amplifikację wirusa przed końcowym ciosem.
Cytowanie: Manohar, P., Wan, J., Ganser, G. et al. The Lysis cassette of jumbophage PhiKZ. Sci Rep 16, 5840 (2026). https://doi.org/10.1038/s41598-026-36188-9
Słowa kluczowe: lizowanie bakteriofagów, phiKZ dżumfag, system holin-endolizyna, fag Pseudomonas aeruginosa, hamowanie lizy