Clear Sky Science · pl
FcIgG-GE11-Melittin jako nowy peptibody ukierunkowany na EGFR o silnym działaniu cytotoksycznym wobec komórek nowotworowych
Gdy jad pszczeli spotyka precyzyjną terapię przeciwnowotworową
Wiele obiecujących leków przeciwnowotworowych jest po prostu zbyt szkodliwych dla reszty organizmu, by można je było bezpiecznie stosować. Jednym z uderzających przykładów jest melityna, główny toksyn w jadu pszczelego: potrafi rozrywać komórki nowotworowe, lecz jednocześnie może uszkadzać czerwone krwinki i zdrowe tkanki. Niniejsze badanie opisuje sprytne obejście tego problemu — zbudowanie „sterowanego pocisku”, który przenosi melitynę bezpośrednio do komórek guza prezentujących konkretny marker powierzchniowy, jednocześnie w dużej mierze oszczędzając komórki prawidłowe.
Dlaczego warto celować w powszechny przełącznik nowotworowy
Kluczowym graczem w wielu nowotworach jest receptor naskórkowego czynnika wzrostu, znany jako EGFR. Receptor ten znajduje się na powierzchni komórek i pomaga kontrolować wzrost oraz przeżycie. W kilku rodzajach raka — w tym płuca, jelita grubego, prostaty oraz niektórych nowotworach głowy, szyi i nerki — EGFR bywa nadmiernie produkowany, napędzając niekontrolowane dzielenie się komórek. Z tego powodu leki wiążące EGFR stały się ważną klasą terapii celowanych. Jednak istniejące leki przeciw EGFR głównie blokują sygnały; nie niszczą aktywnie komórek. Badacze zastanawiali się, czy można wykorzystać silne właściwości lityczne melityny i dostarczyć ją selektywnie do komórek guza bogatych w EGFR.
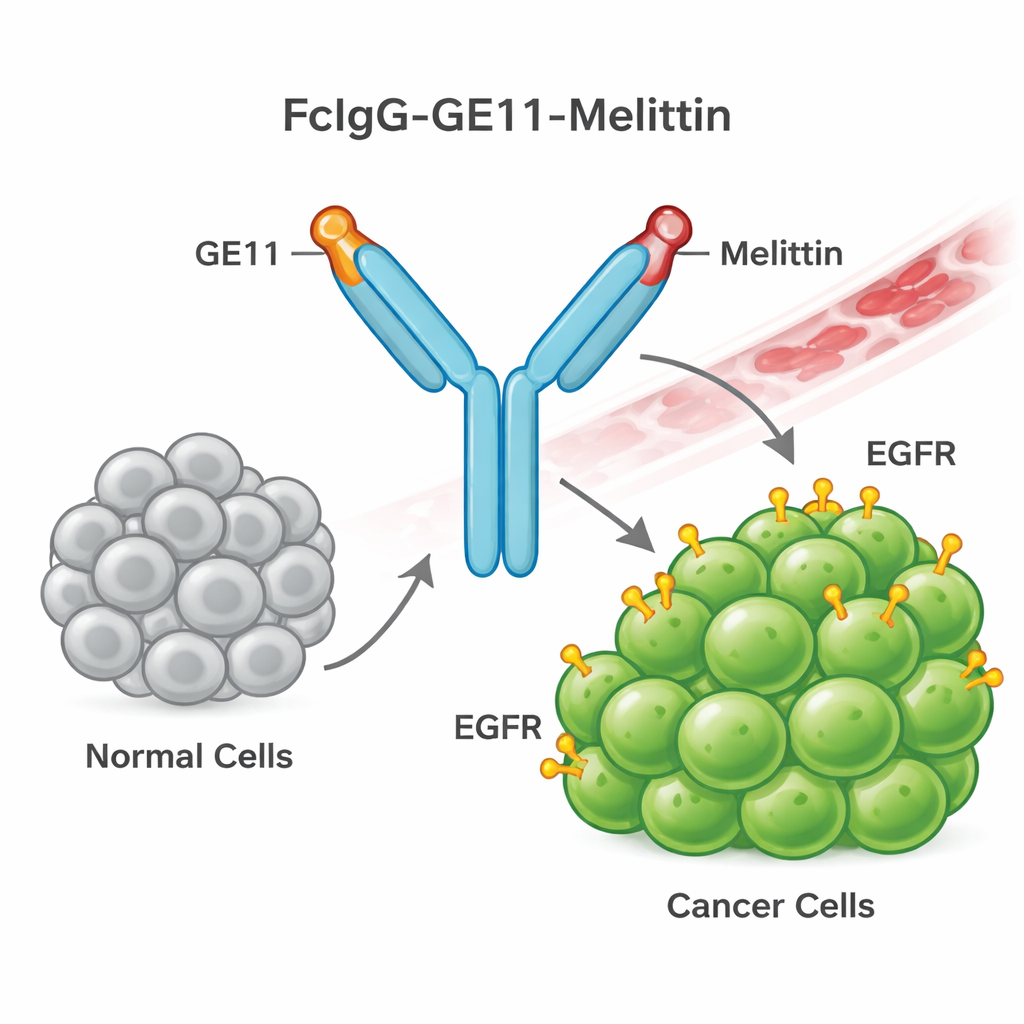
Budowa sterowanej broni z jadu pszczelego
Aby to osiągnąć, zespół zaprojektował nowy białkowy fuzjat, który nazwali FcIgG-GE11-Melittin. Łączy on trzy elementy: „ogon” przeciwciała (region Fc ludzkiego IgG), który poprawia stabilność we krwi i ułatwia oczyszczanie; krótki peptyd przewodnikowy GE11 rozpoznający i wiążący EGFR na komórkach nowotworowych; oraz melitynę, peptyd z jadu pszczelego zdolny do rozrywania błon komórkowych. Bakterie zostały zaprogramowane do produkcji tego białka fuzjowanego w dużych ilościach. Białko następnie poddano ponownemu fałdowaniu i oczyszczaniu, a testy laboratoryjne potwierdziły, że przyjęło oczekiwaną dimerową strukturę i zawiera tag przeciwciała ludzkiego, co wskazuje, że konstrukcja została zbudowana poprawnie.
Przyczepianie się do komórek guza, nie do każdej komórki
Następne pytanie brzmiało, czy zaprojektowana cząsteczka rzeczywiście odnajduje i przyczepia się do komórek bogatych w EGFR. Używając cytometrii przepływowej, autorzy testowali wiązanie na komórkach raka płuca A549, znanych z nadekspresji EGFR. Komórki potraktowane FcIgG-GE11-Melittin wykazały silny wzrost fluorescencji, co wskazuje, że wiele cząsteczek fuzjatu przyłączyło się do ich powierzchni. Niespowinowacony peptibody, Romiplostim, wykazał niemal brak wiązania i służył jako kontrola negatywna. Profil wiązania nowej konstrukcji ściśle odpowiadał profilowi Cetuksymabu, dobrze znanego przeciwciała przeciw EGFR, co wspiera tezę, że składnik GE11 prawidłowo kieruje białko fuzjowane do celu.
Zabijanie komórek nowotworowych przy jednoczesnym oszczędzaniu komórek krwi
Zespół następnie sprawdził, jak dobrze białko fuzjowane zabija różne linie komórek nowotworowych w hodowli. Wolna melityna była niezwykle silna, ale nieselektywna — obniżała przeżywalność komórek ostro nawet przy niskich dawkach w liniach raka płuca (A549), prostaty (DU145) i jelita grubego (SW480). Dla kontrastu, FcIgG-GE11-Melittin wykazywał zabijanie zależne od dawki, najsilniejsze w komórkach pozytywnych pod względem EGFR, podczas gdy linia raka piersi o niskim poziomie EGFR (MDA-MB-453) była stosunkowo oporna. Ten wzorzec sugeruje, że atak konstruktu zależy od ukierunkowania na EGFR, a nie od przypadkowego uszkodzenia błon. Co najważniejsze, w eksperymentach z ludzkimi erytrocytami wolna melityna powodowała niemal całkowitą hemolizę przy umiarkowanych dawkach, podczas gdy białko fuzjowane wywoływało mniej niż 5% hemolizy nawet przy bardzo wysokich stężeniach. Innymi słowy, przyłączenie melityny do nośnika szukającego EGFR dramatycznie zmniejszyło jej tendencję do pękania czerwonych krwinek.
Co to może znaczyć dla przyszłej opieki onkologicznej
Podsumowując, praca pokazuje, że sprzężenie silnego toksyny niszczącej błony, jak melityna, z precyzyjnym systemem celowania może przemienić ją z ogólnie toksycznej substancji w bardziej wybiórczą broń przeciw guzowi. FcIgG-GE11-Melittin silnie wiąże się z komórkami nowotworowymi nadekspresjonującymi EGFR, zabija je w kontrolowany, zależny od dawki sposób i wykazuje minimalne uszkodzenia czerwonych krwinek in vitro. Choć potrzebne są dalsze badania na zwierzętach i testy bezpieczeństwa przed ewentualnym zastosowaniem u pacjentów, podejście to ilustruje, jak przeprojektowanie naturalnych toksyn w ukierunkowane terapie może otworzyć nowe drogi leczenia nowotworów EGFR-dodatnich skuteczniej i z mniejszą liczbą skutków ubocznych.
Cytowanie: Hallaji, M., Fayaz, S., Allahyari, M. et al. FcIgG-GE11-Melittin as a novel EGFR targeted peptibody with potent cytotoxic activity against cancer cells. Sci Rep 16, 7047 (2026). https://doi.org/10.1038/s41598-026-36167-0
Słowa kluczowe: ukierunkowana terapia przeciwnowotworowa, EGFR, melityna z jadu pszczelego, peptibody, toksyczny wybór guza