Clear Sky Science · pl
Cytoplazmatyczny TDP-43 prowadzi do wczesnych zaburzeń behawioralnych bez neurodegeneracji w modelu C. elegans specyficznym dla neuronów serotoninergicznych
Dlaczego drobne robaki mają znaczenie dla dużych chorób mózgu
Choroby takie jak stwardnienie zanikowe boczne (ALS) i otępieńczość czołowo-skroniowa (FTD) stopniowo odbierają ludziom zdolność poruszania się, mówienia i cechy osobowości. Głównym podejrzanym w tych schorzeniach jest białko zwane TDP-43, które zagęszcza się w niewłaściwym miejscu wewnątrz komórek nerwowych. W tym badaniu użyto maleńkiego robaka, Caenorhabditis elegans, aby obserwować, co dzieje się u żywych zwierząt, gdy TDP-43 przemieszcza się ze swojego normalnego miejsca do cytoplazmy. Skupiając się na niewielkim, dobrze poznanym zestawie neuronów produkujących serotoninę, badacze pokazują, jak zachowanie może ulec zaburzeniu na długo zanim neurony widocznie obumrą — co daje wgląd w najwcześniejsze, najbardziej podatne na interwencję etapy choroby. 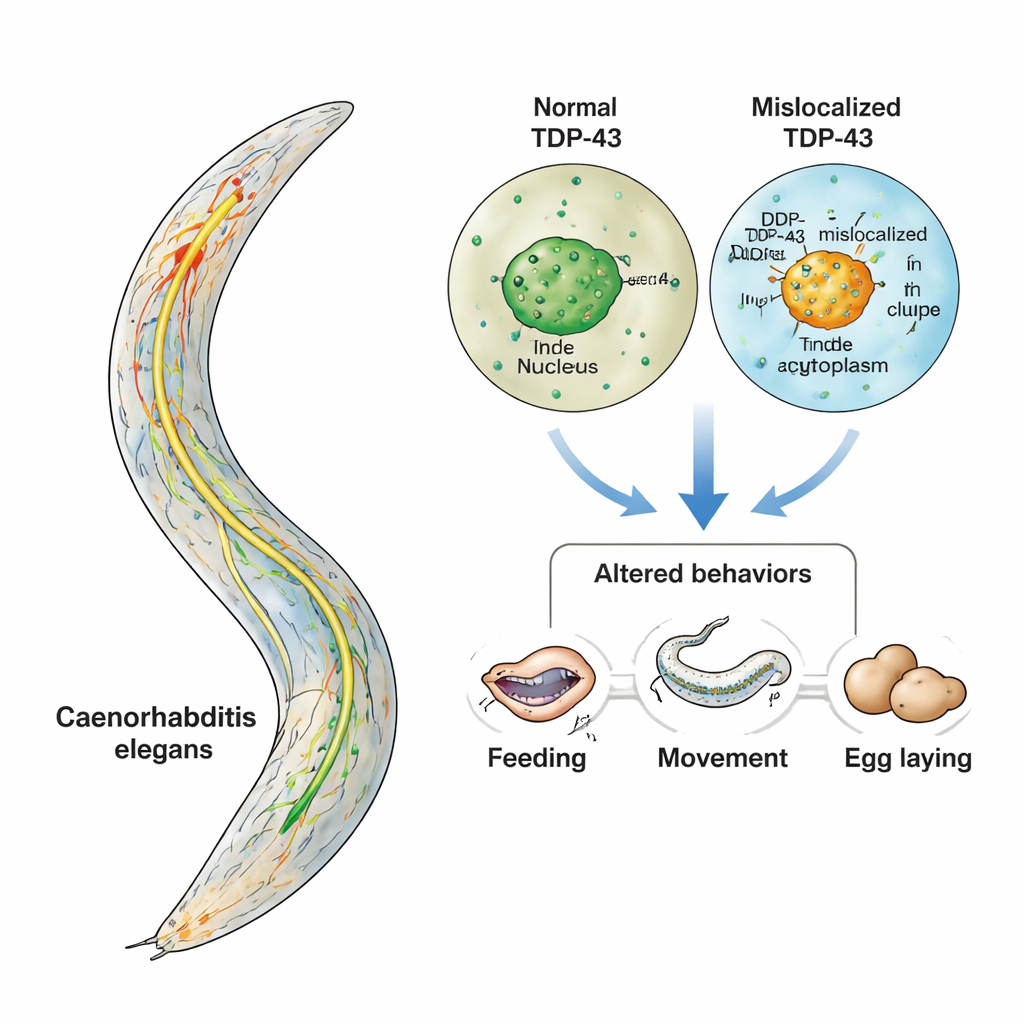
Białko tworzące grudki i przekaźnik chemiczny
TDP-43 zwykle znajduje się w jądrze komórkowym, gdzie pomaga zarządzać RNA, pracującymi kopiami instrukcji genetycznych. W ALS i FTD jednak TDP-43 często opuszcza jądro, gromadzi się w cytoplazmie i tworzy lepiące agregaty. Równocześnie dane z badań pacjentów i modeli mysich sugerują, że serotonina — przekaźnik chemiczny kojarzony głównie z nastrojem — także bywa zaburzona w tych chorobach. Ponieważ serotonina wpływa na wiele zachowań — od pobierania pokarmu po kontrolę ruchu — autorzy postawili konkretne pytanie: jeśli TDP-43 jest nieprawidłowo zlokalizowany specyficznie w neuronach produkujących serotoninę, czy te neurony funkcjonują wadliwie w sposób, który zmienia zachowanie, nawet zanim ulegną degeneracji?
Przeprogramowanie prostego układu nerwowego
Zespół sięgnął po C. elegans, mikroskopijnego robaka, którego cały układ nerwowy liczący 302 neurony został starannie zmapowany. Tylko trzy pary tych neuronów wytwarzają serotoninę, a każda para kontroluje dobrze określone zachowanie: pobieranie pokarmu (pompy gardzieli), spowalnianie przy znalezieniu pożywienia oraz składanie jaj. Przy użyciu narzędzi genetycznych badacze zmodyfikowali robaki tak, by tylko te serotonergiczne neurony produkowały ludzkie TDP-43. Jeden szczep wytwarzał normalną, zlokalizowaną w jądrze formę; inny szczep wytwarzał wariant mutantowy pozbawiony „adresu” jądrowego, co zmuszało TDP-43 do akumulacji w cytoplazmie. Ponieważ wszystkie inne neurony pozostały nietknięte, wszelkie zmiany w zachowaniu można było bezpośrednio przypisać problemom w tym jednym, niewielkim obwodzie.
Zachowanie zawodzi zanim neurony umrą
W szeregu testów zmodyfikowane robaki zachowywały się nieprawidłowo w sposób, który ściśle odzwierciedlał częściową lub silną utratę funkcji serotoniny. Robaki z cytoplazmatyczną wersją TDP-43 wykazywały wolniejsze rytmiczne pompowanie narządu pokarmowego, słabszą tendencję do spowalniania po napotkaniu jedzenia po głodówce oraz zmniejszone składanie jaj. Robaki wyrażające normalne, jądrowe TDP-43 również radziły sobie gorzej niż nienaruszone zwierzęta, ale nie tak źle jak te z cytoplazmatycznym TDP-43, co ujawniło wyraźny gradient upośledzenia. Co istotne, gdy te same zwierzęta testowano w kontekście, w którym serotonina nie jest potrzebna — pływanie w cieczy — ich ruch był normalny. Wskazuje to, że podstawowy mechanizm lokomocyjny był nienaruszony, a deficyty dotyczyły specyficznych zachowań zależnych od serotoniny, a nie ogólnego pogorszenia stanu zdrowia. 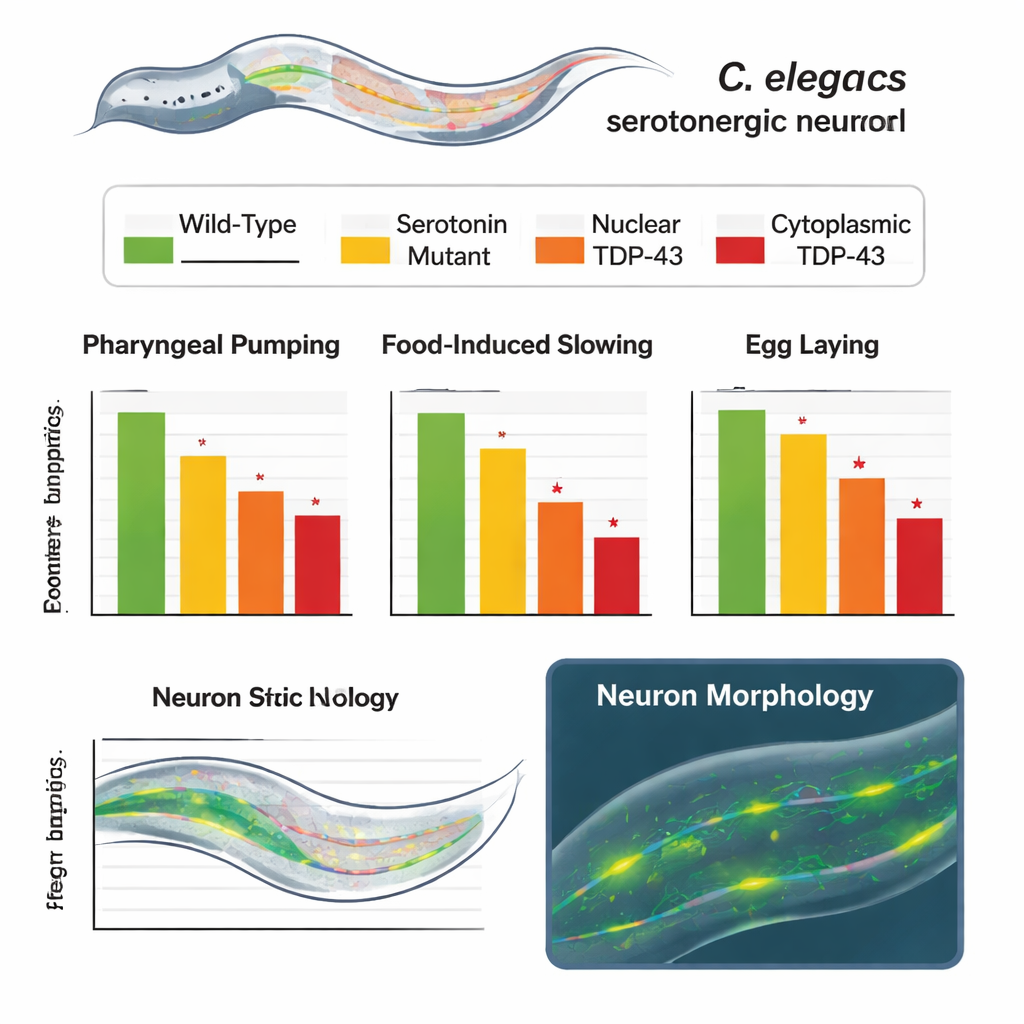
Ukryte uszkodzenia ujawnione testem farmakologicznym
Aby sprawdzić, czy dotknięte neurony nadal żyją i są funkcjonalne, badacze użyli fluoksetyny, znanej szerzej jako Prozac, leku wzmacniającego sygnalizację serotoninergiczną. U normalnych robaków fluoksetyna zdecydowanie zwiększa składanie jaj. U zmodyfikowanych robaków lek nadal podnosił liczbę złożonych jaj, ale odpowiedź była stłumiona — szczególnie u tych z cytoplazmatycznym TDP-43. Ten wzorzec sugeruje, że neurony serotoninergiczne nadal potrafiły uwalniać sygnały, ale robiły to mniej efektywnie. Mikroskopowe obrazowanie dostarczyło podobnego obrazu: neurony produkujące serotoninę wyglądały strukturalnie normalnie, bez utraty ciał komórkowych czy poważnych deformacji ich rozgałęzień, a ich ogólna fluorescencja — będąca wskaźnikiem stanu komórek — odpowiadała temu obserwowanemu u robaków kontrolnych.
Wczesne sygnały ostrzegawcze i nowe możliwości
Razem te wyniki kreślą obraz, w którym nieprawidłowo zlokalizowany TDP-43 może poważnie zaburzać funkcjonowanie neuronów serotoninergicznych, pozostawiając je na pozór nienaruszonego wzorku. U robaków zachowanie ulega zaburzeniu — pobieranie pokarmu, modulacja ruchu i reprodukcja — zanim pojawi się widoczna śmierć neuronów. To odzwierciedla obserwacje kliniczne, że subtelne zmiany w zachowaniu i nastroju często poprzedzają oczywiste kurczenie się mózgu w ludzkich chorobach neurodegeneracyjnych. Dzięki prostemu, genetycznie podatnemu systemowi, w którym wczesne, specyficzne dla obwodu defekty można precyzyjnie mierzyć, ten model robaka może pomóc naukowcom badać, jak TDP-43 zaburza funkcję neuronów i testować terapie mające na celu uratowanie neuronów w tym wrażliwym, przeddegeneracyjnym oknie.
Cytowanie: Lacour, A., Vassallu, F., Romussi, S. et al. Cytoplasmic TDP-43 leads to early behavioral impairments without neurodegeneration in a serotonergic neuron-specific C. elegans model. Sci Rep 16, 6068 (2026). https://doi.org/10.1038/s41598-026-36138-5
Słowa kluczowe: TDP-43, neurony serotoninergiczne, C. elegans, ALS i FTD, neurodegeneracja