Clear Sky Science · pl
Transkrypcyjny pejzaż pojedynczych komórek w płucach pediatrycznych chorych na mukowiscydozę uzyskany z minimalnie inwazyjnych próbek oddechowych
Dlaczego to ma znaczenie dla dzieci z mukowiscydozą
Mukowiscydoza jest najbardziej znana z gęstego śluzu i infekcji płuc, ale pod tymi objawami toczy się złożona walka między komórkami odpornościowymi a delikatną wyściółką dróg oddechowych. Badanie to przygląda się tej walce u dzieci, komórka po komórce, wykorzystując niewielkie próbki pobrane podczas rutynowych kontroli płuc. Mapując, jakie komórki występują i jak są aktywne, badacze pokazują, że szkodliwe wzorce zapalenia zaczynają się wcześnie i mogą być trudne do odwrócenia, nawet przy nowoczesnych lekach naprawiających defekt genetyczny u źródła choroby.
Zerknięcie do młodych płuc — po jednej komórce
Aby zbadać, co dzieje się w płucach dzieci, zespół użył minimalnie inwazyjnych narzędzi podczas giętkiej bronchoskopii — procedur, które pacjenci i tak przechodzili z powodów medycznych. Delikatnie szczotkowali wewnętrzną powierzchnię tchawicy i oskrzeli oraz pobierali płukanie z głębszych partii płuc. Próbki pochodziły od dwojga dzieci z mukowiscydozą (niemowlęcia i nastolatka) oraz trojga dzieci w tym samym wieku bez choroby. Wykorzystując sekwencjonowanie RNA pojedynczych komórek — technikę odczytującą, które geny są włączone w tysiącach pojedynczych komórek — zbudowali mapę o wysokiej rozdzielczości komórek odpornościowych i komórek wyściełających drogi oddechowe w płucach każdego dziecka. 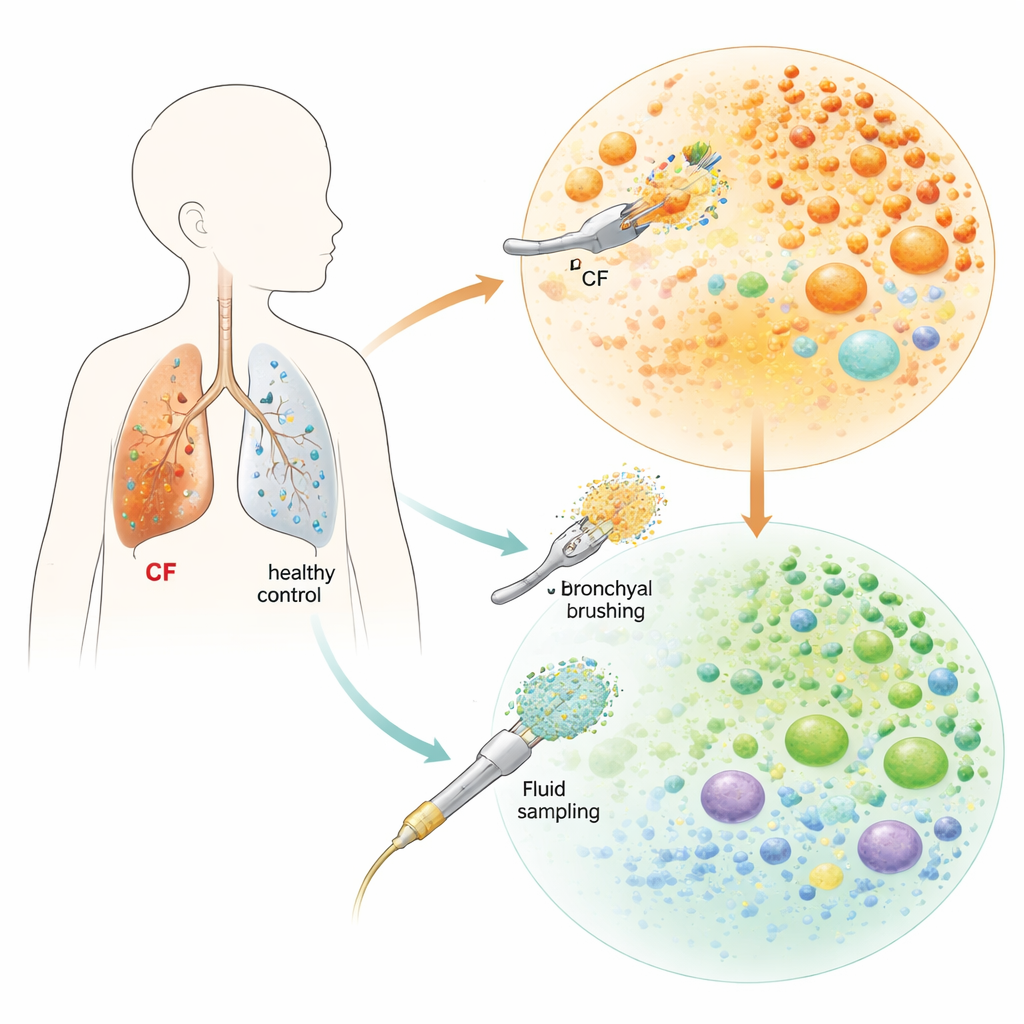
Zagęszczone szeregi komórek pierwszej reakcji
W próbkach płukania z płuc dzieci bez mukowiscydozy dominowały makrofagi — komórki sprzątające, które patrolują przestrzenie oddechowe i pomagają utrzymać równowagę. W przeciwieństwie do tego, u dzieci z mukowiscydozą zaobserwowano dramatyczne przesunięcie w stronę neutrofili, szybko działających „pierwszorazowych” krwinek białych, które mogą uszkadzać tkankę, gdy utrzymują się zbyt długo. Neutrofile nie tylko występowały w większej liczbie, ale pojawiały się w kilku odmiennych odmianach. Były to formy niedojrzałe, silnie aktywowane komórki zapalne oraz uderzający podzbiór oznaczony białkami odpowiedzi na stres znanymi jako białka szoku cieplnego. Choć takie reakcje stresowe mogą początkowo chronić, mogą też zahamować neutrofile w długotrwałym, agresywnym stanie, który podtrzymuje zapalenie i może napędzać uszkodzenia dróg oddechowych obserwowane w mukowiscydozie.
Zapaleni obrońcy i brak wzmocnień
Makrofagi, które pozostały w płucach chorych na mukowiscydozę, również wyglądały inaczej. Zamiast mieszanki typów „porządkowych” widocznej w grupie kontrolnej, próbki od pacjentów z mukowiscydozą były wzbogacone w makrofagi produkujące silne sygnały immunologiczne, co sugeruje przejście w bardziej zapalną rolę. Jednocześnie w płynie dróg oddechowych dzieci z mukowiscydozą było stosunkowo niewiele komórek T — innego kluczowego ramienia układu odpornościowego. Poprzednie badania wykazały, że neutrofile mogą pozbawiać komórki T składników odżywczych niezbędnych do ich funkcjonowania, skutecznie wypychając je z dróg oddechowych. To połączenie agresywnych neutrofili, aktywowanych makrofagów i rzadkich komórek T może pomóc wyjaśnić, dlaczego płuca chorych na mukowiscydozę pozostają zapalne i podatne na infekcje przez wiele lat.
Wyściółka dróg oddechowych włącza się do walki
Próbki ze szczotkowania pozwoliły badaczom przyjrzeć się komórkom wyściełającym drogi oddechowe: komórkom podstawowym (zdolnym do odnawiania wyściółki), komórkom rzęsatym (z włosopodobnymi wypustkami, które zamiatają śluz) oraz komórkom wydzielniczym (produkującym śluz i cząsteczki ochronne). Ogólny udział tych typów komórek był podobny między dziećmi z mukowiscydozą a grupą porównawczą, ale ich zachowanie nie. W mukowiscydozie komórki wydzielnicze włączyły geny związane z obroną immunologiczną i aktywnością antymikrobiologiczną, co sugeruje, że pracują ponadnormatywnie jako część odpowiedzi zapalnej. Komórki rzęsate również włączyły geny powiązane z zapaleniem i odpornością na formę śmierci komórkowej związaną z żelazem i uszkodzeniem oksydacyjnym. Razem te wzorce wskazują, że powierzchnia dróg oddechowych nie jest tylko biernym obserwatorem, lecz aktywnym, zapalnym uczestnikiem procesu chorobowego. 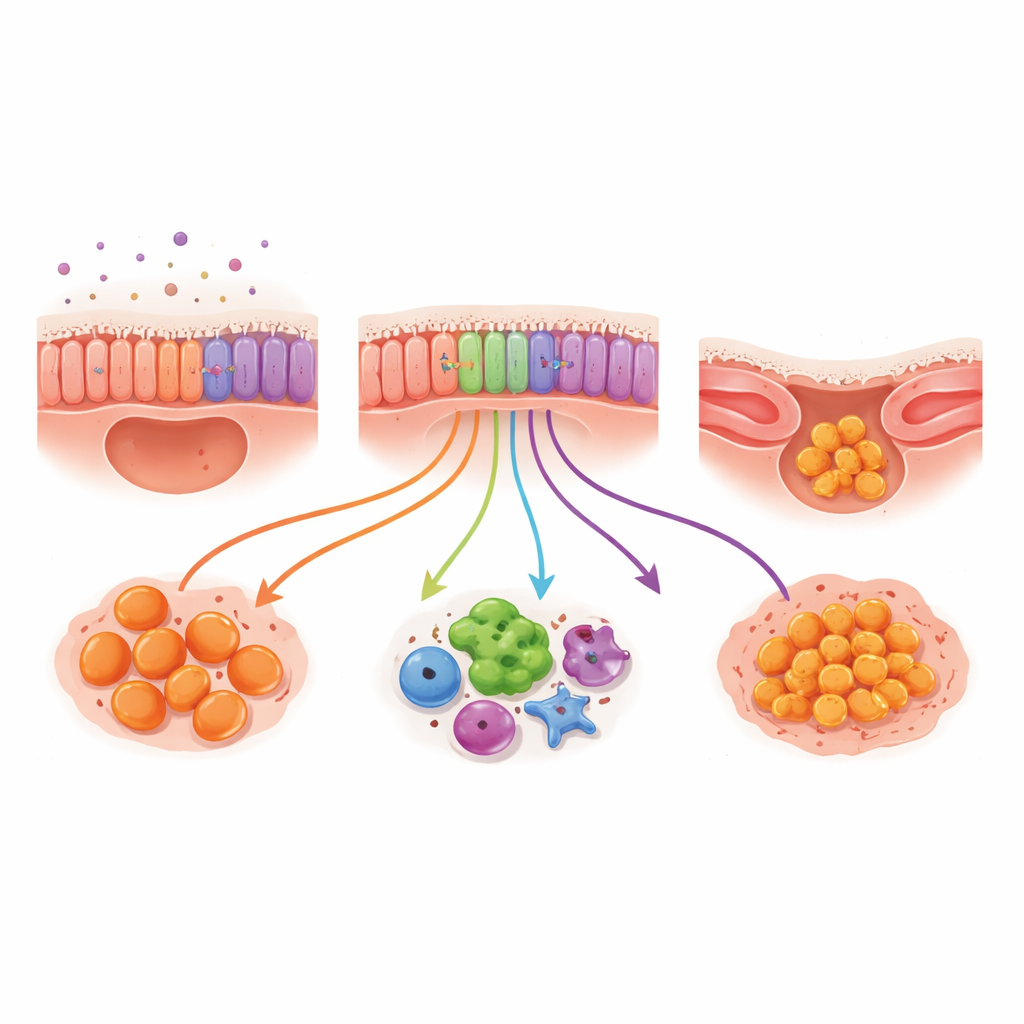
Rozmowy komórka do komórki, które podsycają uszkodzenia płuc
Aby zrozumieć, jak komórki wyściełające drogi oddechowe i neutrofile wpływają na siebie nawzajem, zespół przeanalizował „rozmowy” między nimi — sygnały wysyłane przez jeden typ komórek i odbierane przez inny. Stwierdzili, że komórki nabłonkowe często działają jako nadawcy, używając kilku systemów molekularnych do komunikacji z neutrofilami. Niektóre z tych sygnałów prawdopodobnie pomagają uciszyć zapalenie, podczas gdy inne zachęcają neutrofile do napływu, aktywacji i fagocytozy materiału. To popychanie i przyciąganie sugeruje, że nabłonek próbuje równoważyć kontrolę uszkodzeń i obronę, ale w mukowiscydozie wydaje się, że sygnały prozapalne przeważają, utrzymując płuca w chronicznym stanie tlącego się urazu.
Dlaczego wczesne zmiany trudno odwrócić
Kluczowe odkrycie jest takie, że te wzorce zapalne występowały zarówno u niemowlęcia, jak i u nastolatka, który przyjmował zaawansowany lek na mukowiscydozę poprawiający funkcję wadliwego białka. Pomimo tej ukierunkowanej terapii, komórki płuc nastolatka wciąż przypominały bardziej komórki nieleczonego niemowlęcia niż komórki dzieci z grupy porównawczej. Sugeruje to, że gdy rozwija się strukturalne uszkodzenie i utrwalone zapalenie, samo przywrócenie funkcji białka może nie wystarczyć, by zresetować krajobraz immunologiczny i nabłonkowy. Badanie pokazuje także, że delikatne pobieranie próbek dróg oddechowych w połączeniu z analizą genów na poziomie pojedynczych komórek i analizą przestrzenną może śledzić te zmiany w czasie. Podejście to może pomóc w projektowaniu i testowaniu nowych terapii przeciwzapalnych i przeciwmikrobiotycznych mających na celu ochronę struktury płuc od najwcześniejszych etapów życia.
Cytowanie: Sun, Y., Vicencio, A.G., Beasley, M.B. et al. The single-cell transcriptional landscape of the pediatric cystic fibrosis lung from minimally invasive respiratory specimens. Sci Rep 16, 8113 (2026). https://doi.org/10.1038/s41598-026-36125-w
Słowa kluczowe: płuca w mukowiscydozie, neutrofilowe zapalenie, sekwencjonowanie RNA pojedynczych komórek, nabłonek dróg oddechowych, bronchoskopia pediatryczna