Clear Sky Science · pl
Kompleksowa ocena genotoksyczności wywołanej przez złote nanorodziny z użyciem wielomodelowych systemów biologicznych
Dlaczego maleńkie złote pręciki mają znaczenie dla naszego DNA
Złoto może przywodzić na myśl biżuterię czy finanse, ale we współczesnej medycynie jest też formowane w maleńkie pręciki tysiące razy cieńsze od włosa. Te „złote nanorodziny” pomagają lekarzom lepiej zobaczyć guzy, ogrzewać i niszczyć komórki nowotworowe oraz precyzyjnie dostarczać leki. Jednocześnie te niezwykłe właściwości, które czynią te cząstki tak użytecznymi, rodzą kluczowe pytanie: czy uszkadzają materiał genetyczny wewnątrz naszych komórek? W badaniu tym przeanalizowano szeroko działanie złotych nanorodzin w bakteriach, drożdżach i ludzkich komórkach nowotworu wątroby, aby sprawdzić, jak wchodzą one w interakcje z DNA i co to może oznaczać dla terapii medycznych oraz regulacji bezpieczeństwa. 
Od probówek po żywe komórki
Aby zbadać ryzyko i korzyści związane ze złotymi nanorodzinami, badacze najpierw przygotowali jednorodne cząstki w kształcie pręcików o długości około 50 nanometrów — zbyt małe, by zobaczyć je gołym okiem, ale na tyle małe, by łatwo przenikać do komórek. Następnie testowali te cząstki w kilku systemach biologicznych, które razem tworzyły swego rodzaju „pipeline toksyczności”. Dwie powszechne bakterie, Salmonella typhimurium i Escherichia coli, służyły jako szybkie, proste sensory uszkodzeń DNA. Specjalnie zaprojektowane szczepy drożdży z usuniętym pojedynczym genem związanym z odpowiedzią na stres lub śmiercią komórkową dostarczyły bardziej zbliżonego do ludzi modelu, ponieważ drożdże dzielą z nami wiele podstawowych szlaków. Na koniec ludzkie komórki raka wątroby (HepG2), szeroko stosowane w testach leków i chemikaliów, zostały wystawione na działanie złotych nanorodzin, aby zespół mógł śledzić zmiany w kluczowych genach związanych z rakiem.
Obserwacja rozrywającego DNA przypominającego ogon komety
W badaniach na bakteriach i drożdżach naukowcy polegali na czułej technice zwanej assay kometowym, aby „zobaczyć” uszkodzenia DNA w pojedynczych komórkach. W tej metodzie komórki zatapia się w żelu, delikatnie rozbija i umieszcza w polu elektrycznym. Nienaruszone DNA pozostaje głównie na miejscu, ale przerwane nici przemieszczają się, tworząc kształt przypominający kometę z jasną głową i ogonem. Mierząc długość i intensywność ogona, badacze mogą oszacować zakres uszkodzeń genetycznych. Zarówno w Salmonella, jak i E. coli, złote nanorodziny powodowały wyraźne, zależne od dawki wzrosty wszystkich miar kometowych: więcej komórek z ogonami, dłuższe ogony i wyższy odsetek DNA przesunięty do ogona. Szczepy drożdży typu knockout wykazały podobny wzorzec, przy czym niektóre szczepy — szczególnie te pozbawione genów związanych ze stresem i funkcją mitochondriów — wykazywały znacznie większe fragmentowanie DNA niż normalne drożdże. 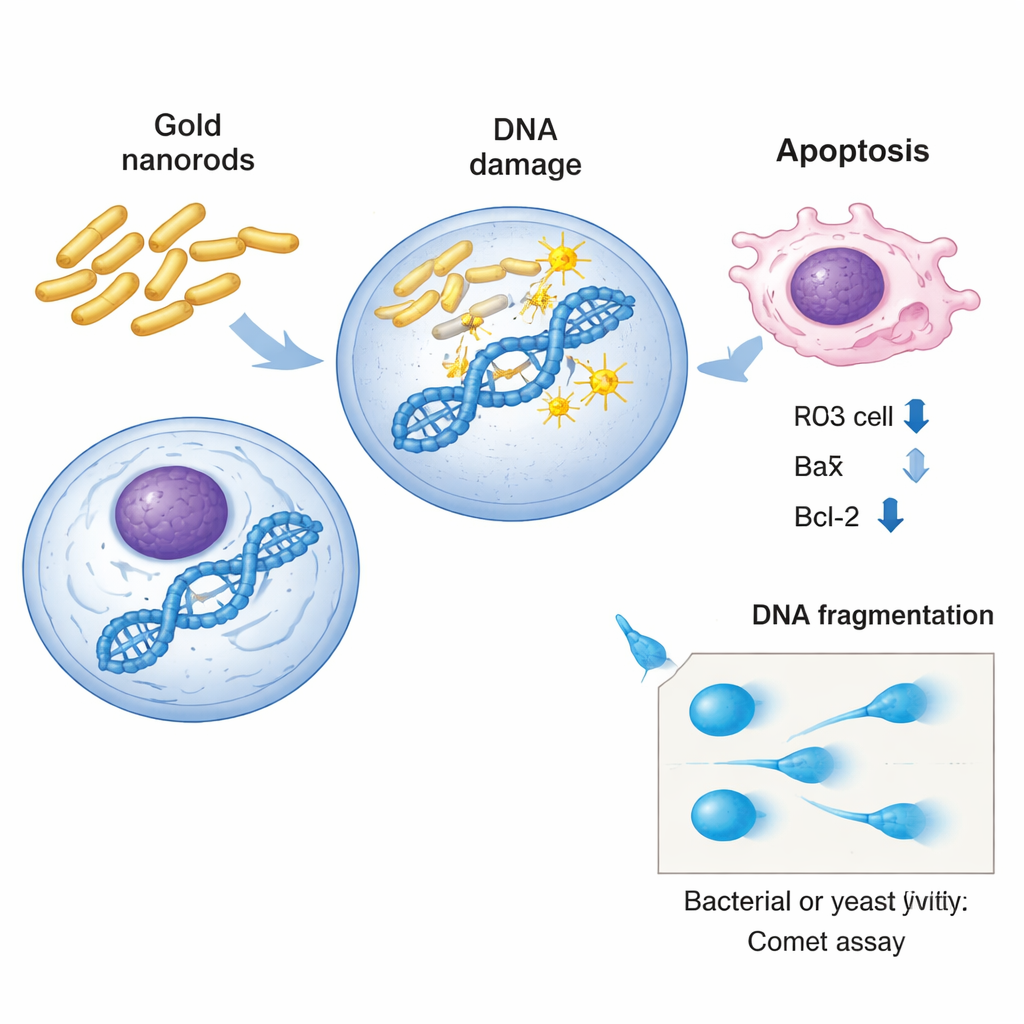
Sieci genów i sygnały śmierci w komórkach ludzkich
W ludzkich komórkach raka wątroby zespół zbadał głębiej, wykraczając poza fizyczne pęknięcia DNA, aby zobaczyć, jak reagują wewnętrzne systemy kontrolne komórek. Z użyciem reakcji PCR w czasie rzeczywistym zmierzono aktywność trzech dobrze znanych strażników i egzekutorów losu komórki: p53 i Bax, które promują śmierć komórkową, gdy wykryte zostanie uszkodzenie, oraz Bcl-2, który pomaga komórkom przeżyć. Po ekspozycji na półsilne toksyczne dawki złotych nanorodzin poziomy p53 i Bax wzrosły, podczas gdy poziom Bcl-2 spadł — molekularny znak zaprogramowanej śmierci komórki (apoptozy). Innymi słowy, nanorodziny nie tylko uszkadzały DNA, ale też popychały komórki nowotworowe w kierunku autodestrukcji. Aby powiązać wyniki z drożdży z biologią ludzką, badacze użyli platformy GeneMANIA do zmapowania sieci interakcji wokół usuniętych genów drożdżowych. Analiza ta wykazała gęste sieci interakcji fizycznych i genetycznych związanych z odpowiedzią na stres, naprawą DNA i funkcją mitochondriów, co wzmacnia tezę, że podobne szlaki są wrażliwe zarówno w drożdżach, jak i w komórkach ludzkich.
Równoważenie obietnicy medycznej z ryzykiem genetycznym
W sumie te eksperymenty malują zniuansowany obraz złotych nanorodzin. Z jednej strony wyraźnie mogą one uszkadzać DNA w bardzo różnych organizmach, a uszkodzenia nasilają się wraz ze wzrostem dawki. Pewne tła genetyczne, takie jak szczepy drożdży pozbawione specyficznych genów związanych ze stresem lub mitochondriami, są szczególnie wrażliwe, co sugeruje, że osoby o określonych cechach genetycznych mogą również reagować odmiennie. Z drugiej strony w ludzkich komórkach raka wątroby te uszkodzenia DNA i wynikająca z nich aktywacja ścieżek śmierci mogą być dokładnie tym, czego lekarze oczekują przy celowaniu w guzy. Dla czytelnika niebędącego specjalistą kluczowe przesłanie jest takie, że złote nanorodziny to potężne narzędzia, które mogą zarówno pomagać, jak i szkodzić: potrafią zabić komórki nowotworowe, ale też stwarzają ryzyko genetyczne dla innych komórek i środowiska. Autorzy argumentują, że przyszłe zastosowania medyczne tych cząstek muszą starannie ważyć dawkowanie, docelowe dostarczanie i genetykę pacjentów, aby wykorzystać ich korzyści przy jednoczesnym kontrolowaniu potencjału genotoksycznego.
Cytowanie: Rashad, S.E., Haggran, A.A. & Abdoon, A.S.S. Comprehensive assessment of gold nanorod-induced genotoxicity using multi-model biological systems. Sci Rep 16, 5429 (2026). https://doi.org/10.1038/s41598-026-36119-8
Słowa kluczowe: złote nanorodziny, uszkodzenia DNA, nanotoksykologia, terapia przeciwnowotworowa, testy genotoksyczności